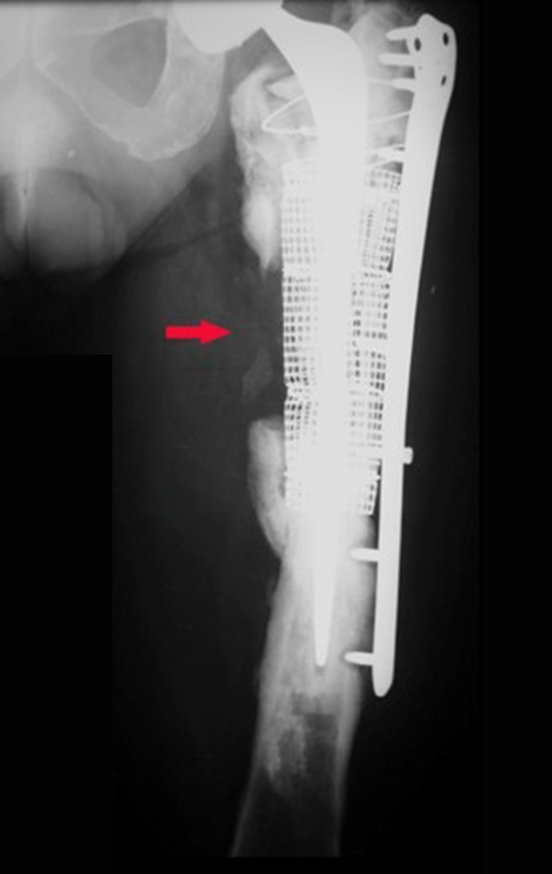
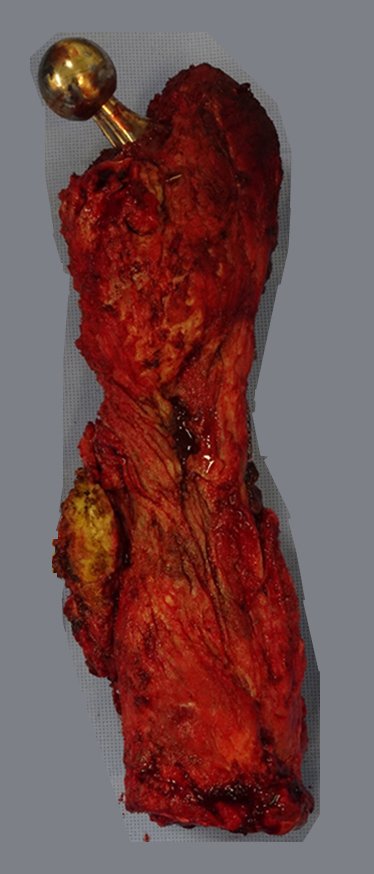
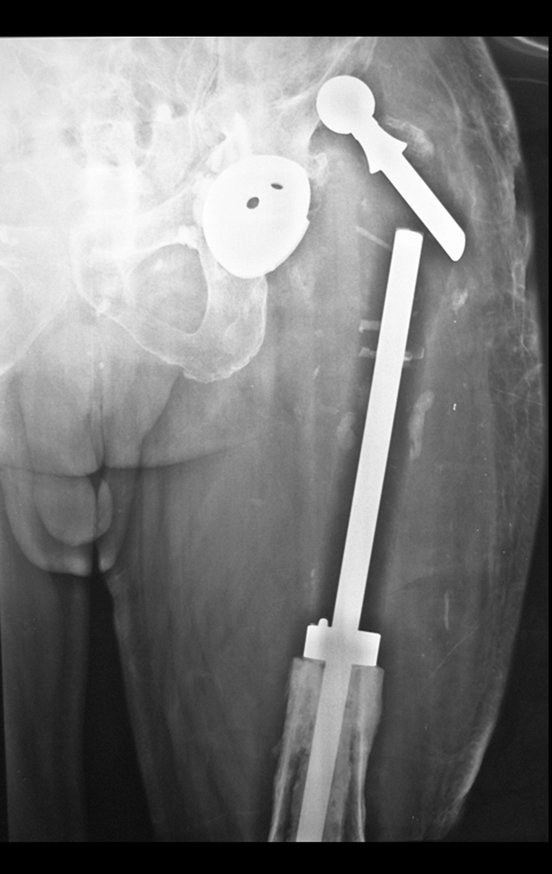
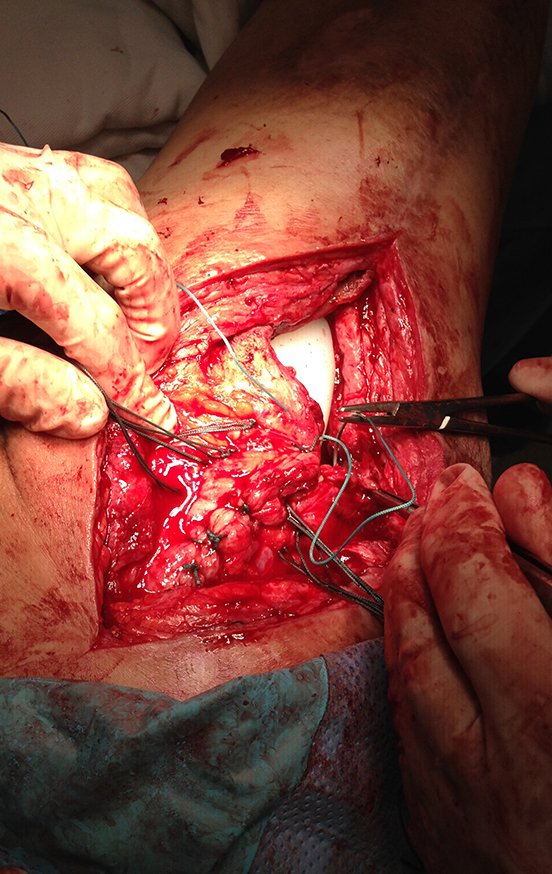
Técnica de revisión de prótesis de cadera infectada – Artrosis por necrosis de cabeza femoral – Aflojamiento y rotura de prótesis, infección y fractura.

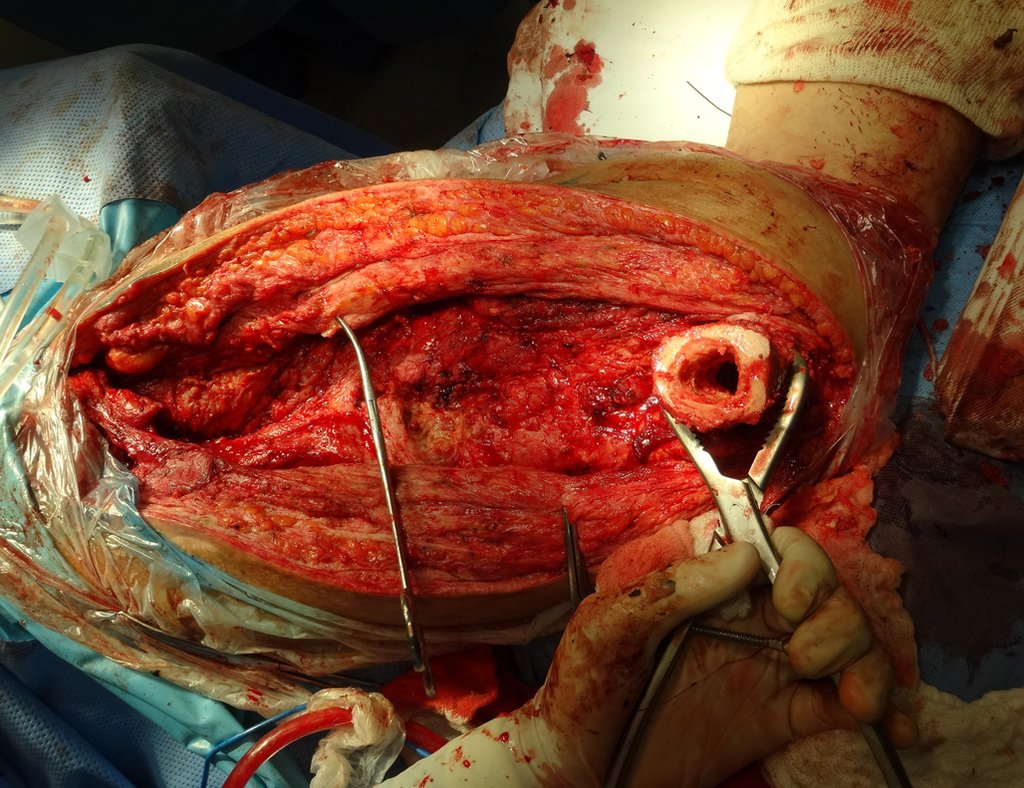
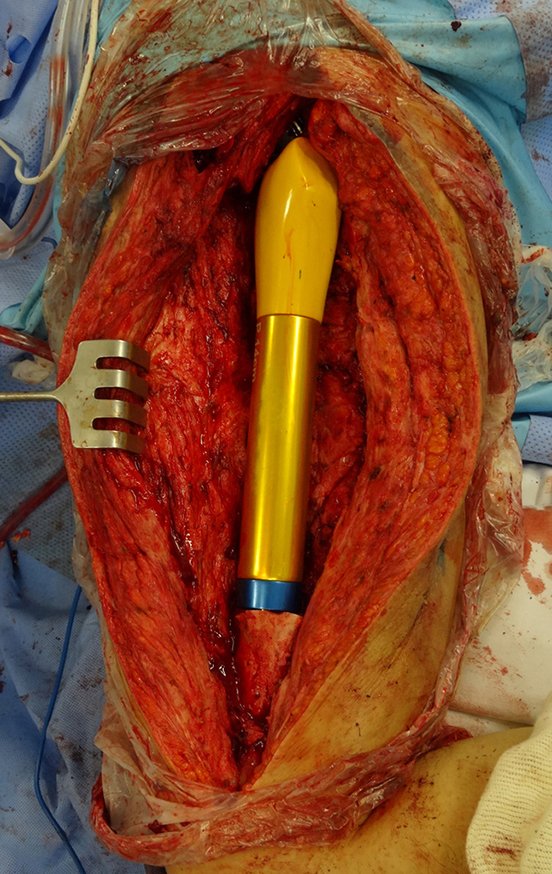
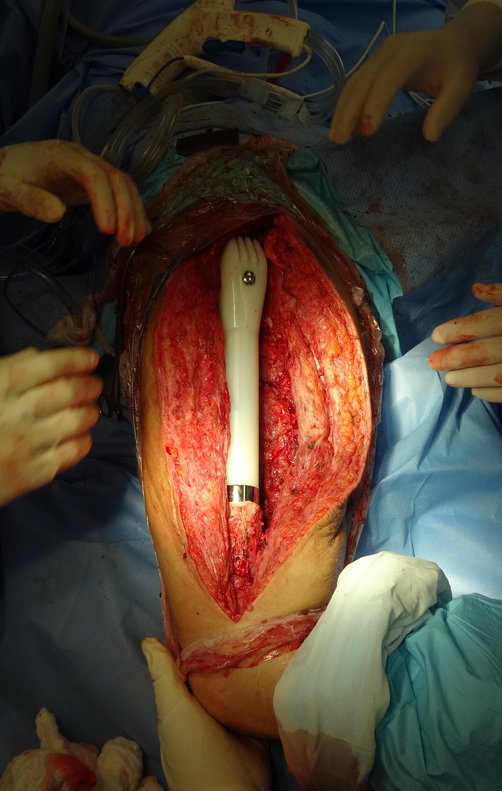
Alrededor de cualquier endoprótesis se forma fibrosis como resultado de una reacción a un cuerpo extraño, dando como resultado una pseudocápsula gruesa, formando una carcasa que prácticamente aísla esta endoprótesis del cuerpo.
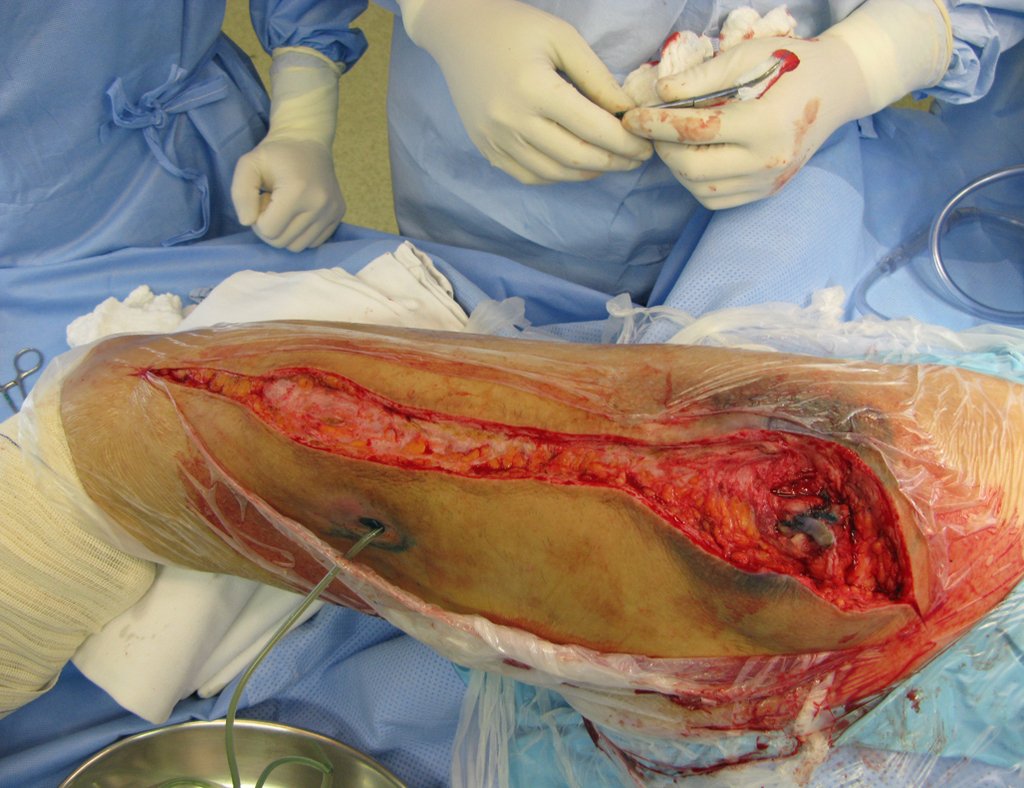
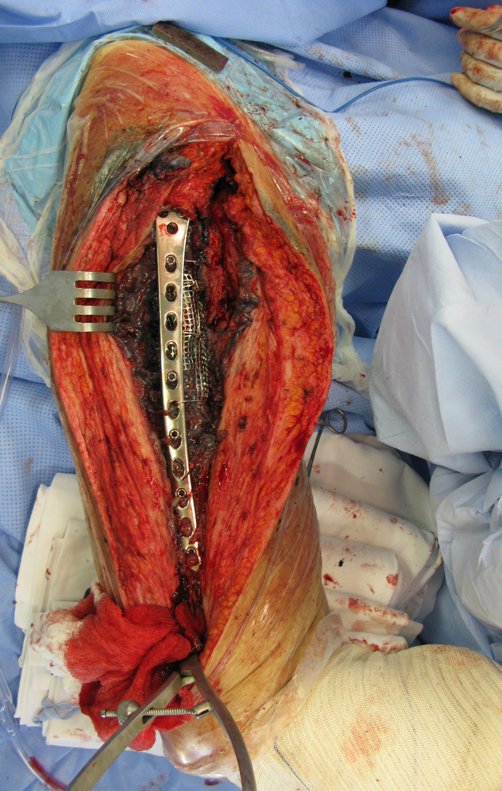
Los músculos y tendones, que inicialmente se insertaron en la prótesis con hilos de ethibond, acaban adhiriéndose definitivamente a esta pseudocápsula. Esta pseudocápsula tiene un revestimiento de epitelio sinovial secretor de líquido, que acaba recubriendo la endoprótesis. Esta fibrosis reactiva de la pseudocápsula puede alcanzar los 5 mm de espesor.
En revisiones e incluso en cirugías con desprendimiento muscular importante, puede ocurrir un aumento del espacio muerto, dando como resultado la formación de exceso de líquido sinovial, lo que aumenta la ¨funda¨ que rodea la prótesis.
Este aumento de volumen, asociado a la debilidad de los músculos abductores, puede facilitar la luxación de cadera.
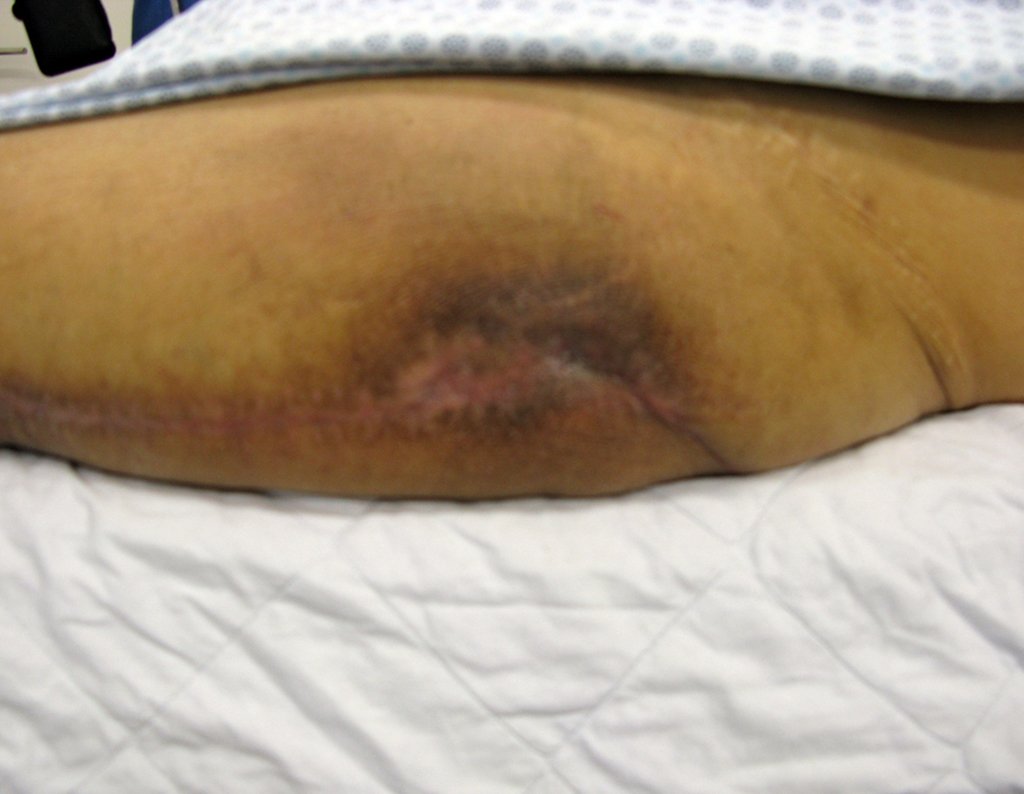
El 15 de mayo de 2014, un mes después de la cirugía, la paciente regresó con aumento de volumen del muslo, sin fiebre, sin calor local y signos de exceso de contenido líquido alrededor de la prótesis.
Este líquido, cuando sobra, hay que escurrirlo. A veces es necesario más de un procedimiento.
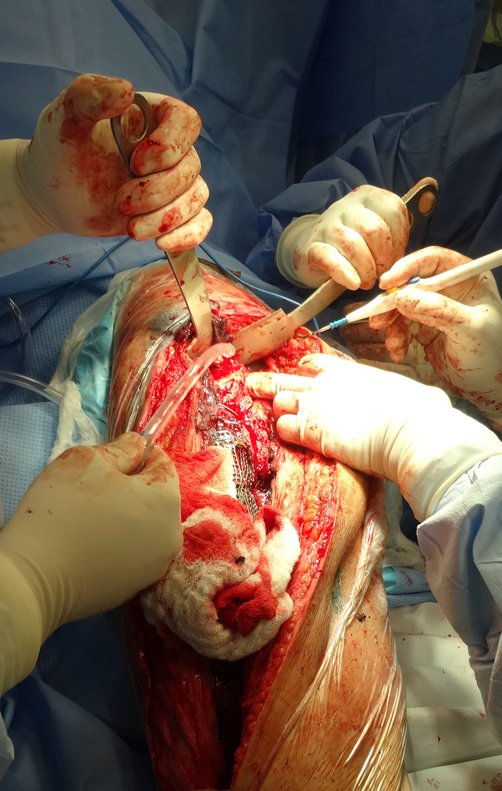
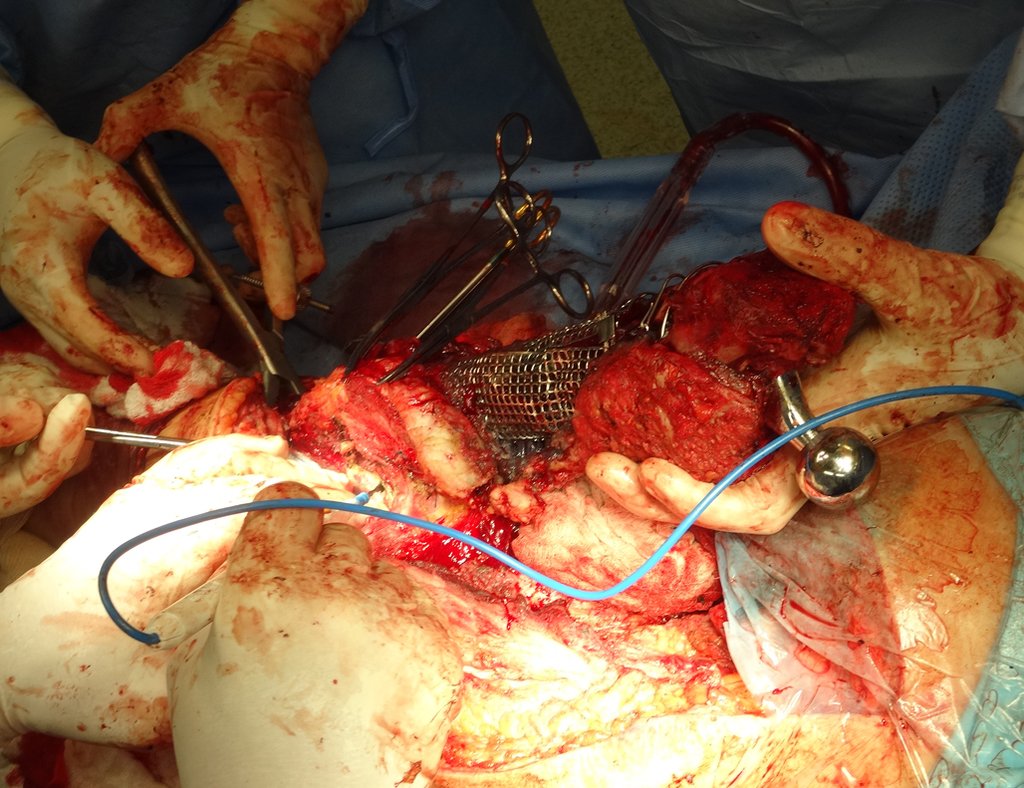
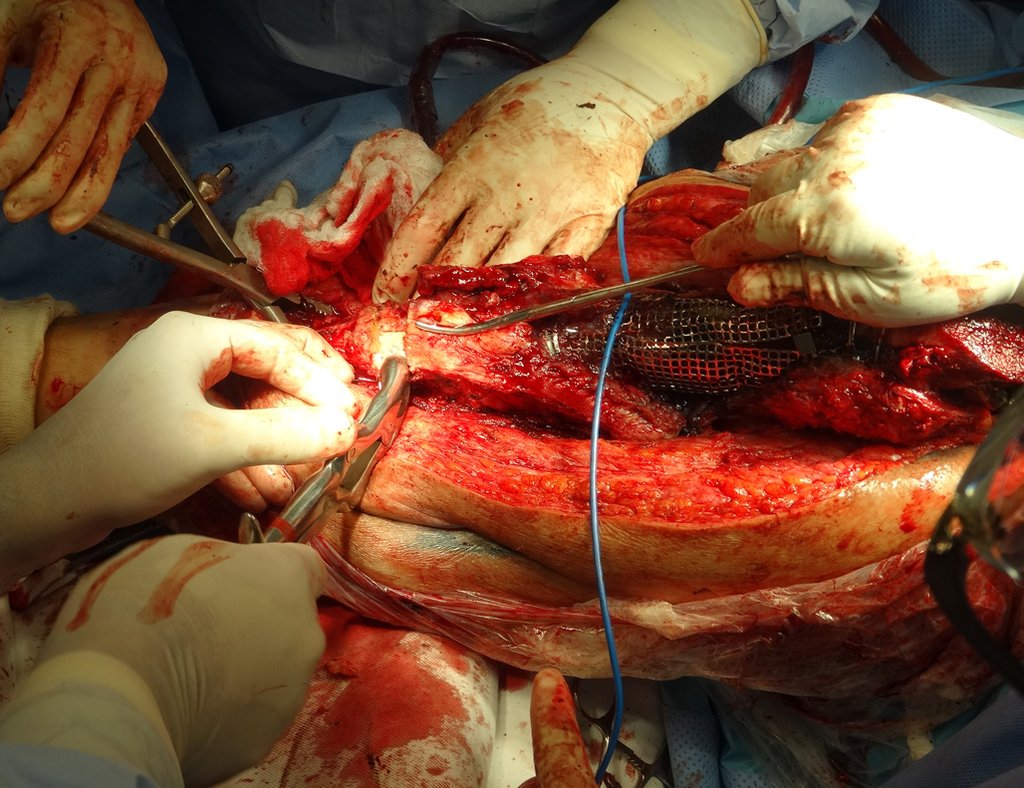
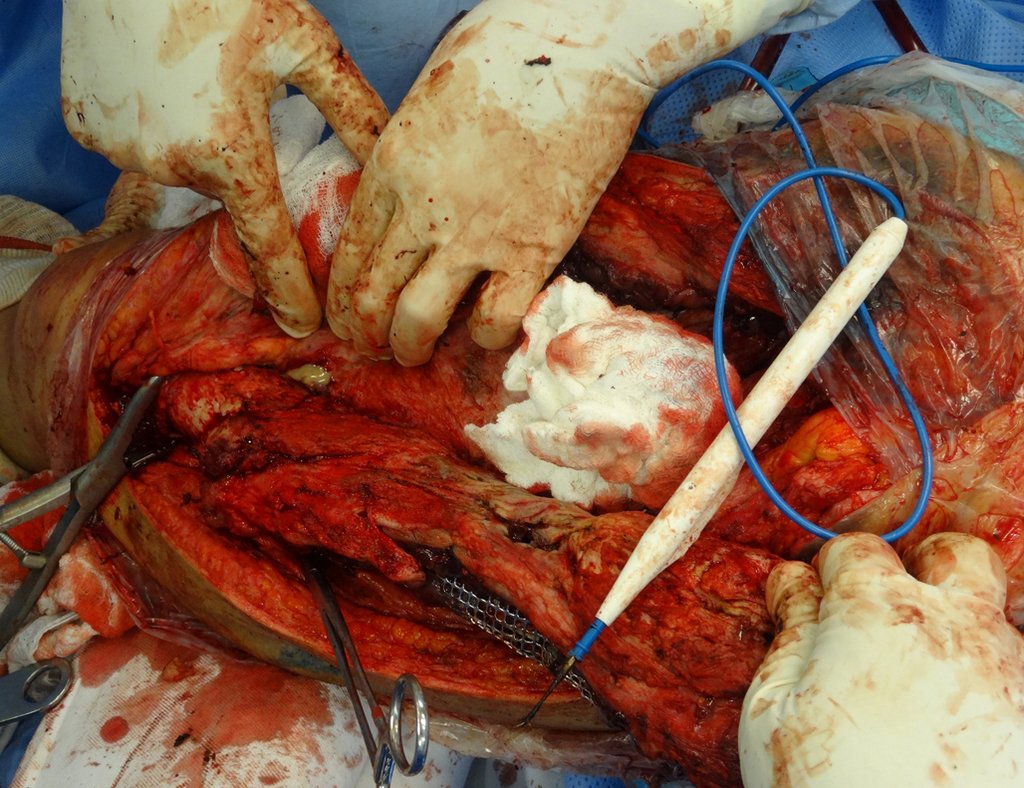
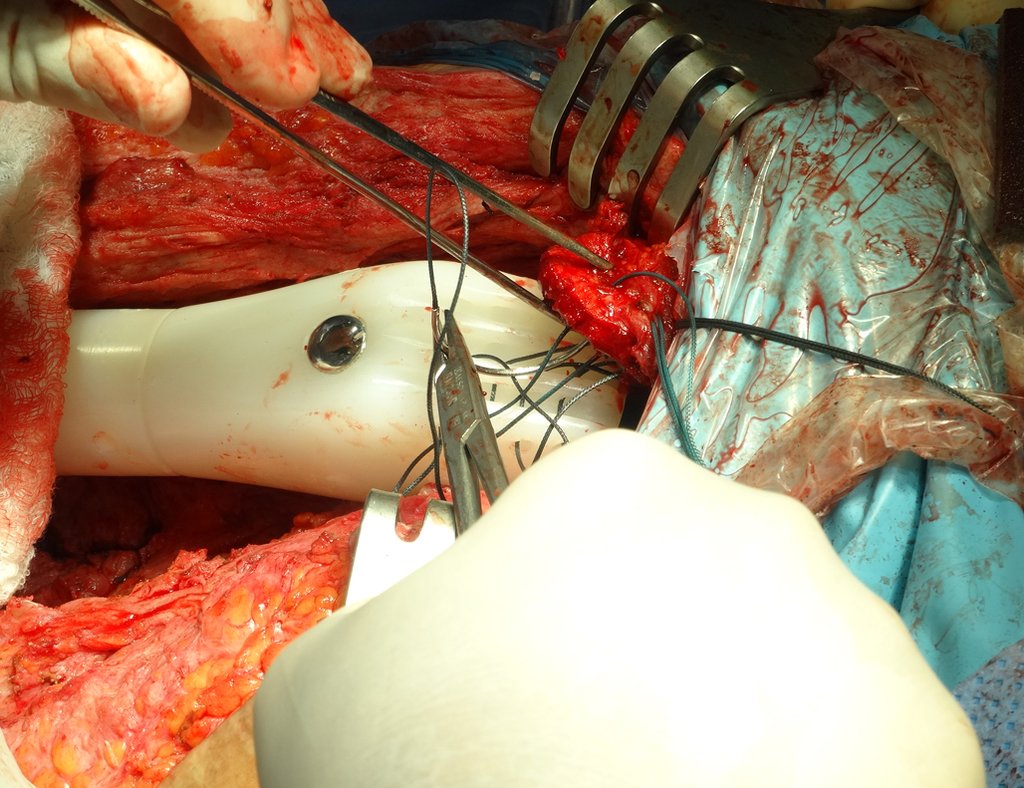
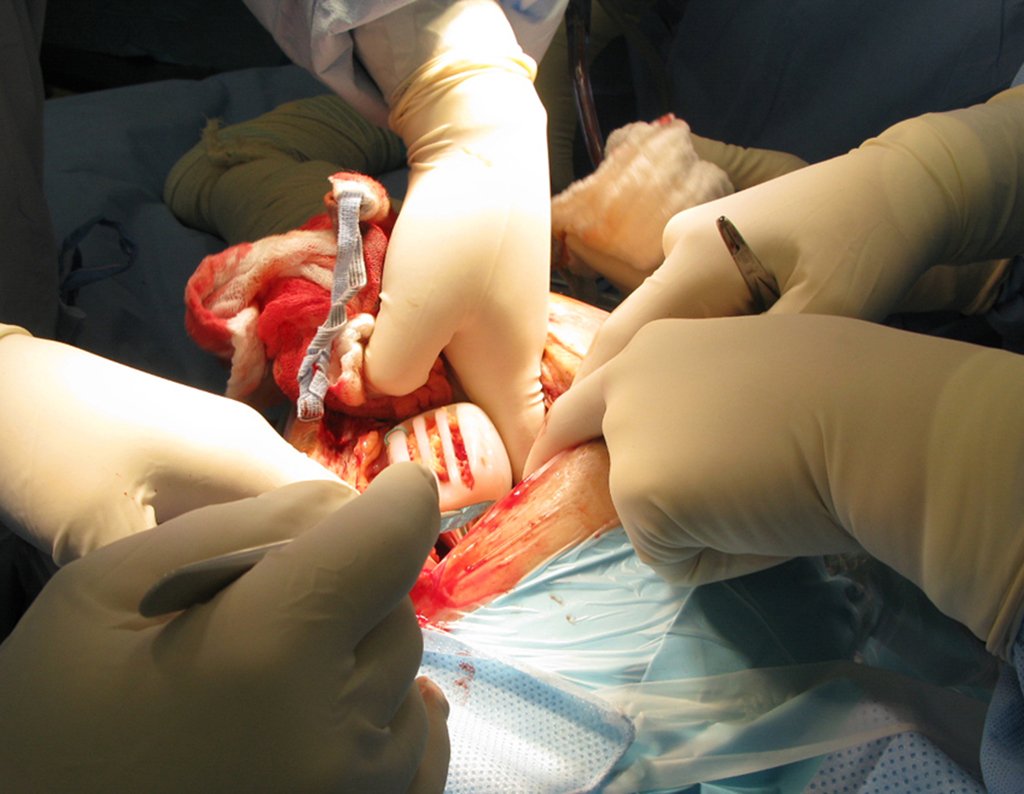
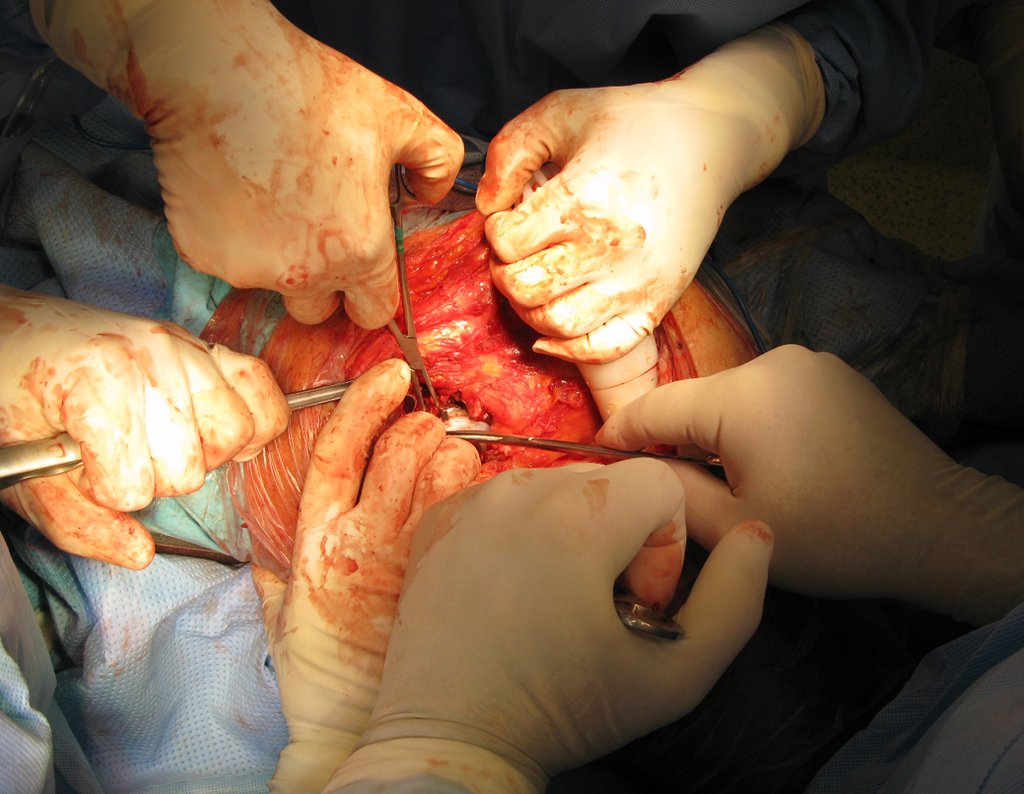
Se debe realizar con total asepsia, utilizando una aguja de gran calibre y vaciando al máximo el contenido, figuras 62 a 64.
Se realizó nuevo drenaje mediante punción, el 28/05/2015, después de dos semanas.
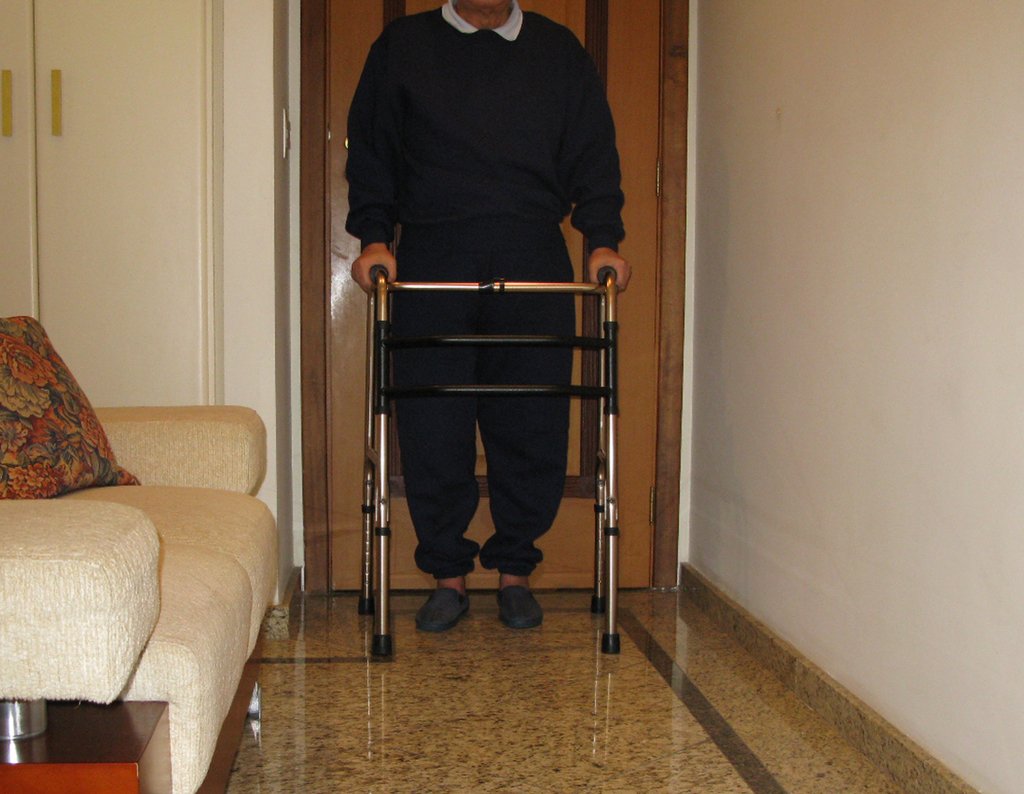
El paciente ya podía caminar con andador y no tuvo recurrencia de la infección, figuras 65 a 67.
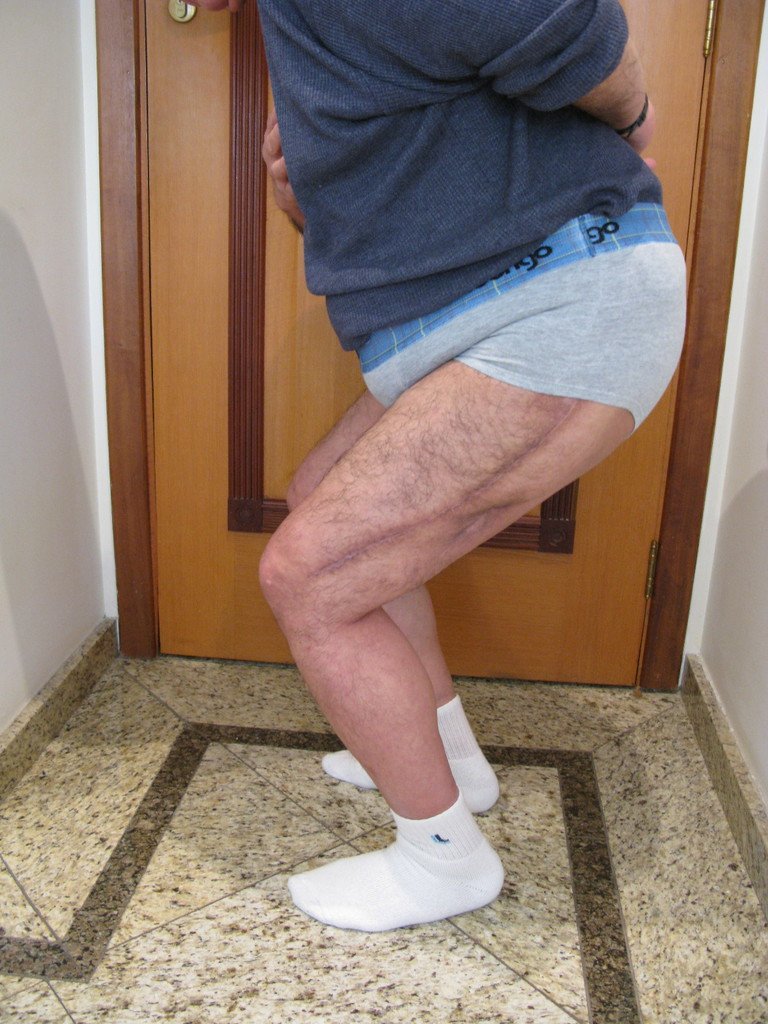
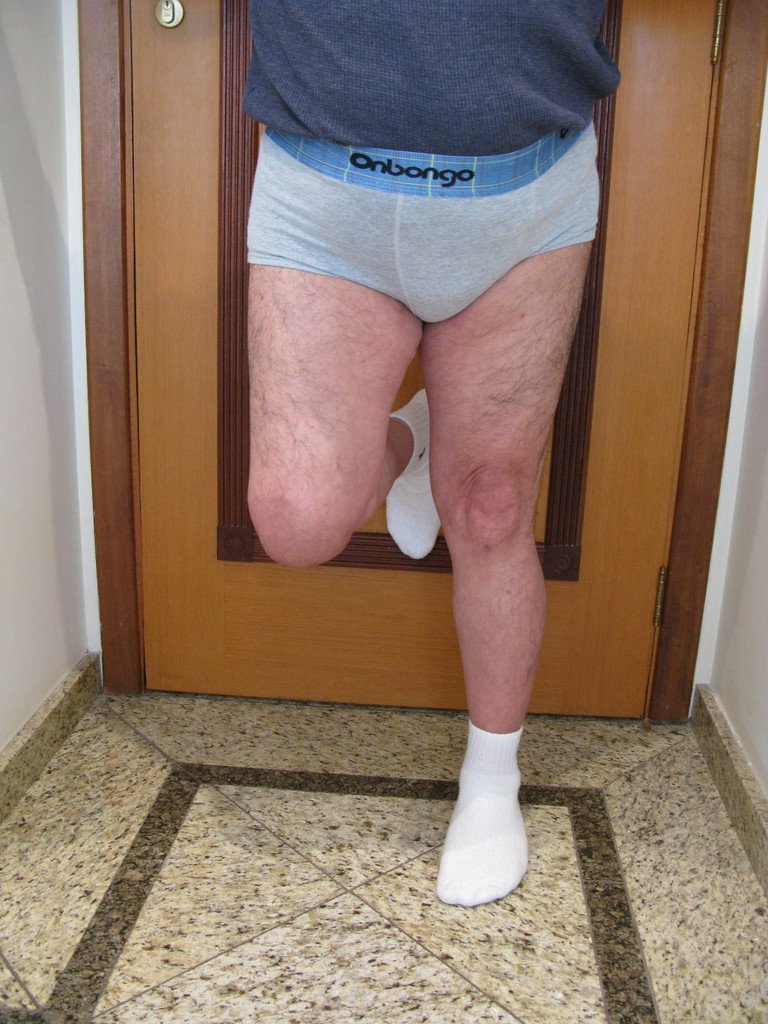
En junio de 2014 realizó un movimiento de hiperflexión y rotación interna, estando sentado en un inodoro bajo, presentando luxación de cadera. Se realizó reducción cerrada y volvimos a reorientar respecto a los movimientos que facilitaban la luxación, al existir importante hipotrofia del glúteo medio, lo que dificultó aún más la estabilización de la prótesis.
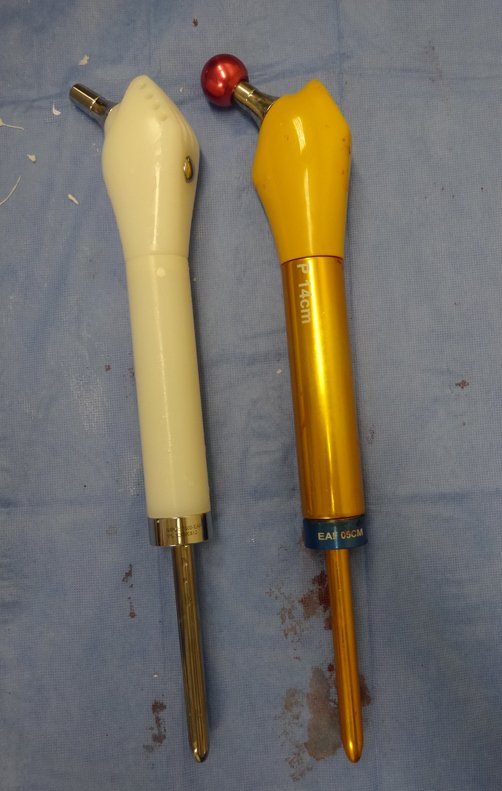
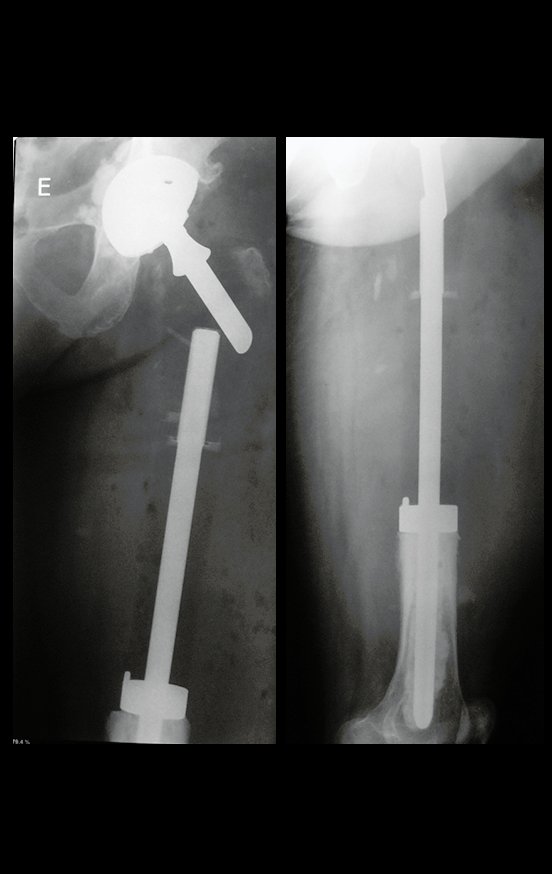
Un nuevo episodio de luxación en julio de 2014, tres meses después de la cirugía. Realizamos maniobras de reducción bajo radioscopia, sin necesidad de sedación y obtuvimos fácil reducción y también fácil desplazamiento, comprobando la imposibilidad de contener la cadera reducida, debido a la insuficiencia de los músculos abductores y de la cabeza femoral que utilizamos, que era pequeña en tamaño, figuras 65 a 67 .
Autor: Profr. Dr. Pedro Péricles Ribeiro Baptista
Oncocirugía Ortopédica en el Instituto Oncológico Dr. Arnaldo Vieira de Carvalho
Oficina : Rua General Jardim, 846 – Cj 41 – Cep: 01223-010 Higienópolis São Paulo – SP
Teléfono: +55 11 3231-4638 Celular:+55 11 99863-5577 Correo electrónico: drpprb@gmail.com