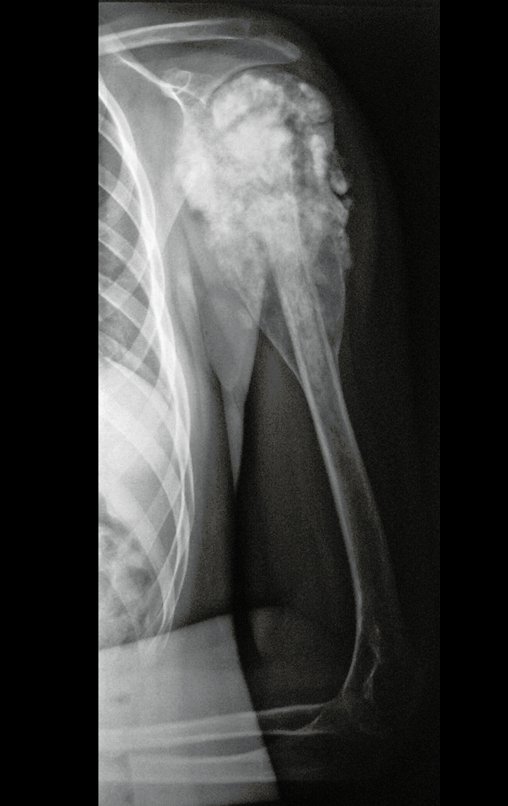
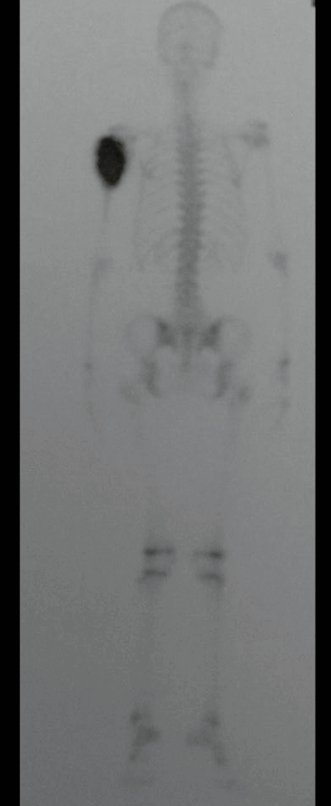
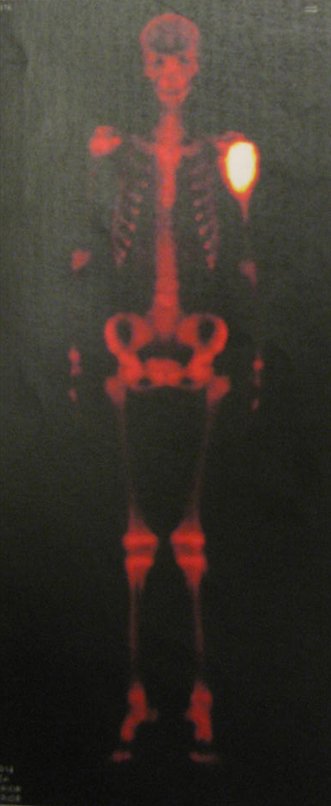
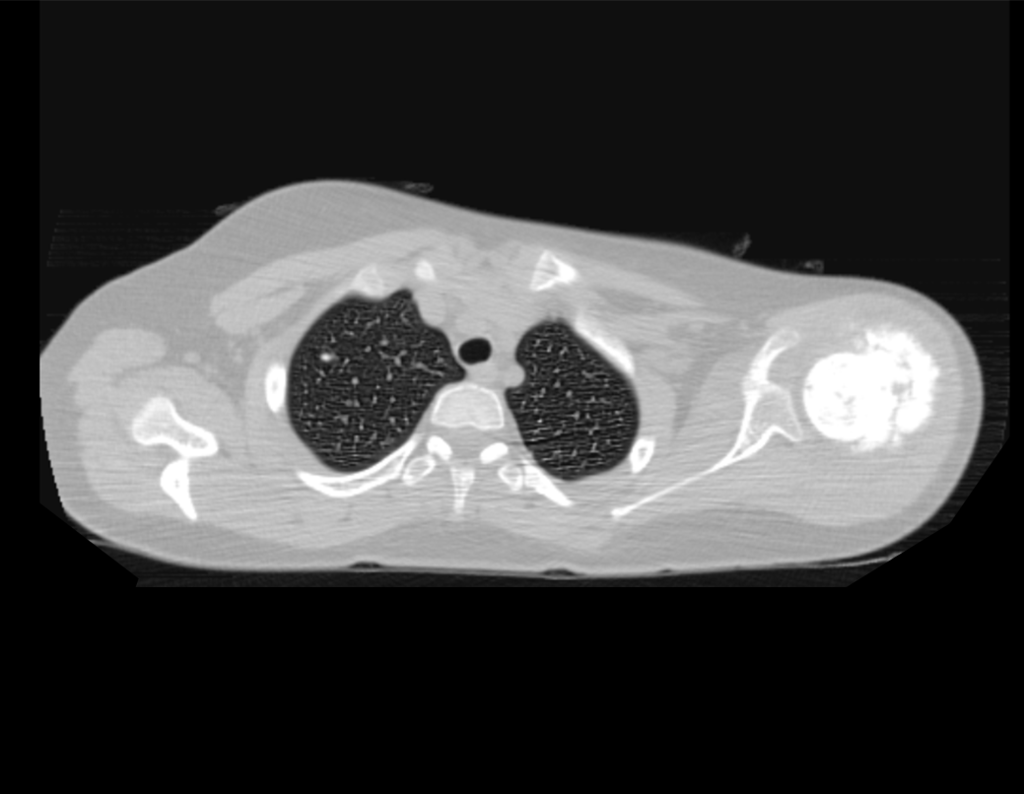
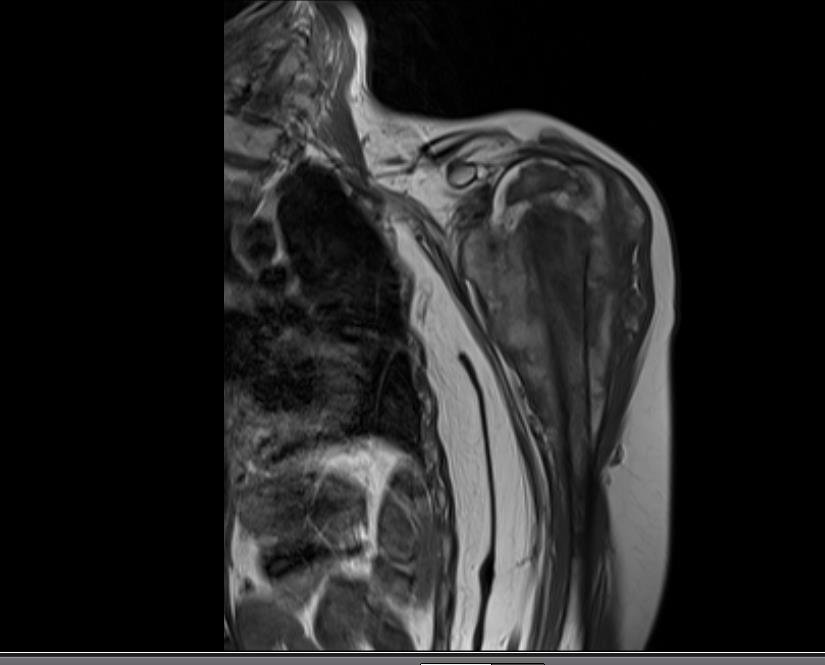
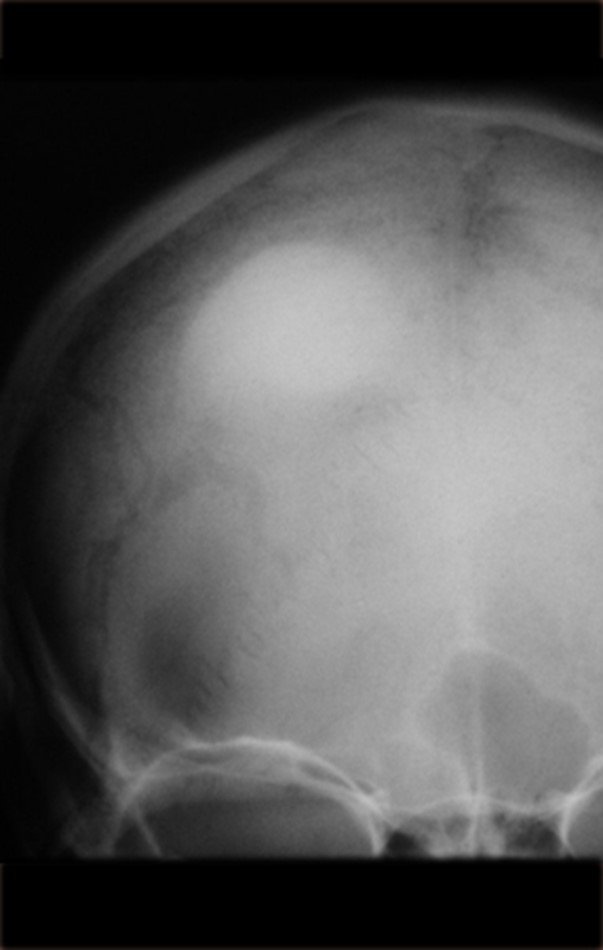
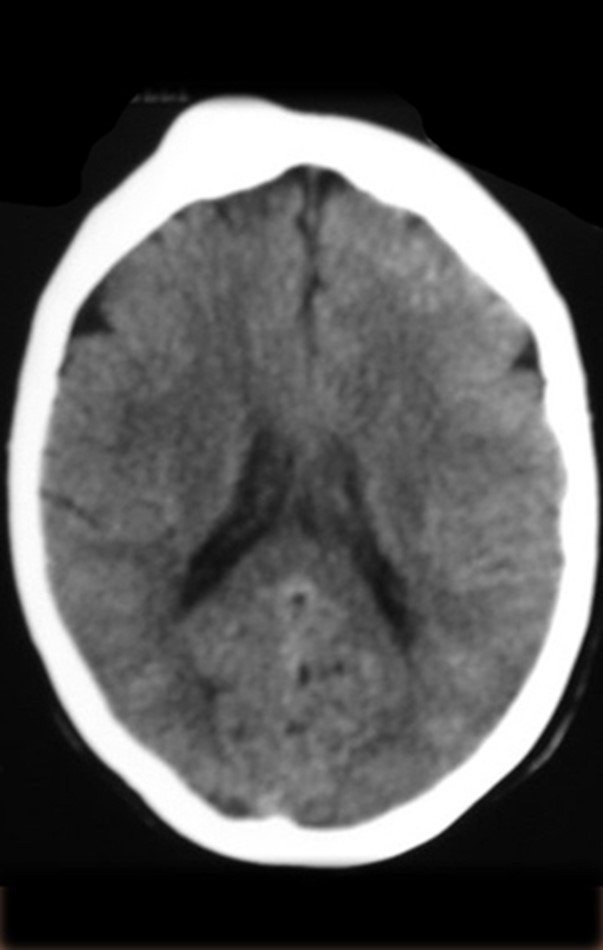
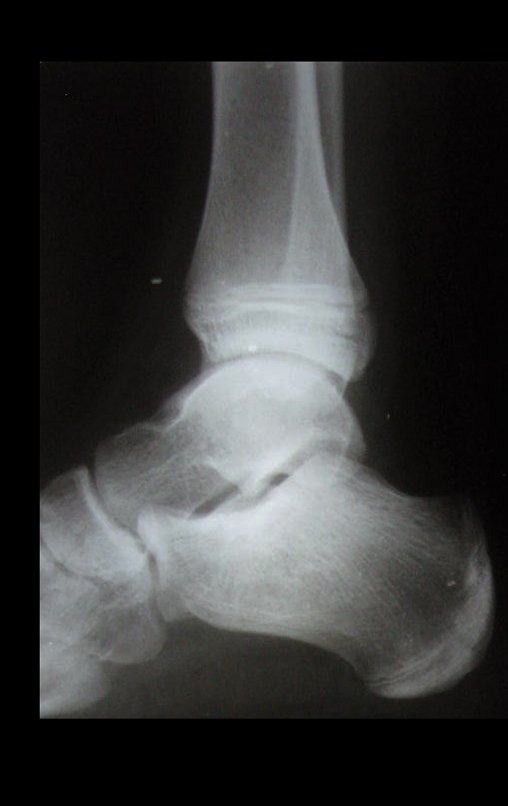
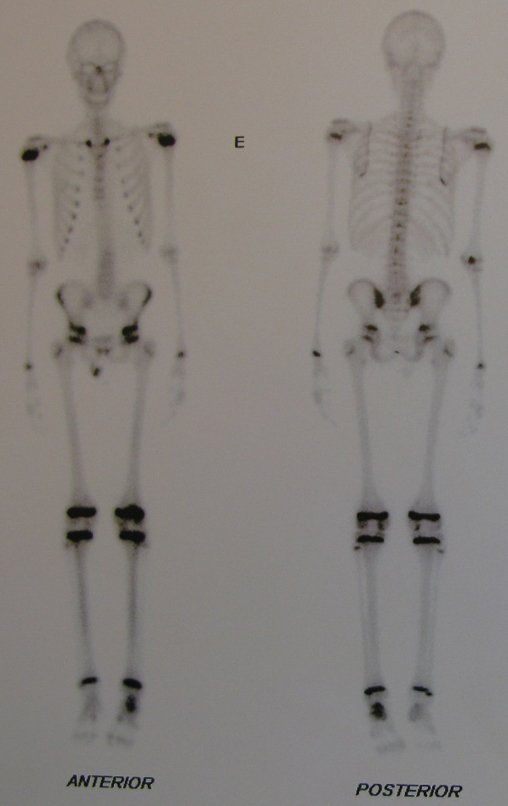
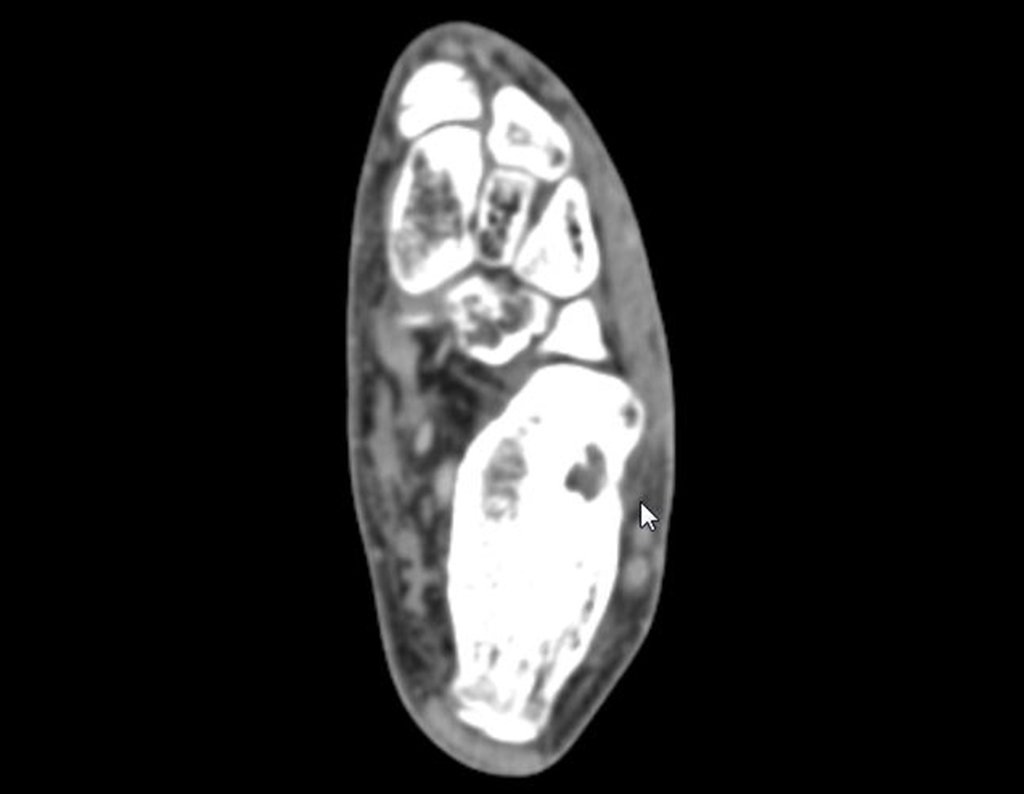
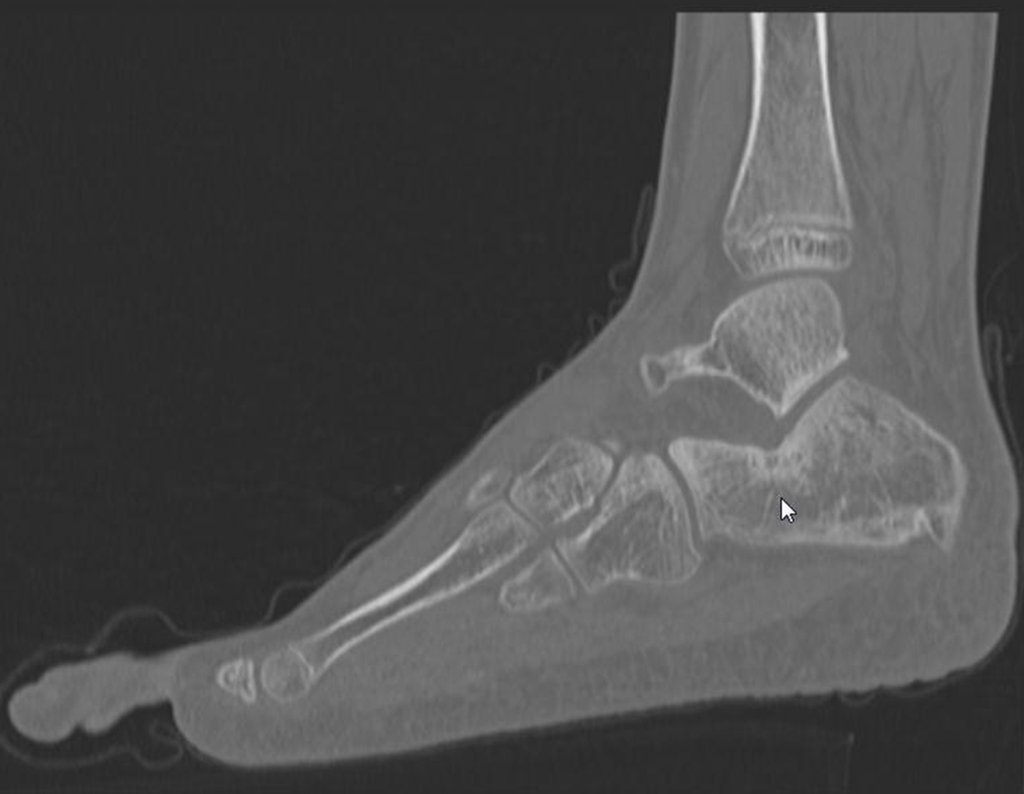
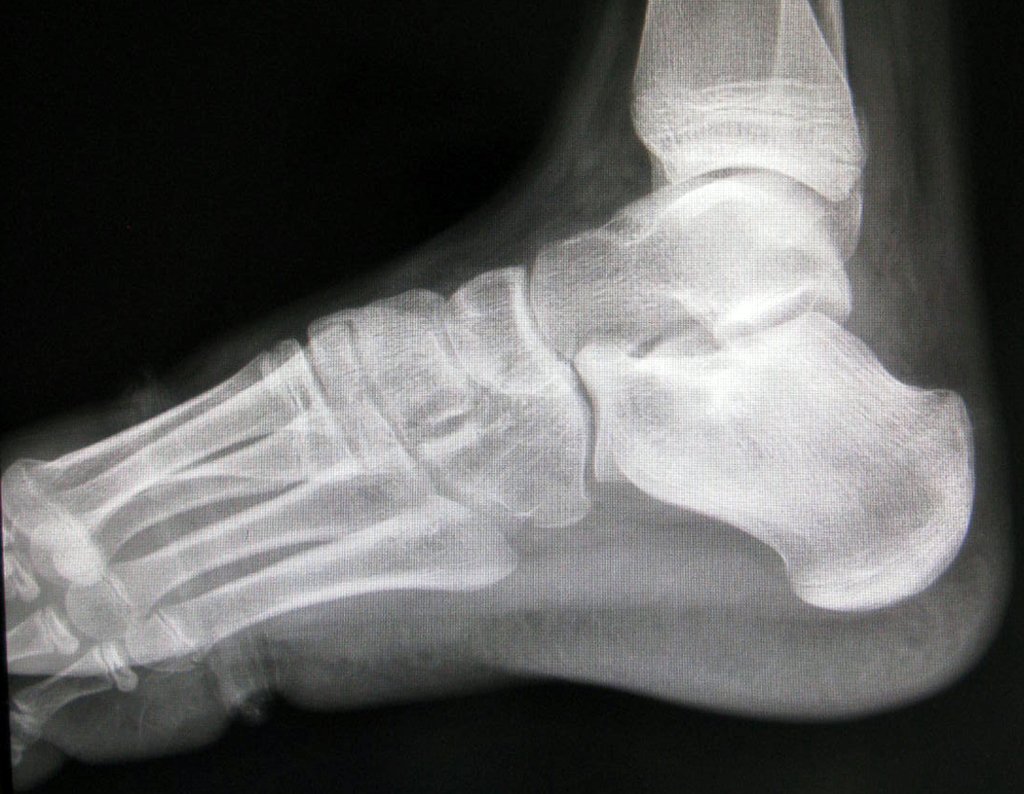
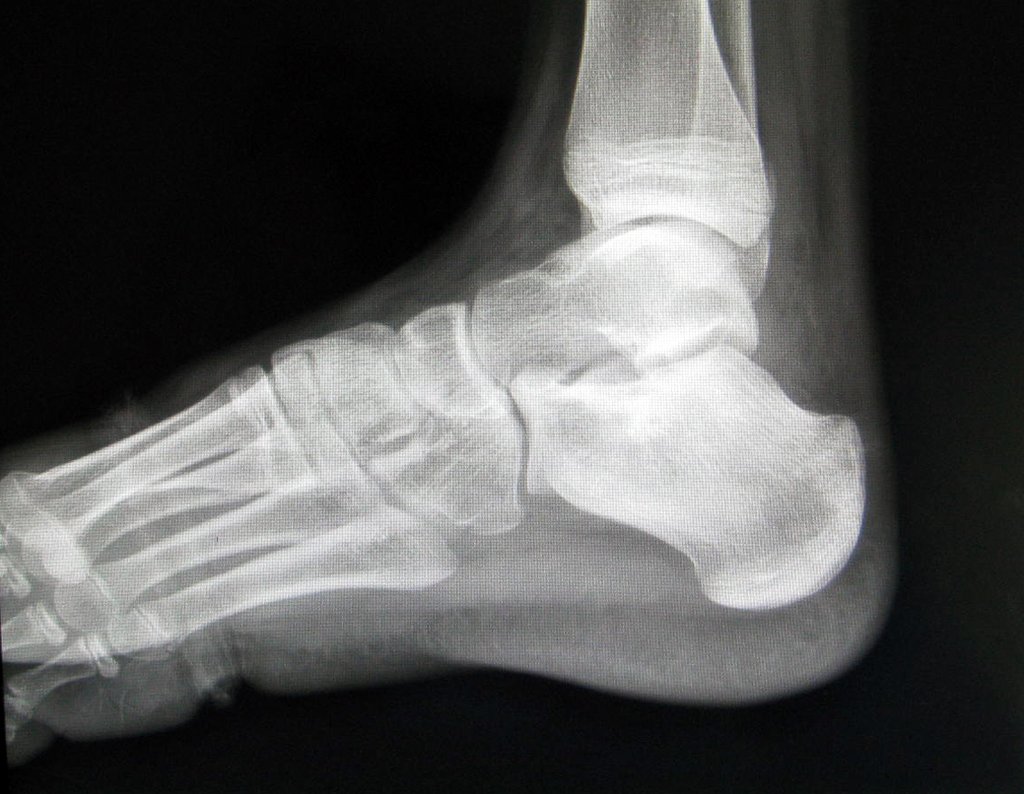
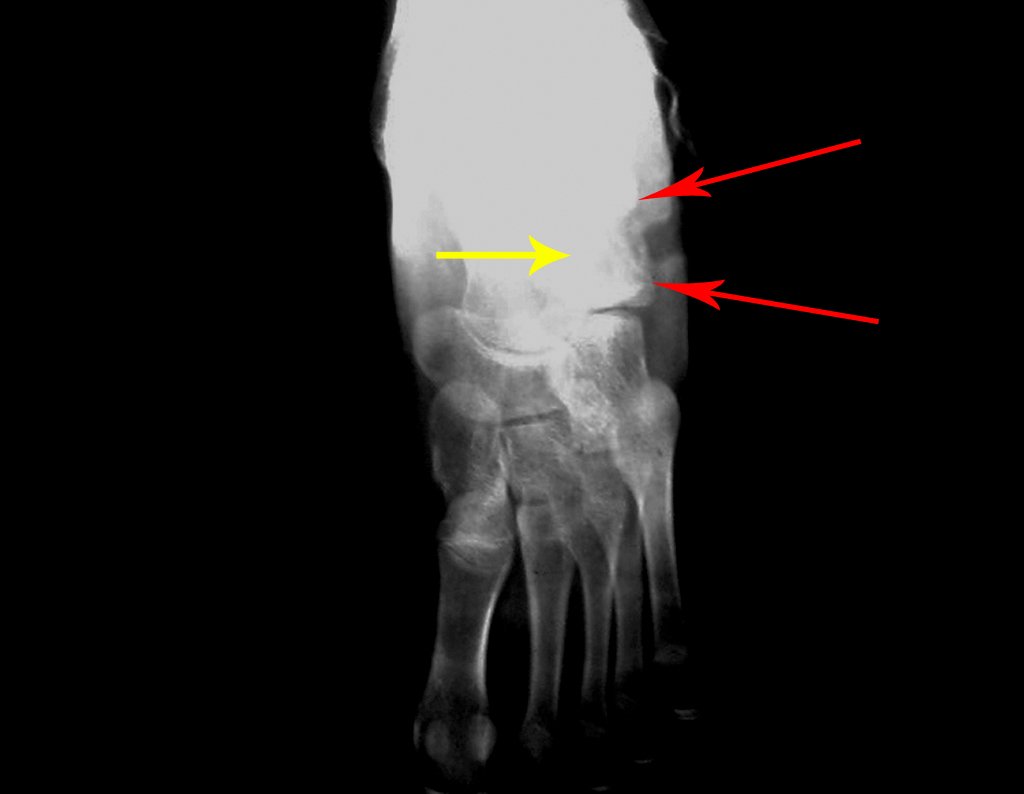
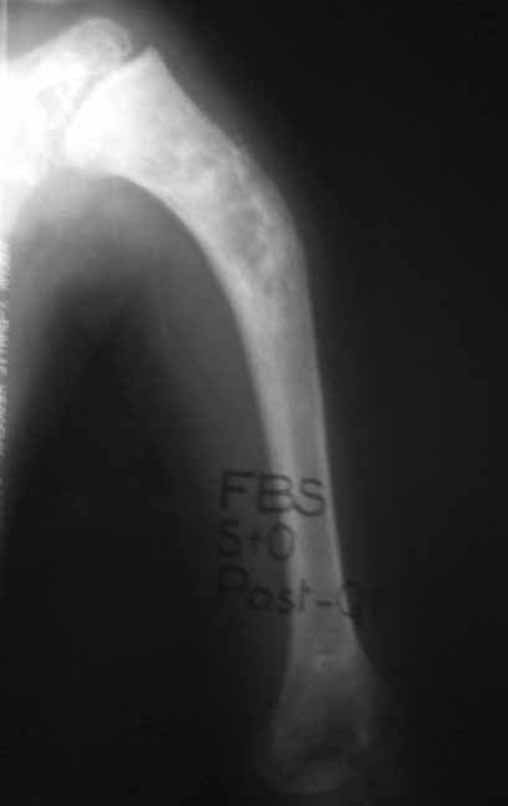
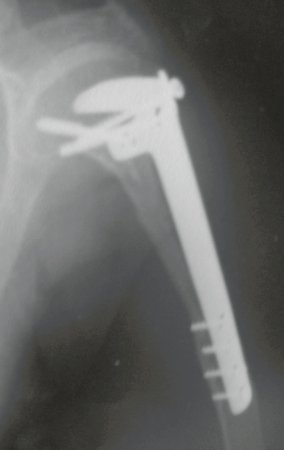
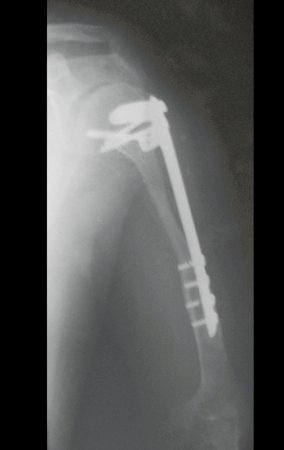
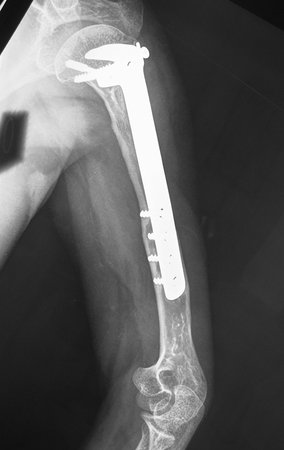
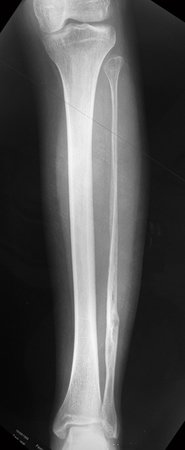
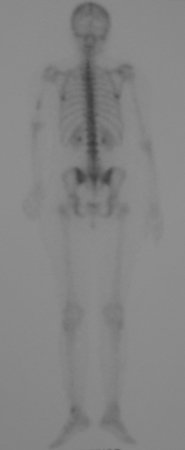
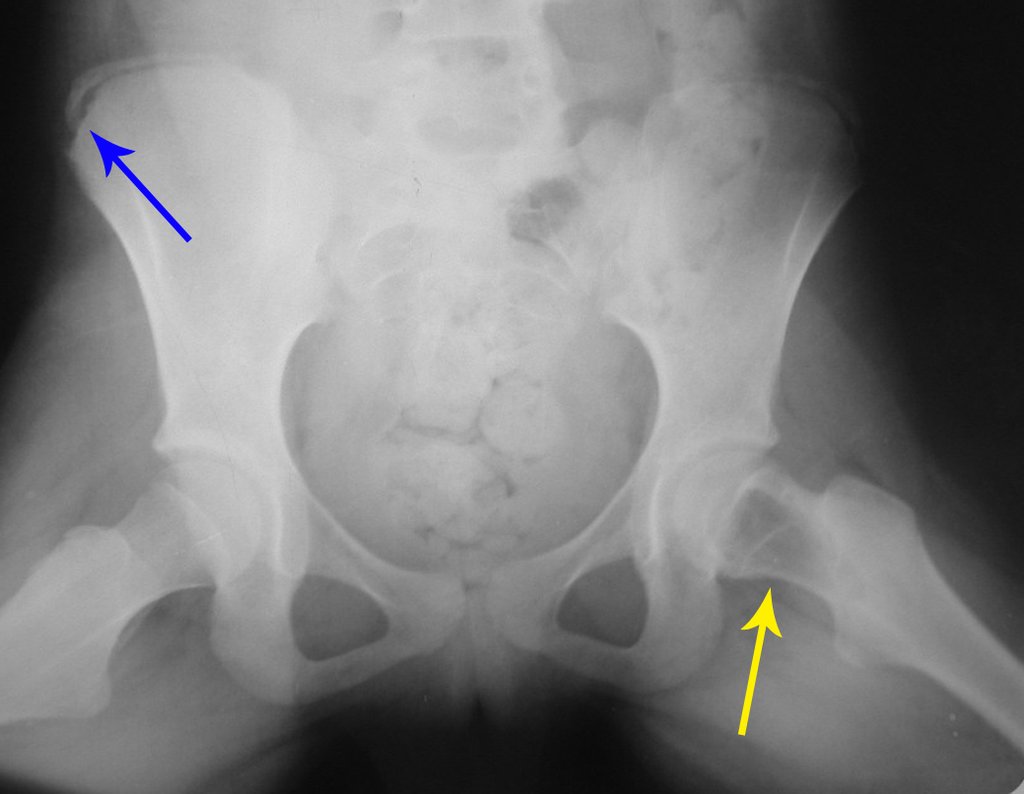
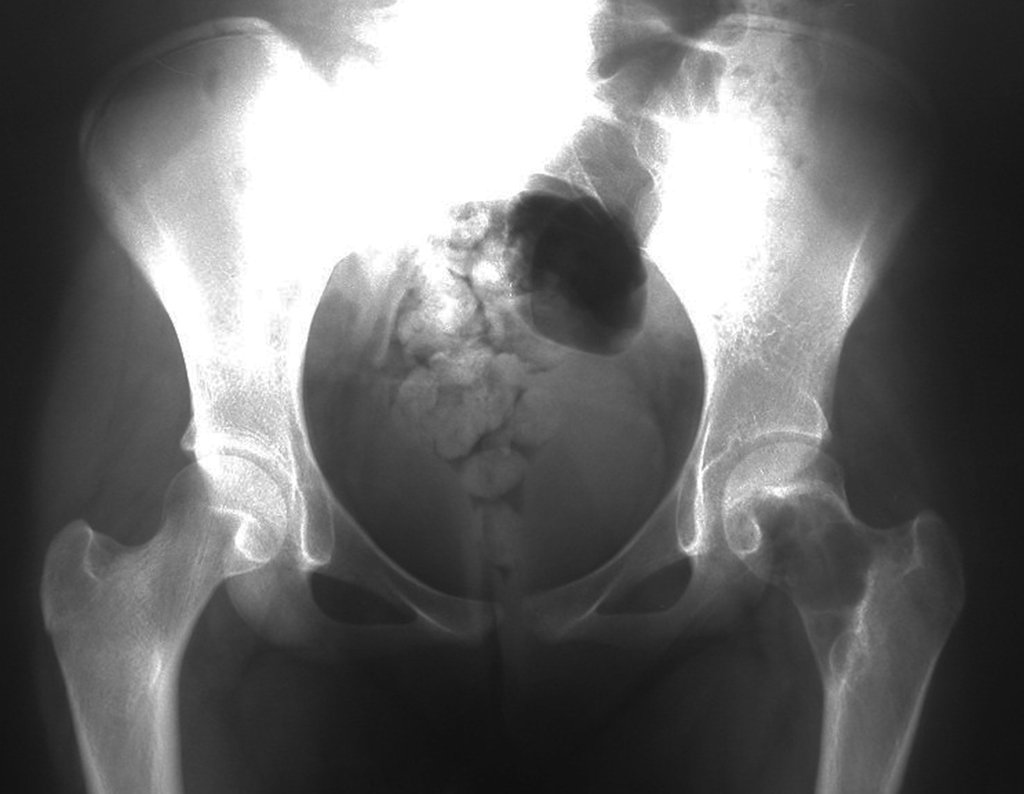
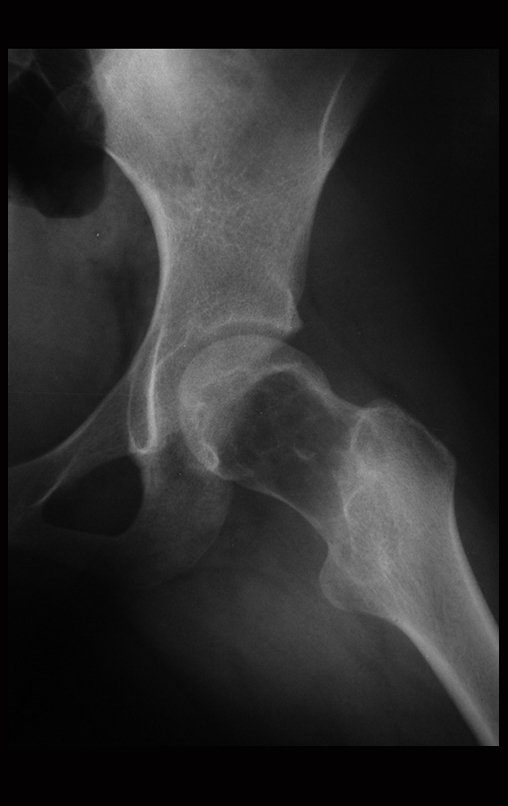
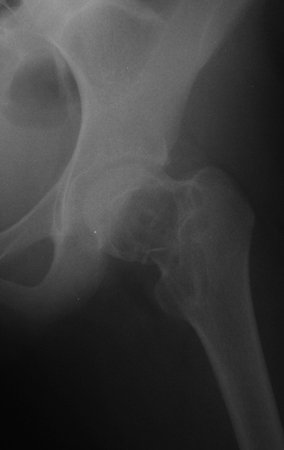
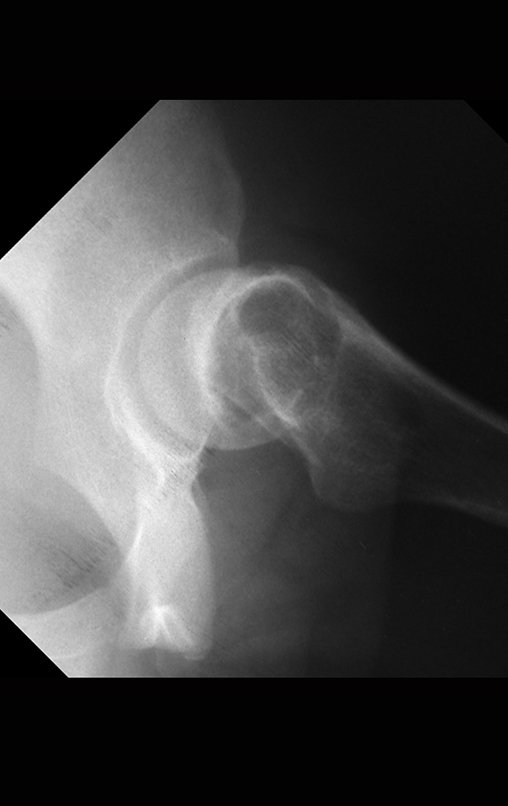
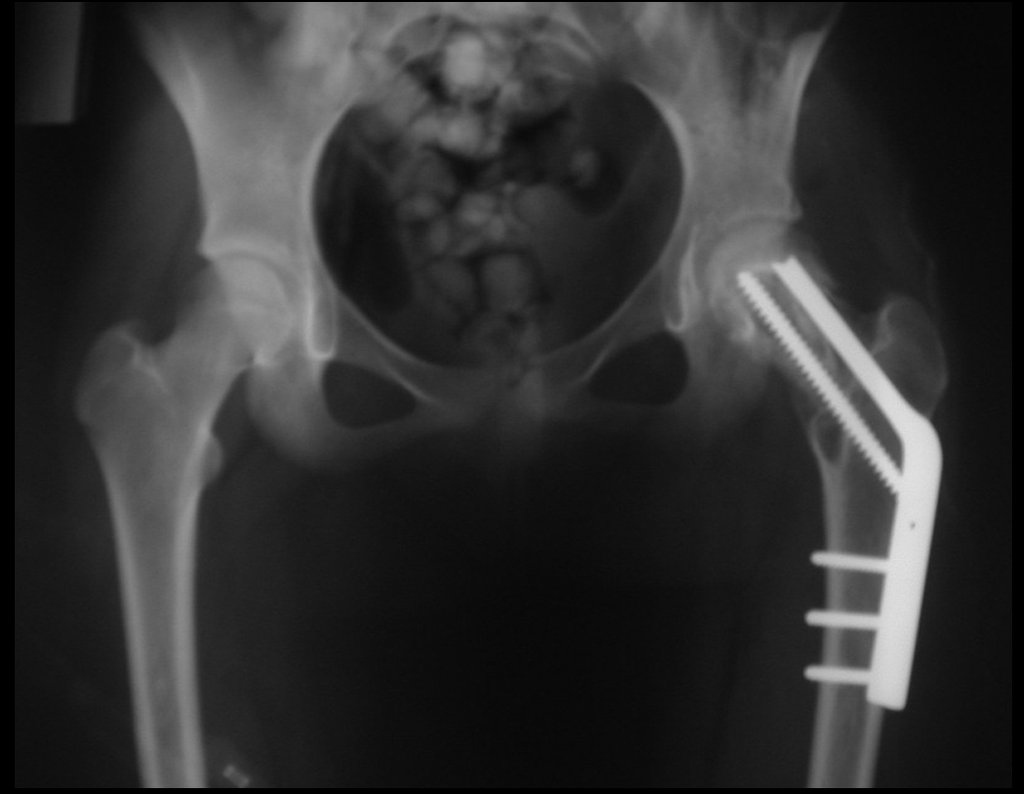
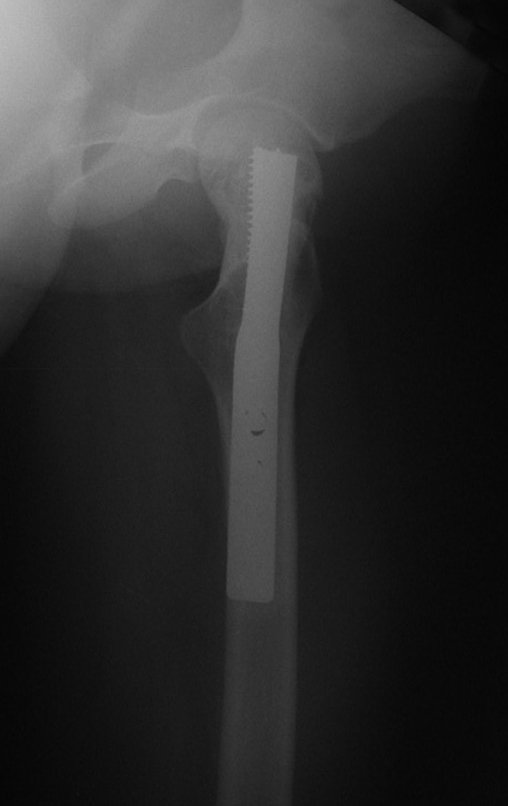
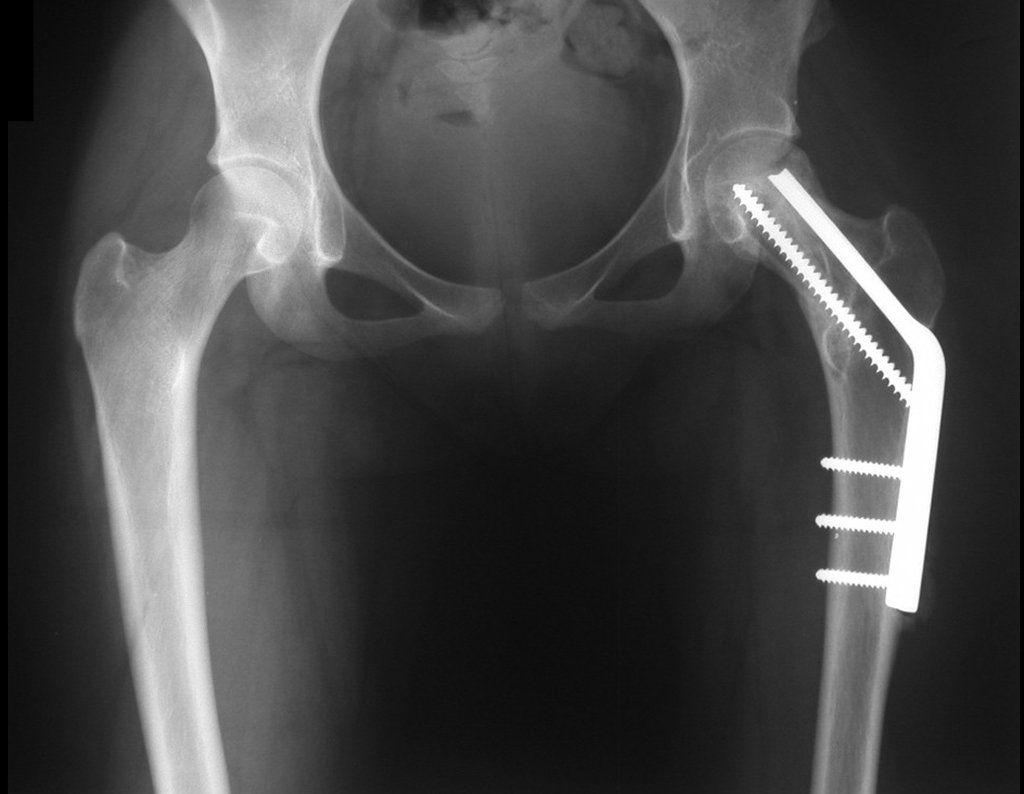
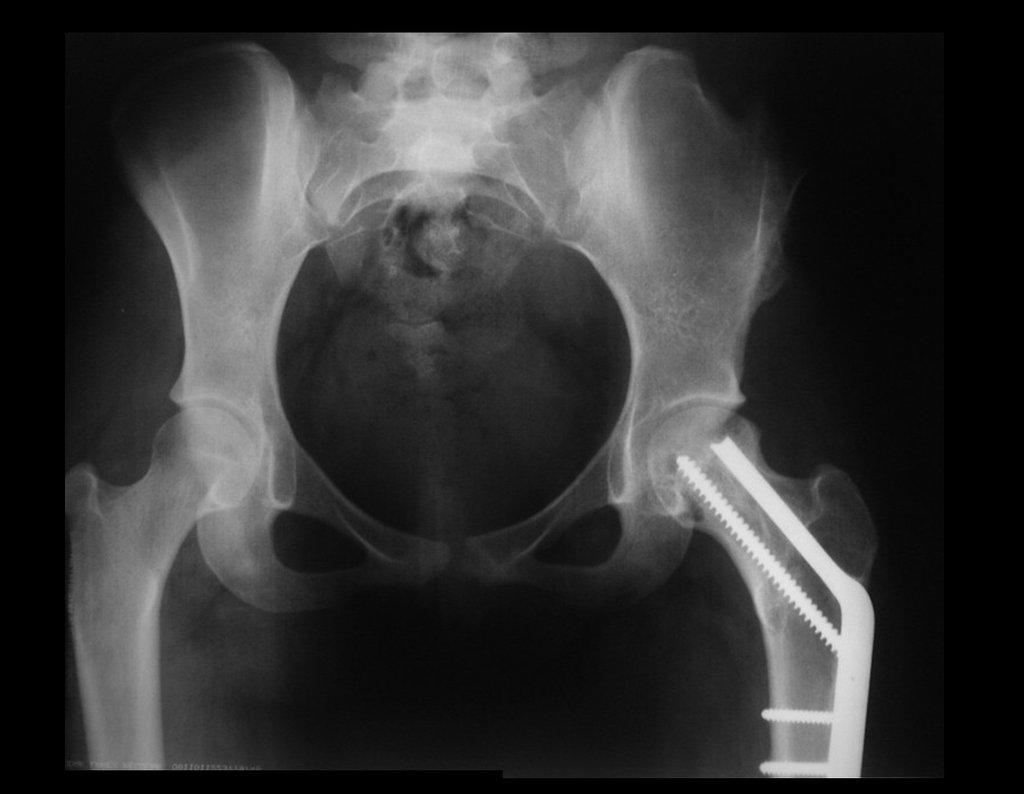
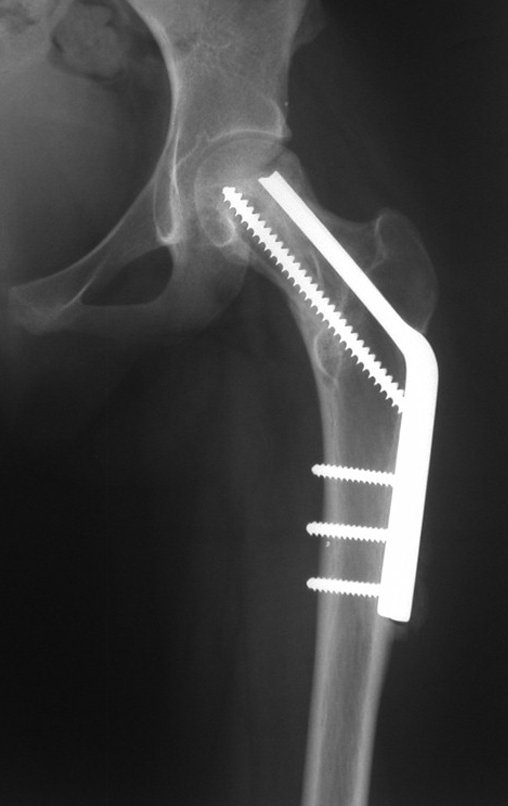
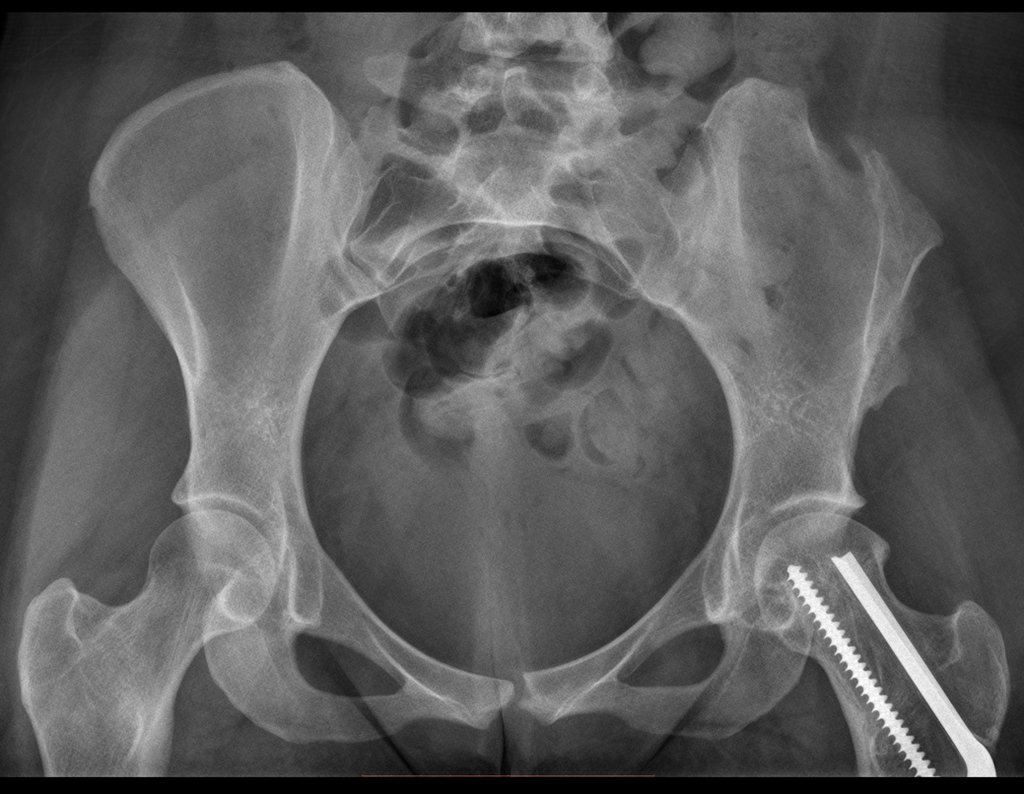
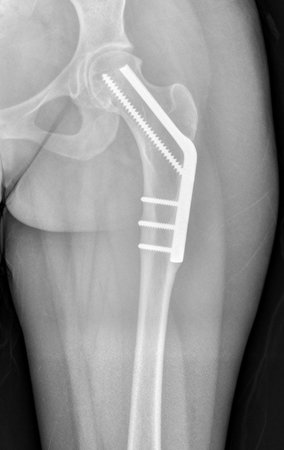
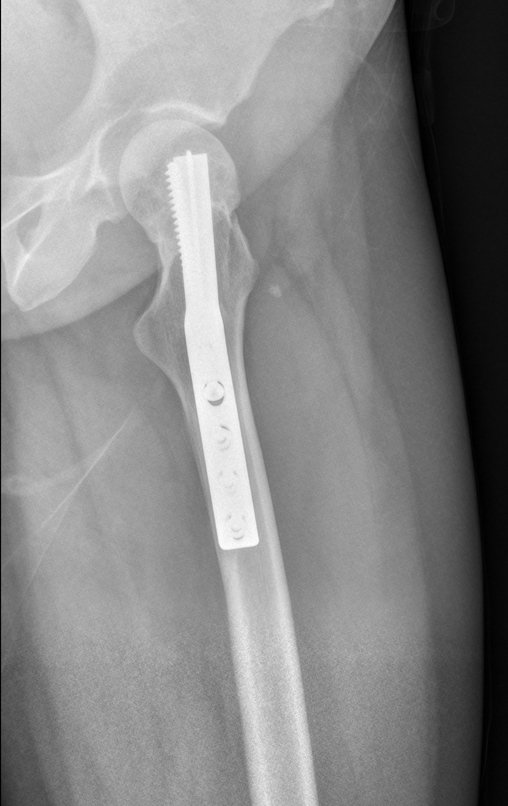
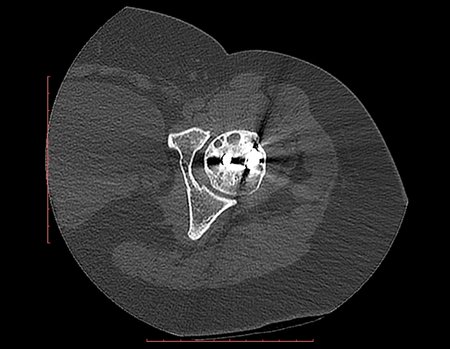
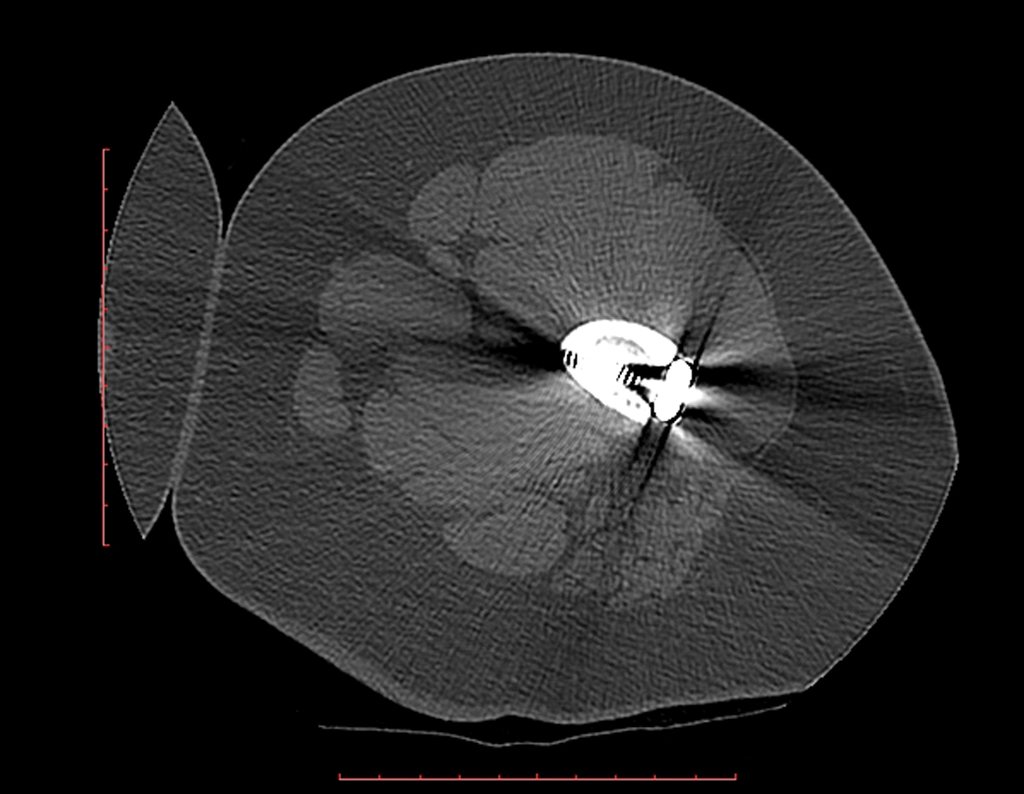
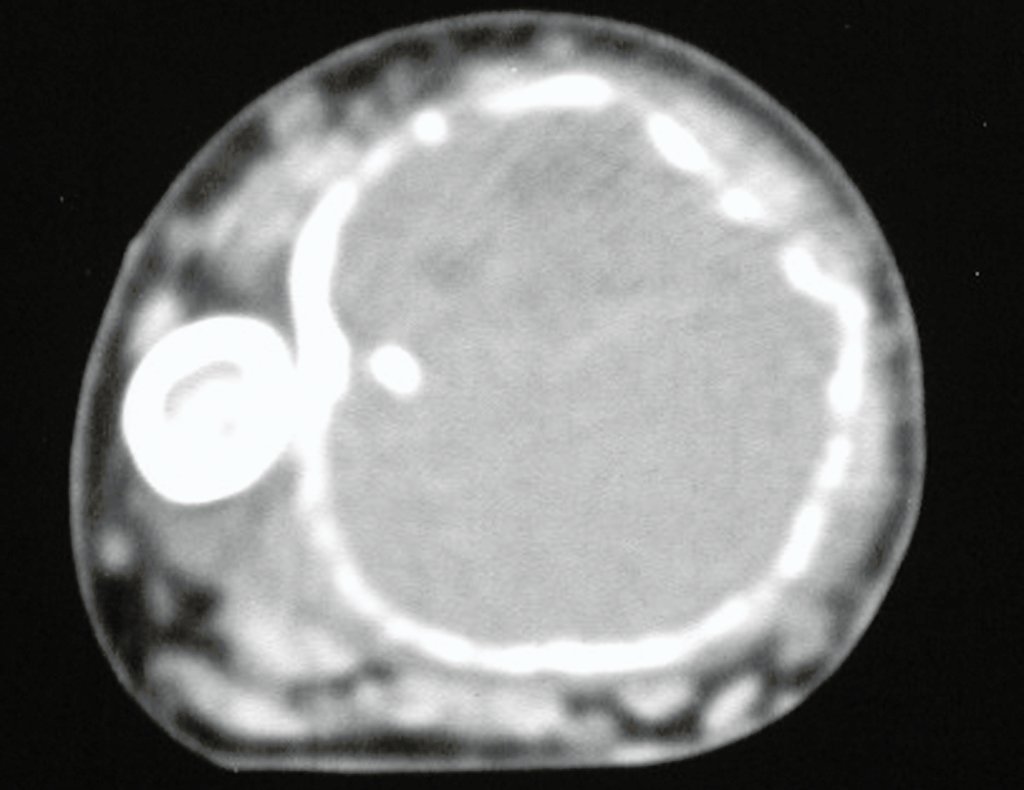
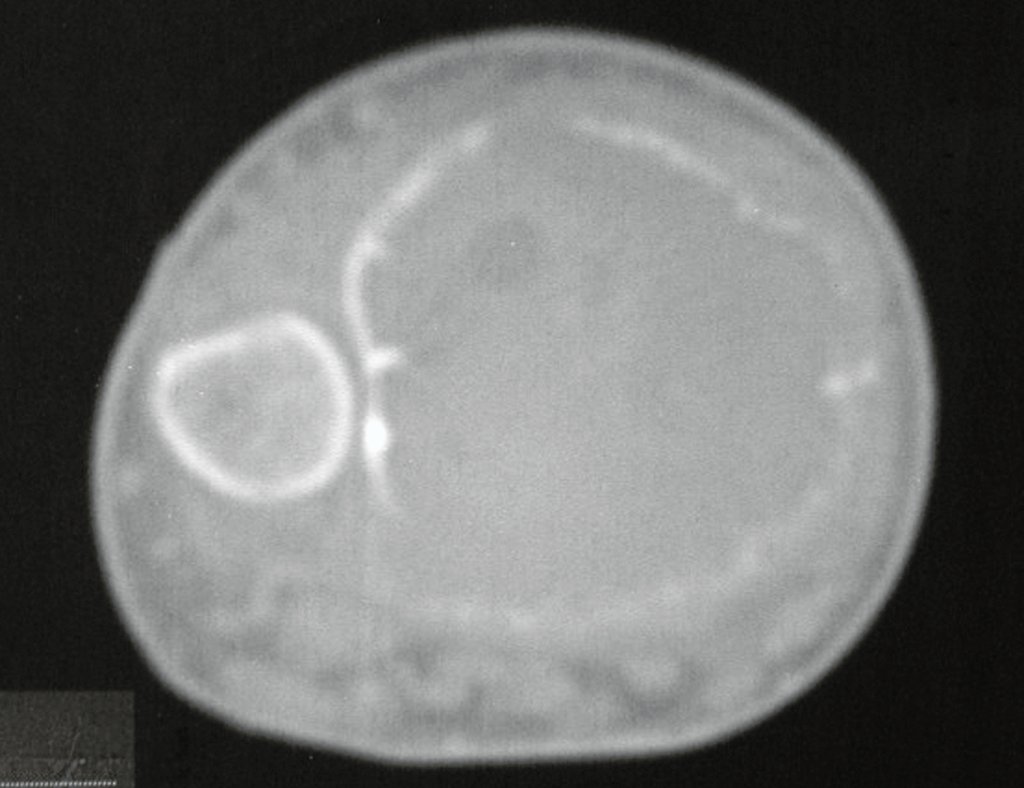
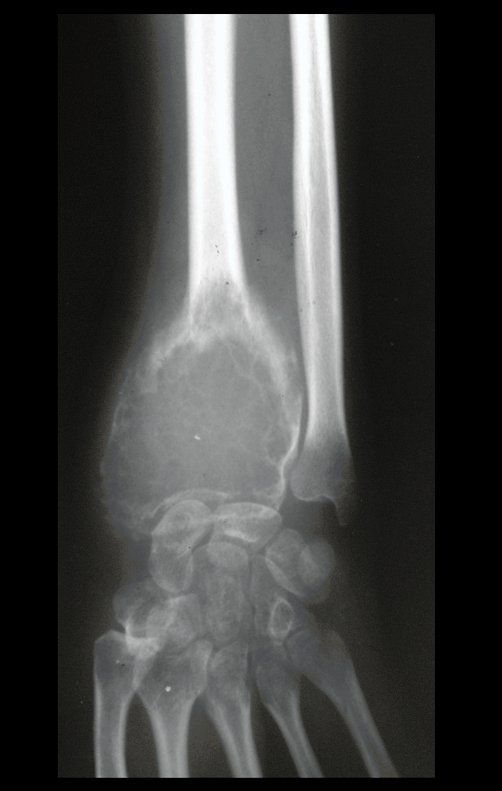
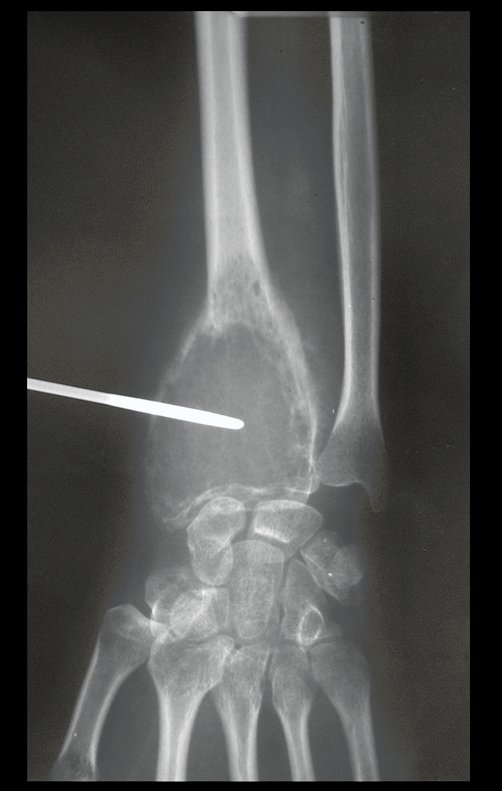
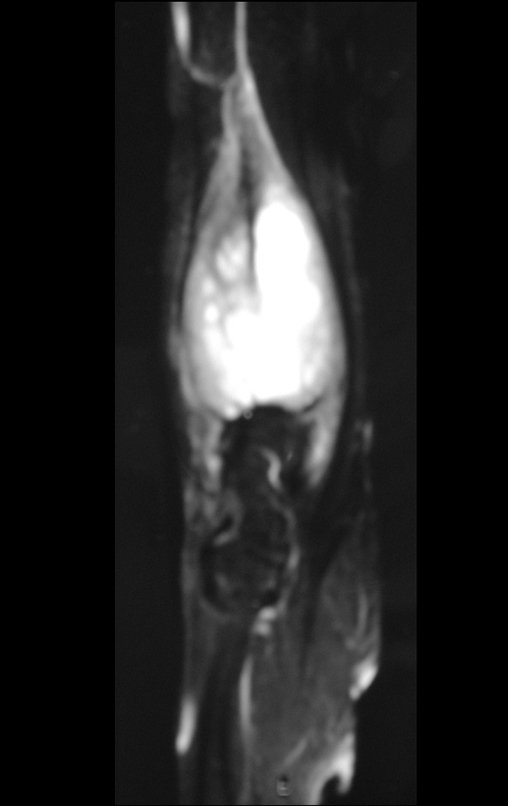
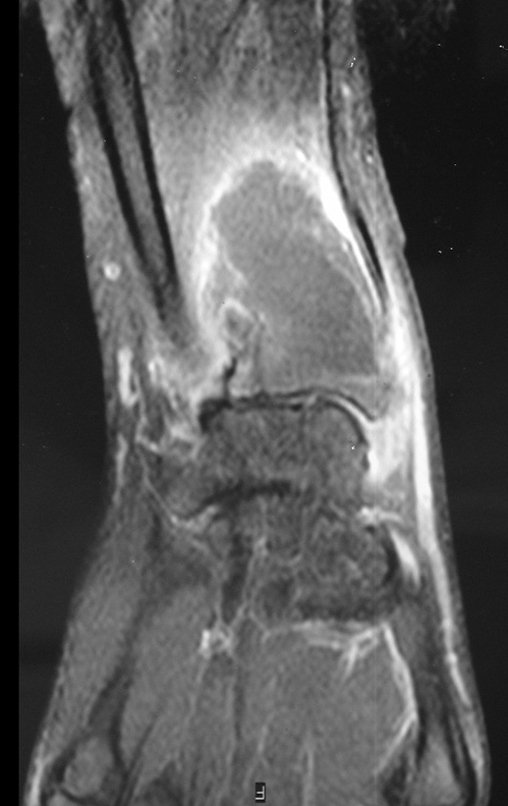
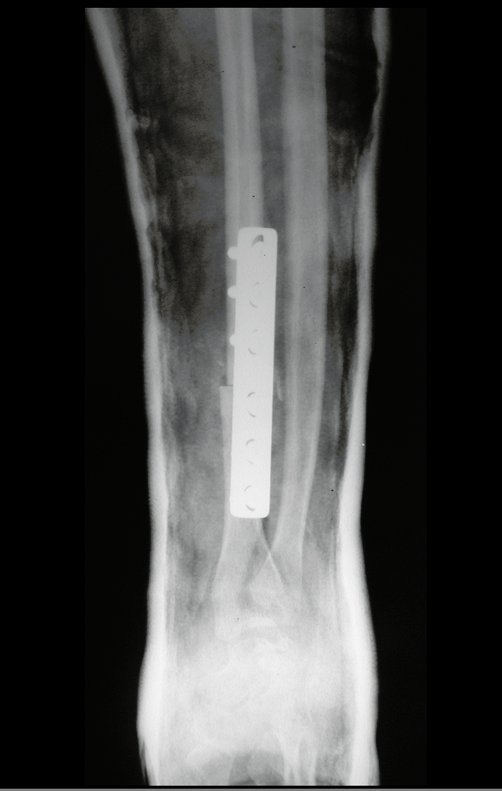
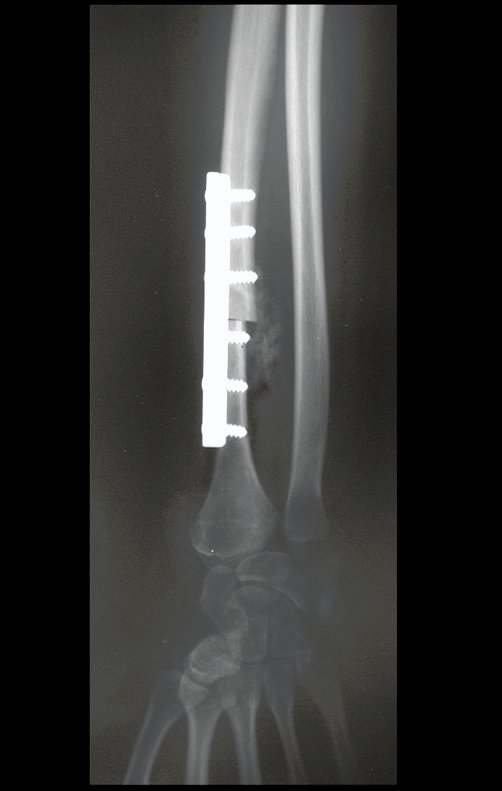
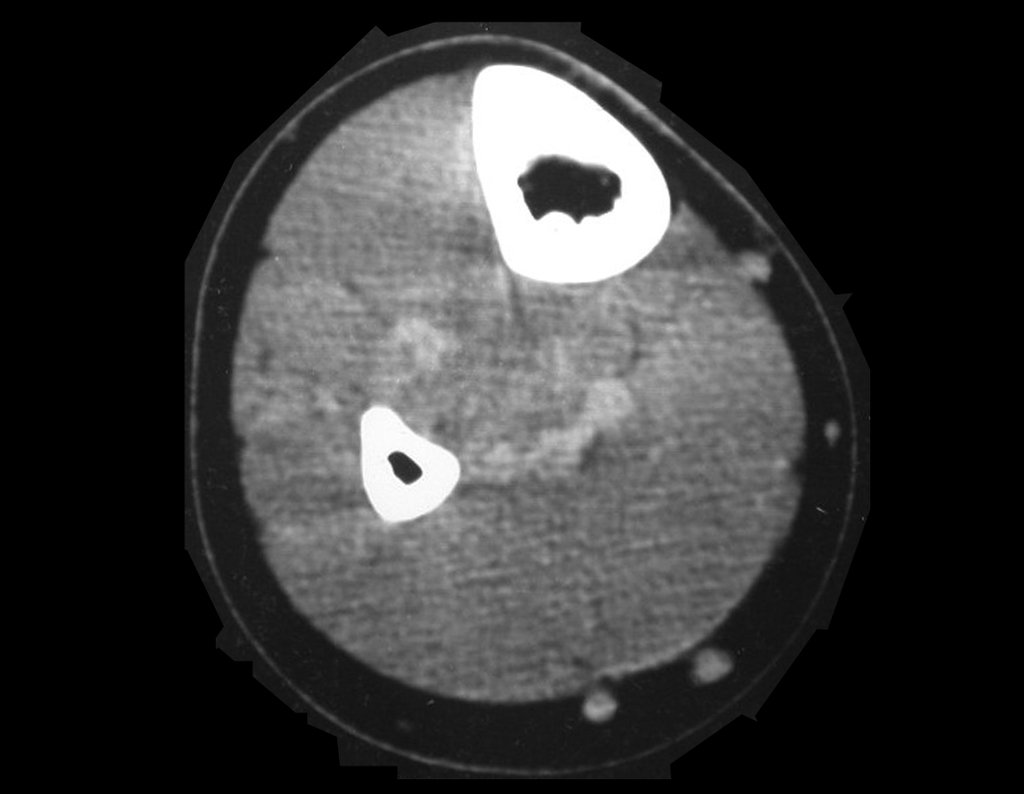
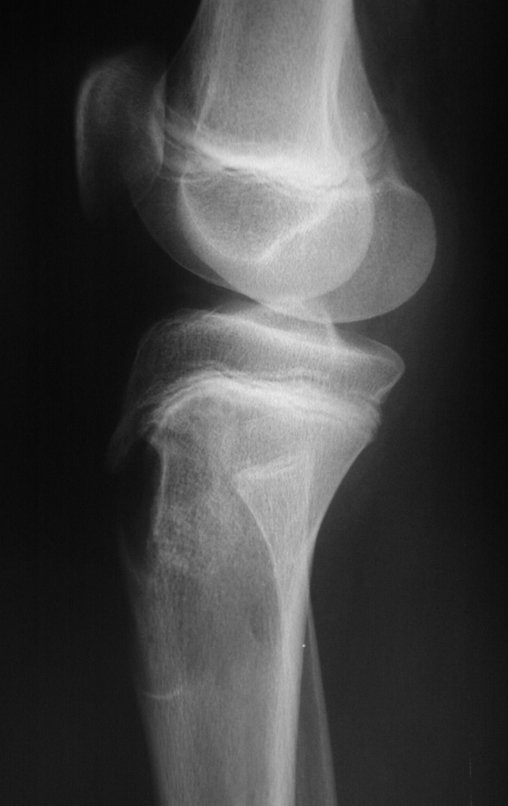
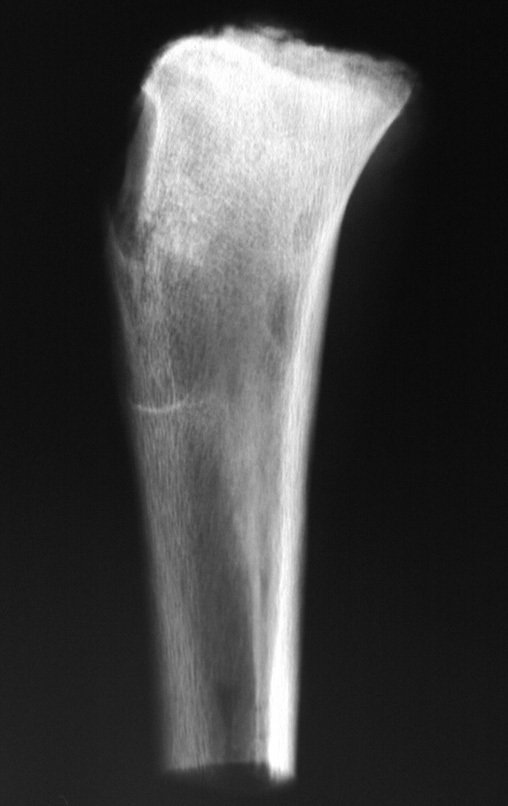
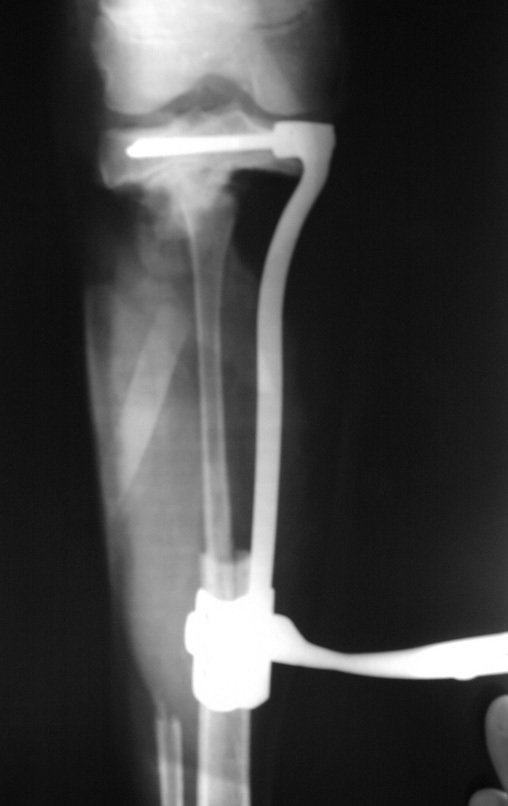
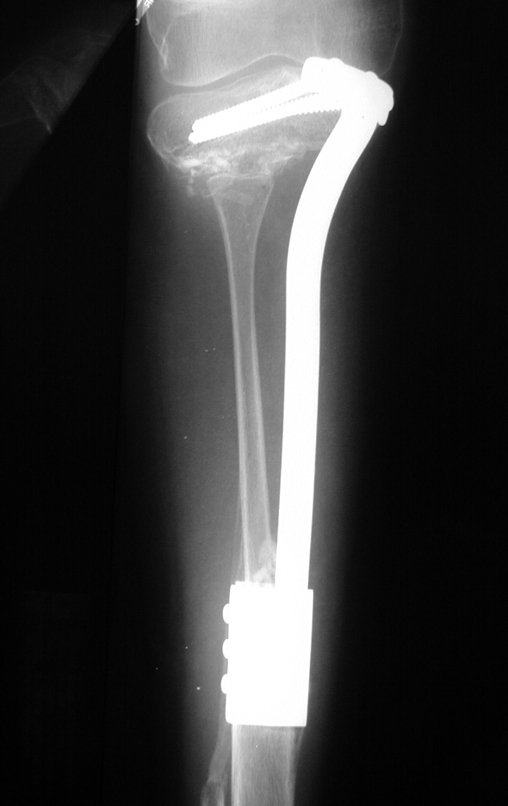
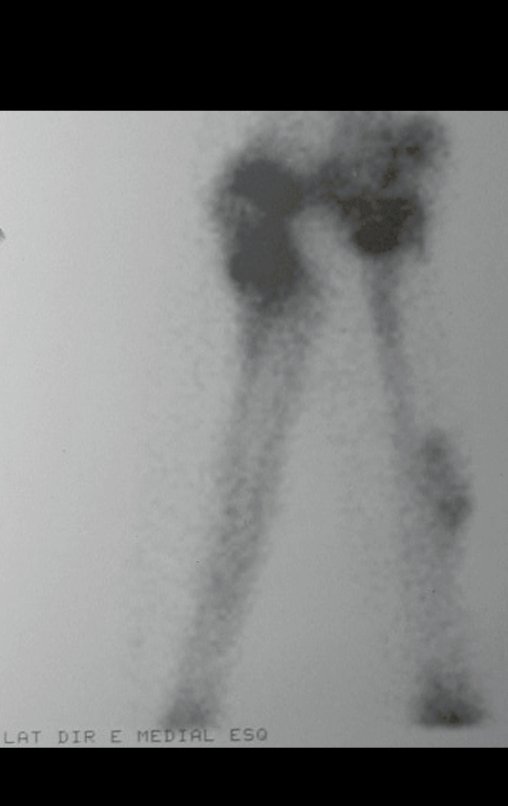
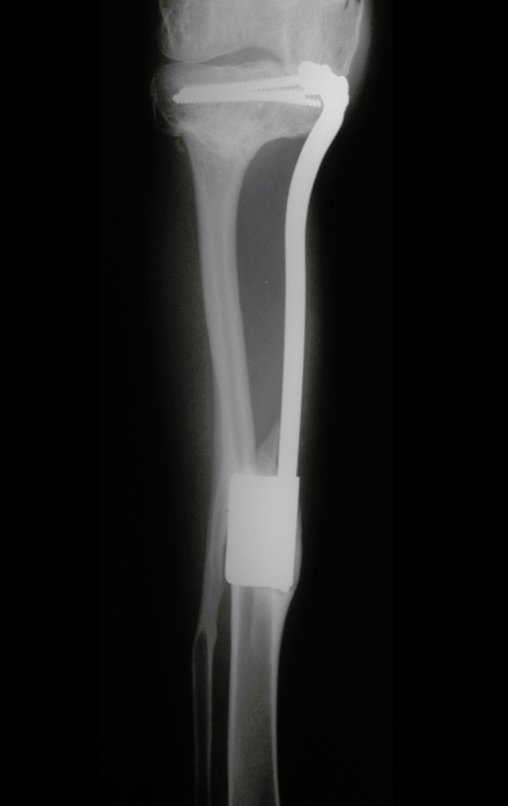
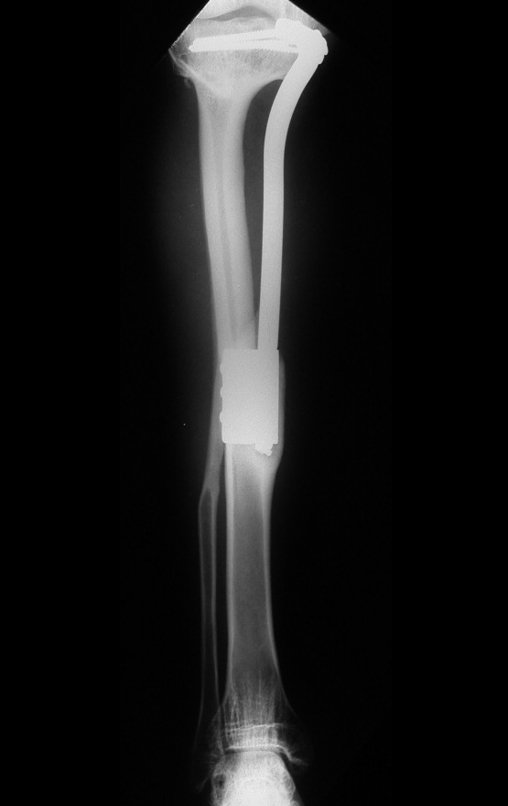
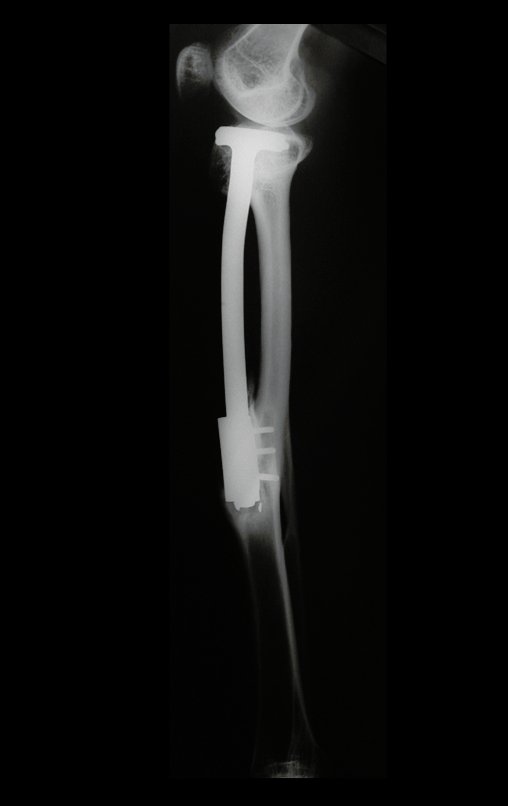
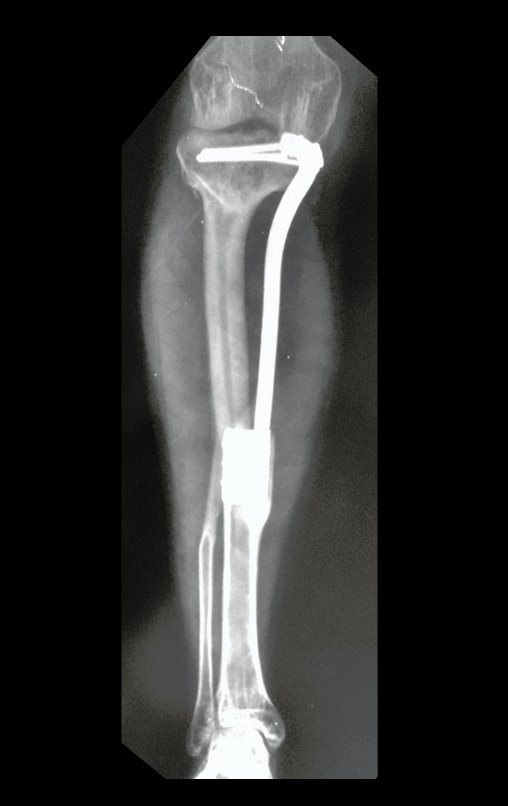
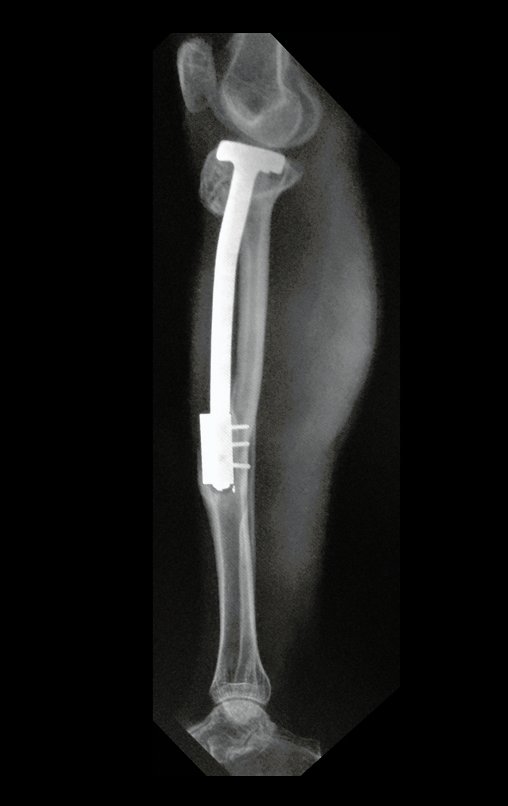
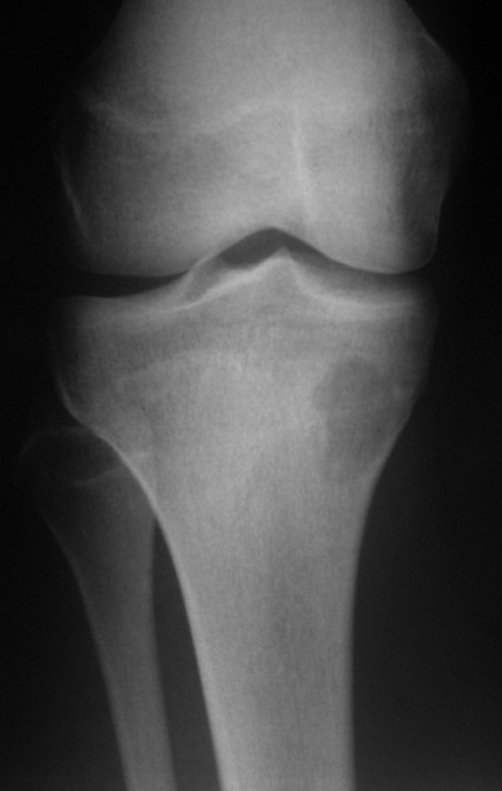
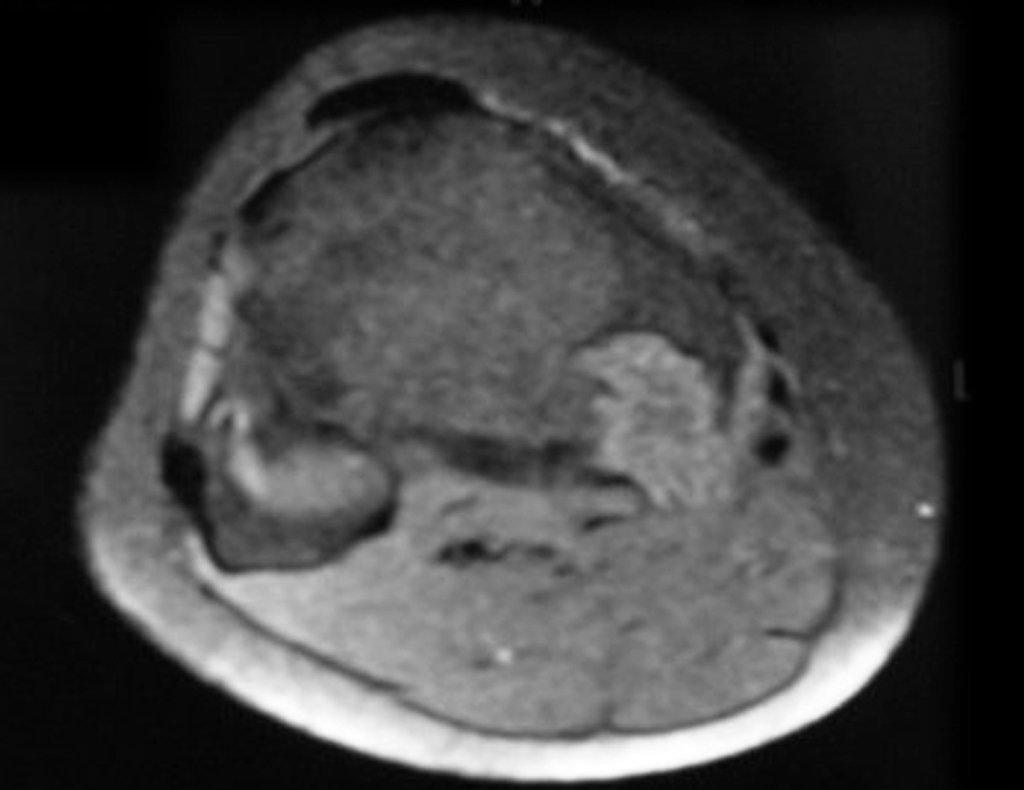
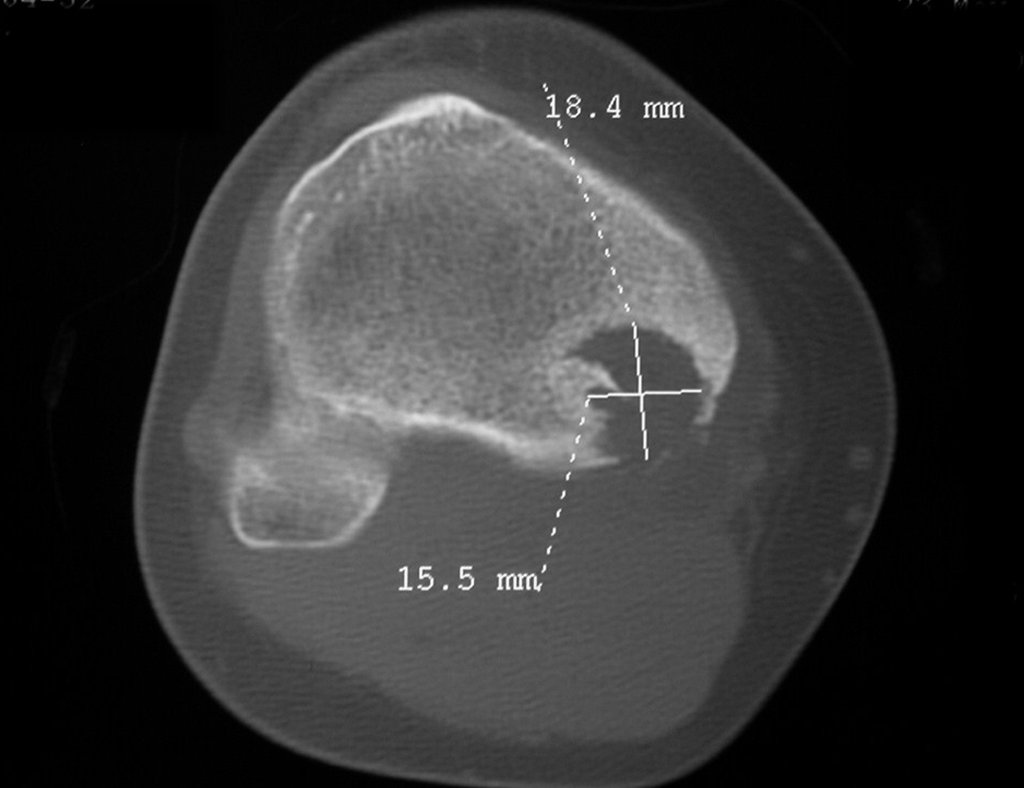
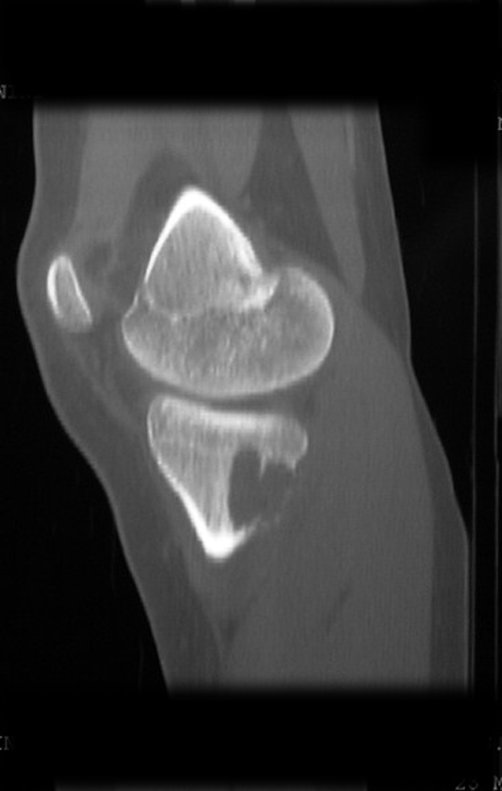
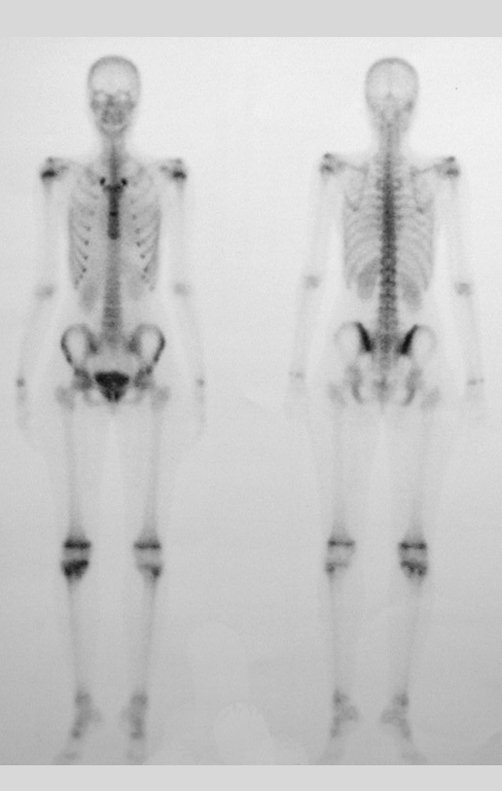
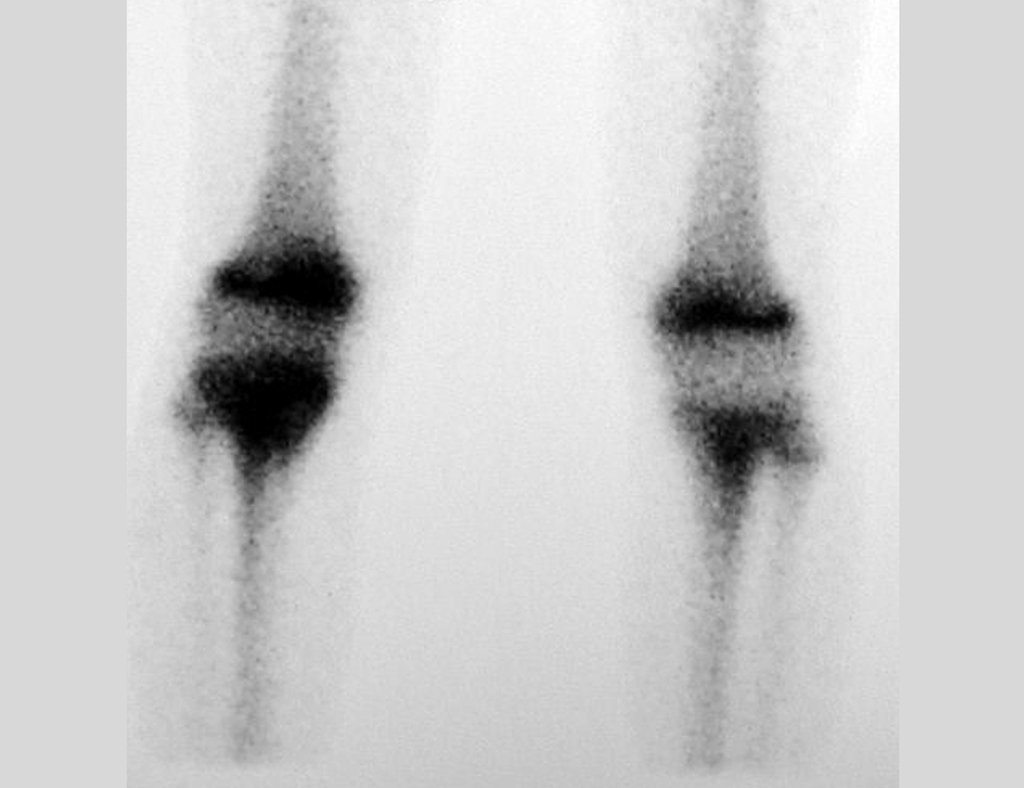
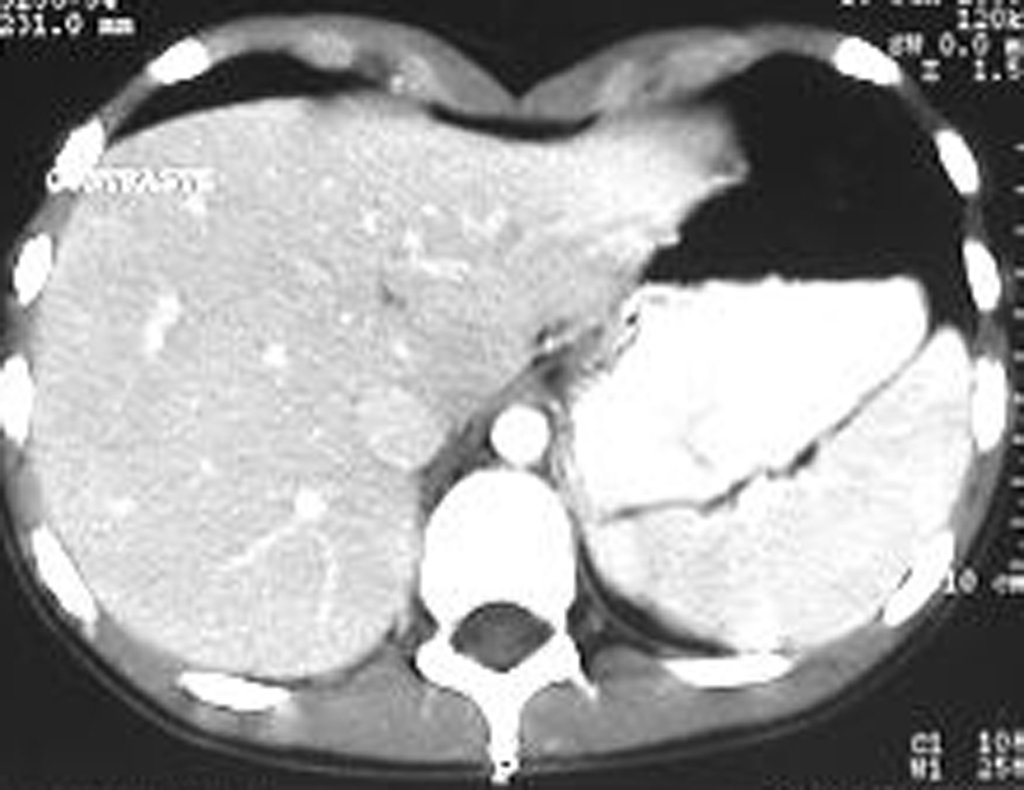
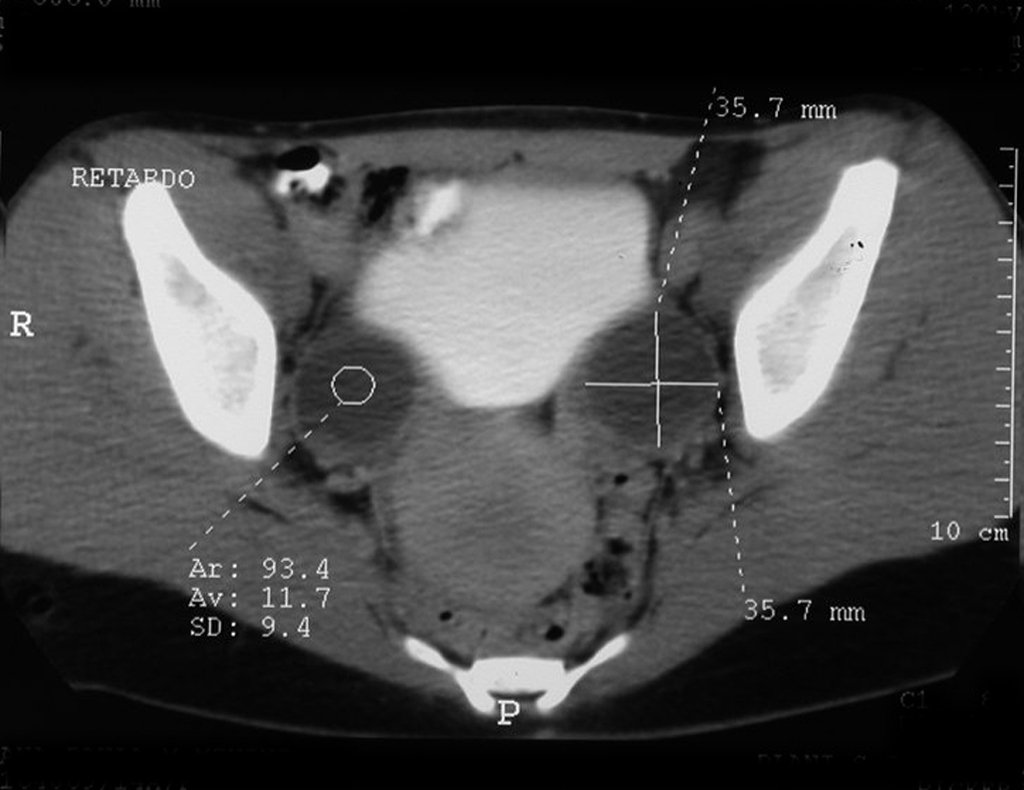
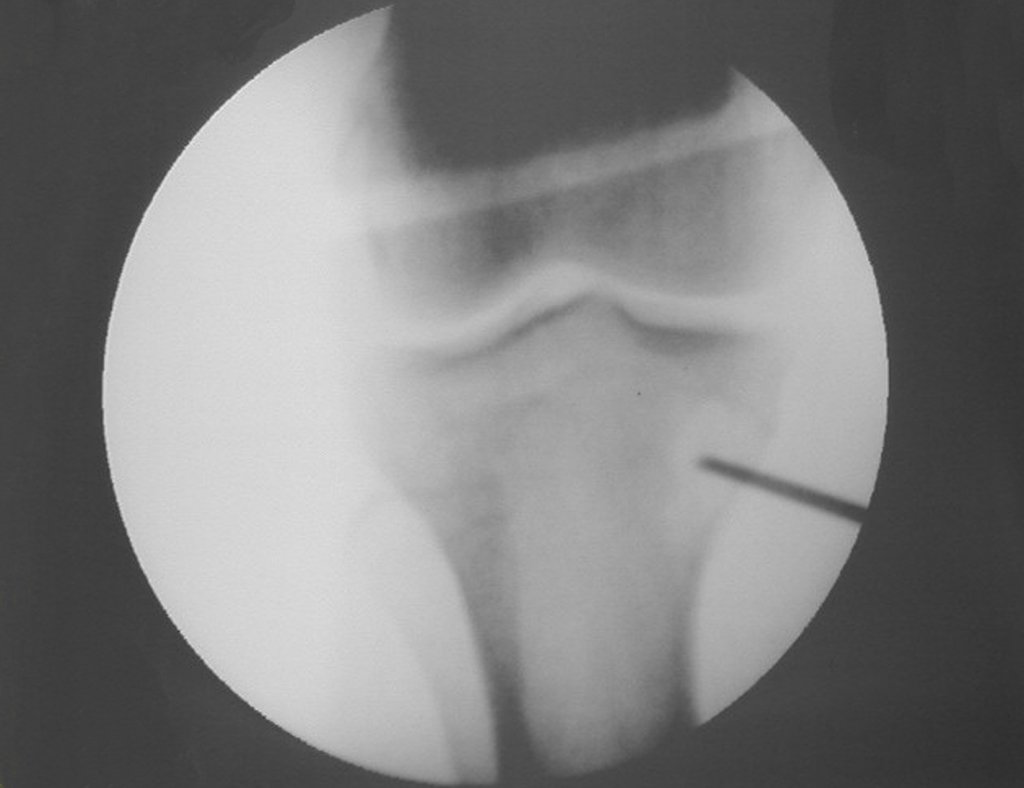
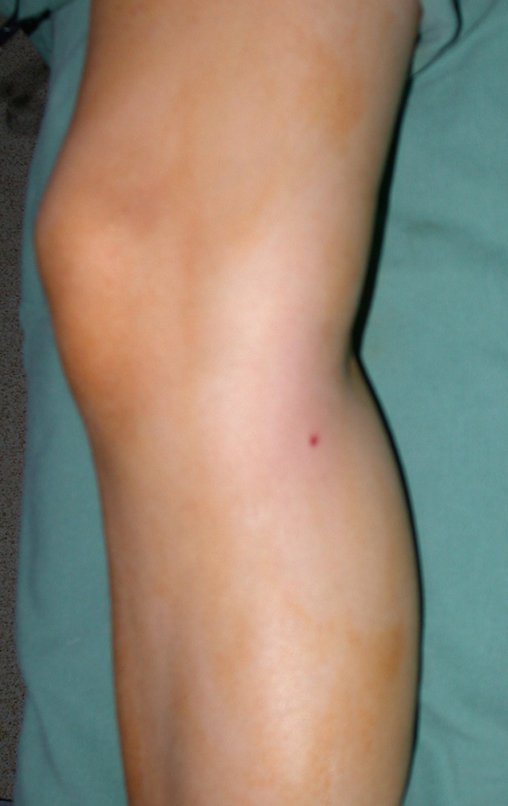
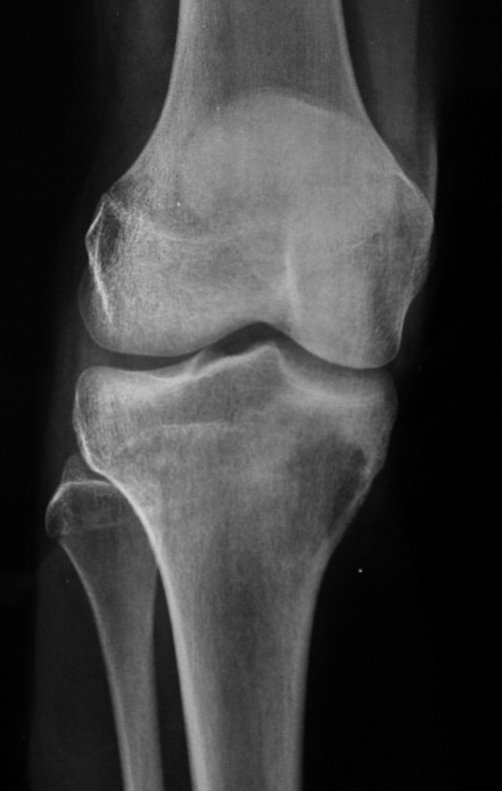
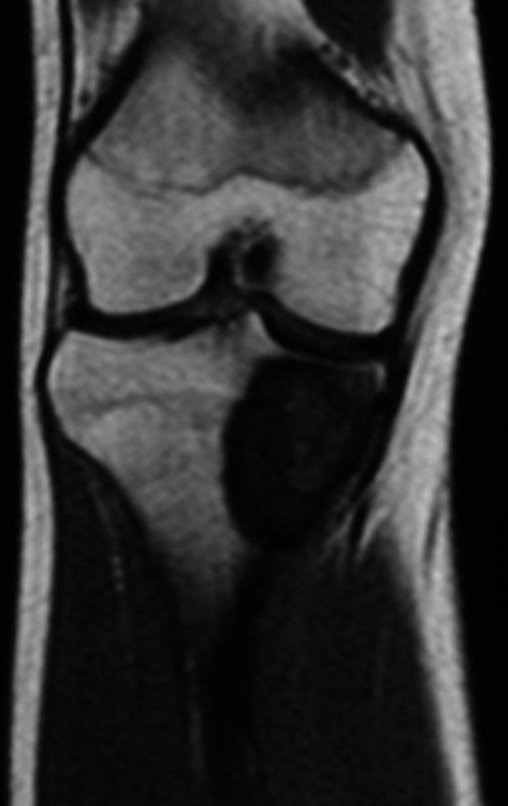
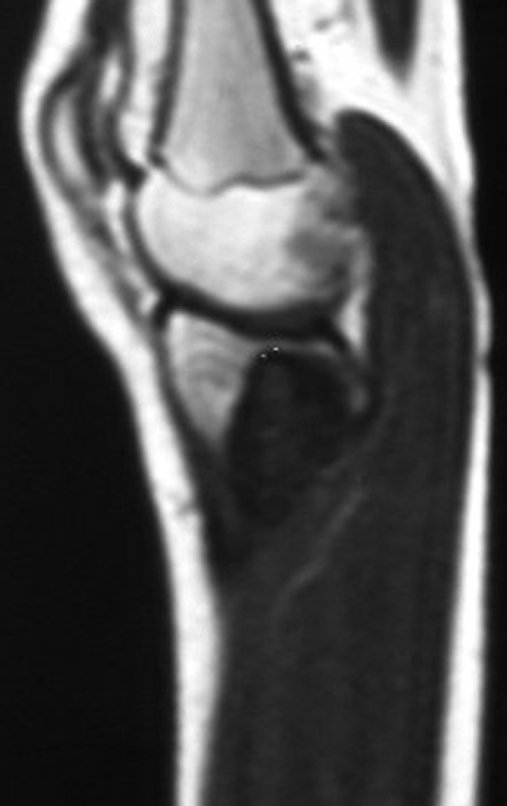
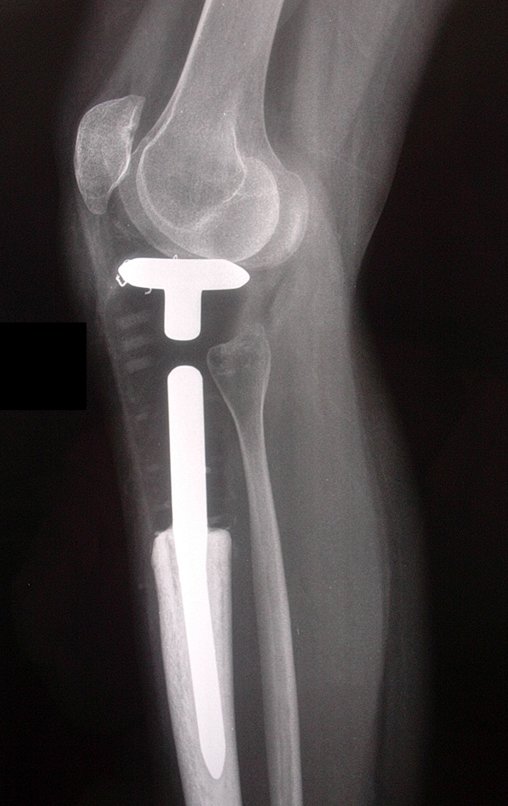
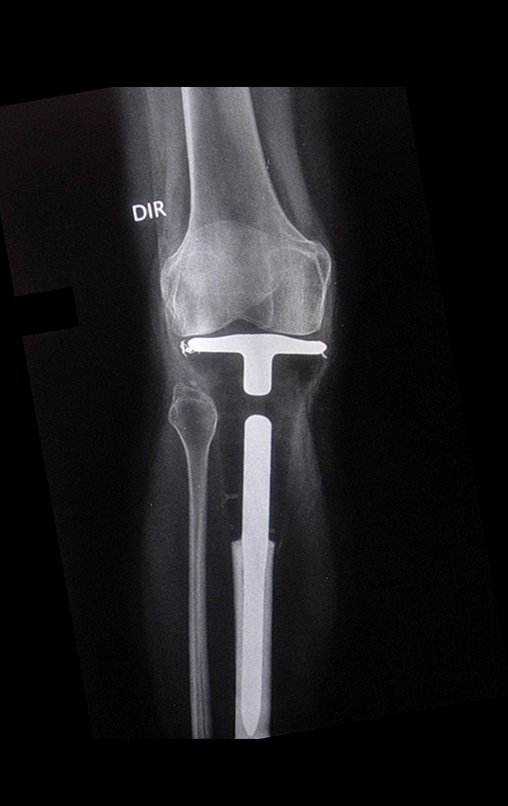
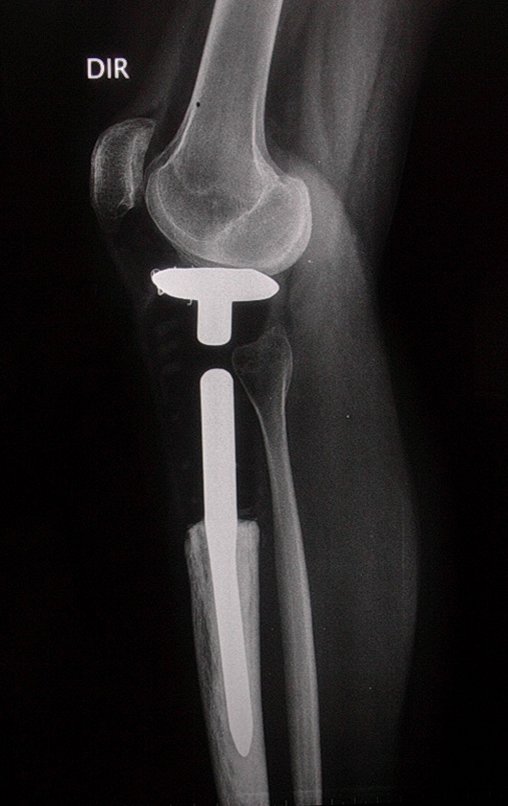
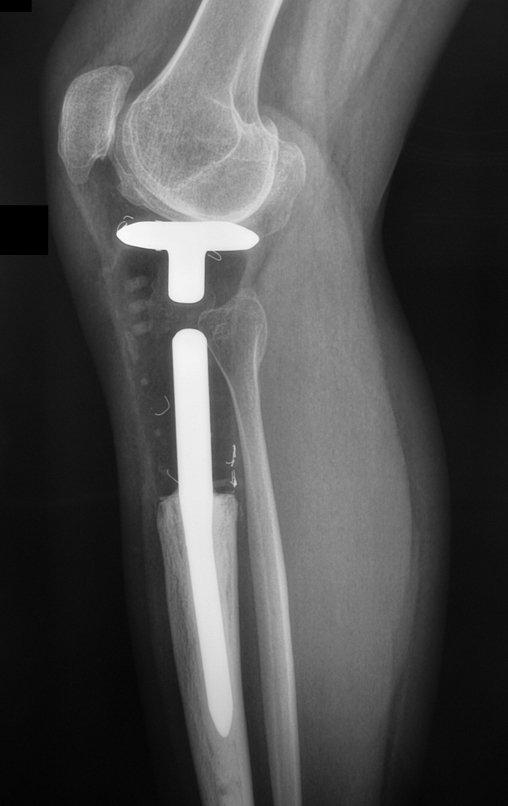
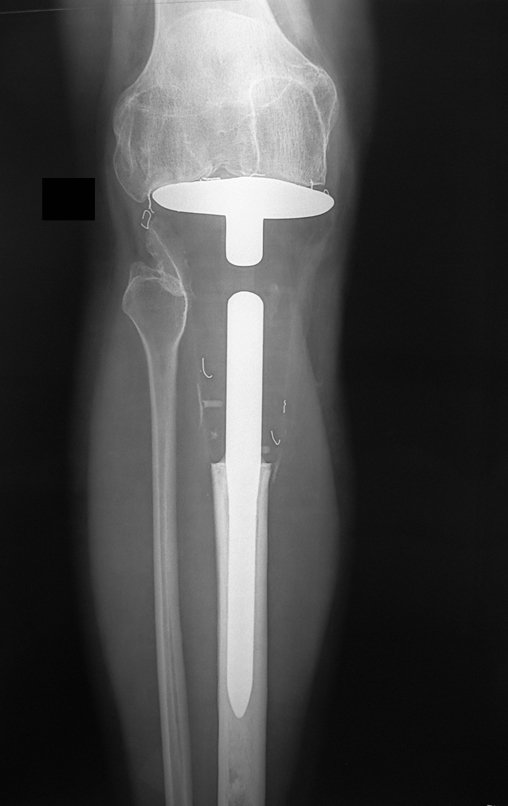
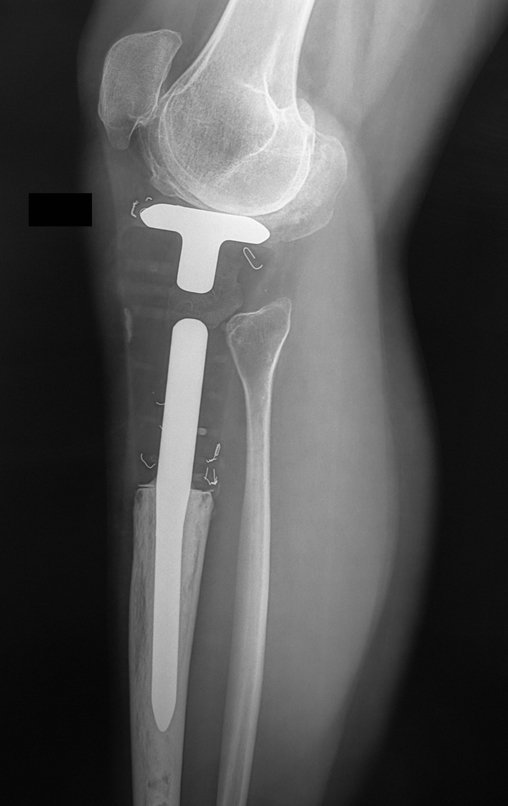
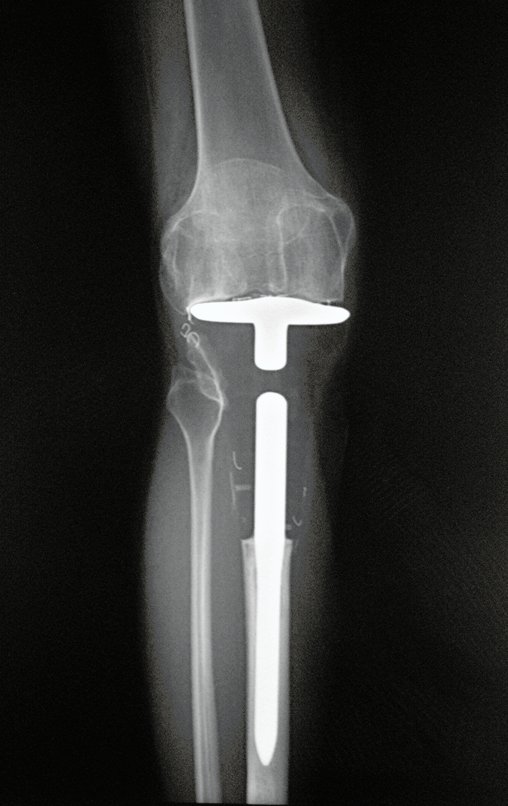
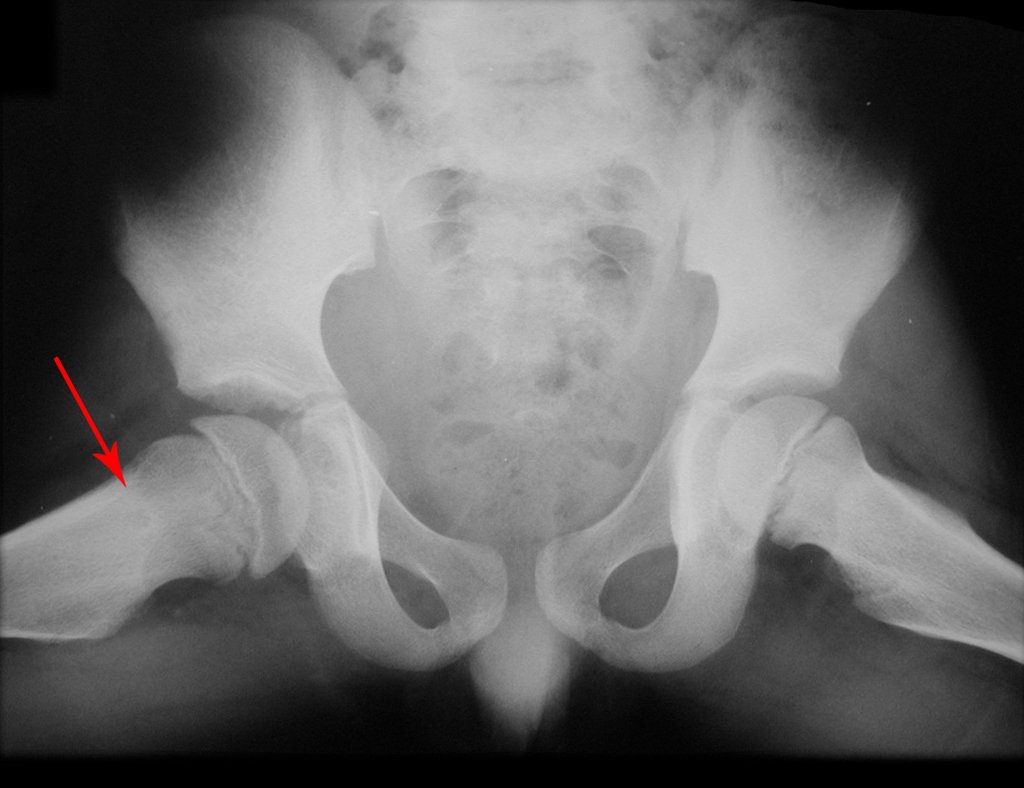
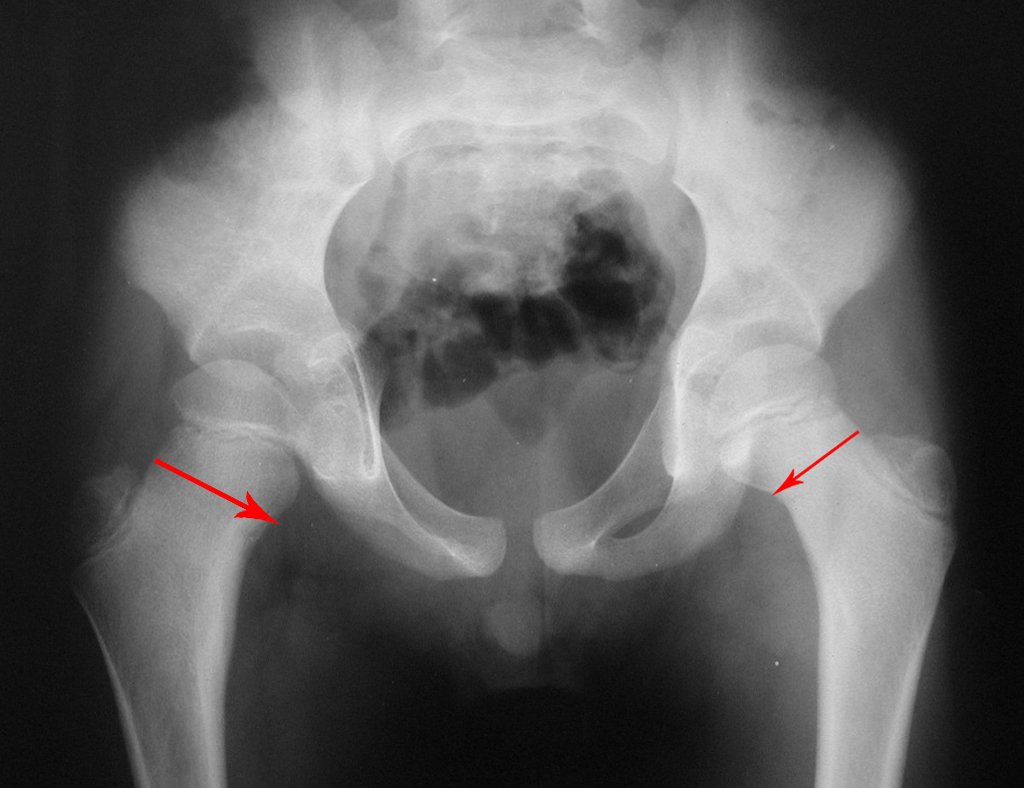
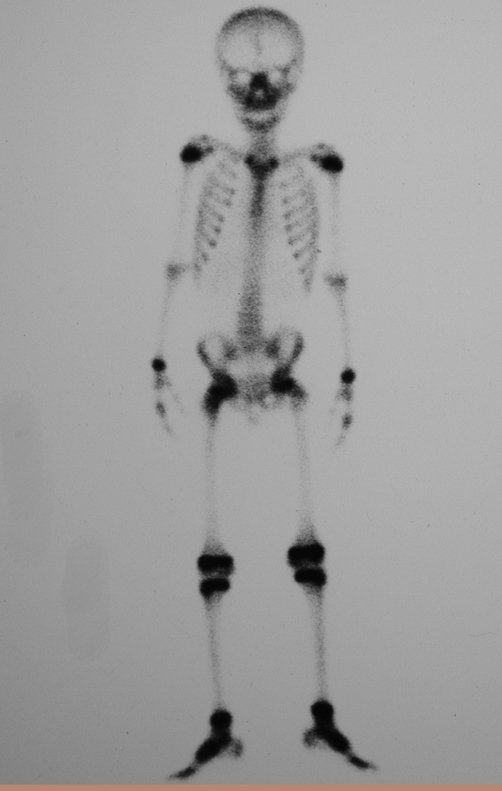
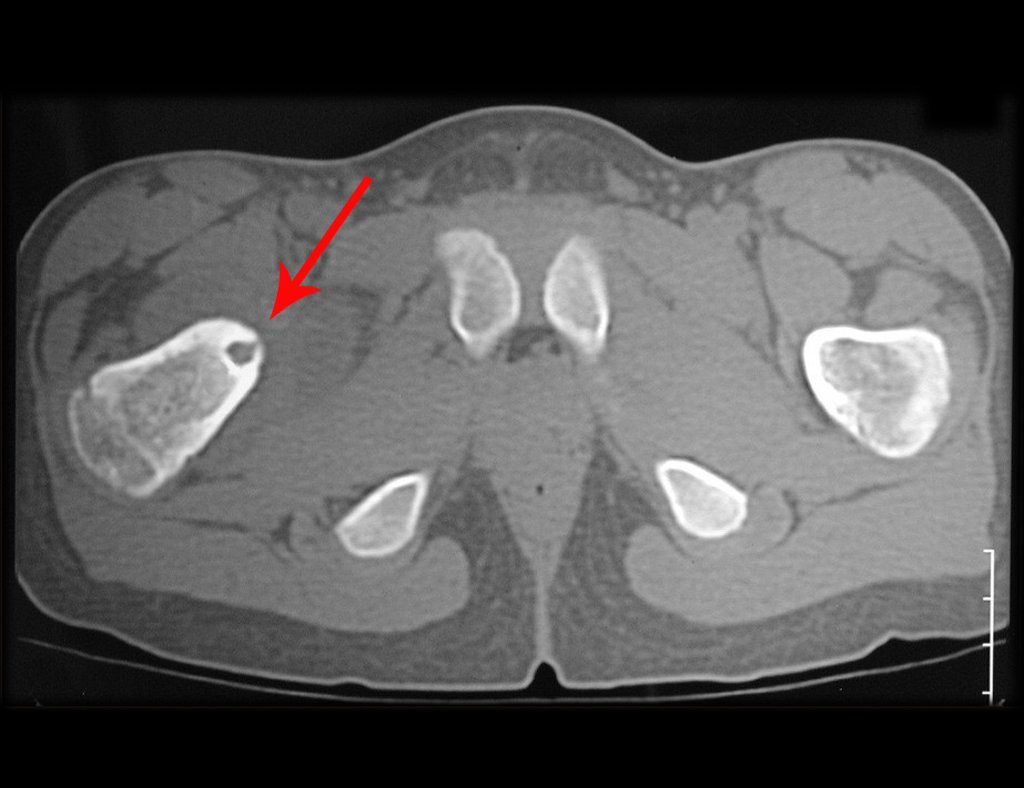
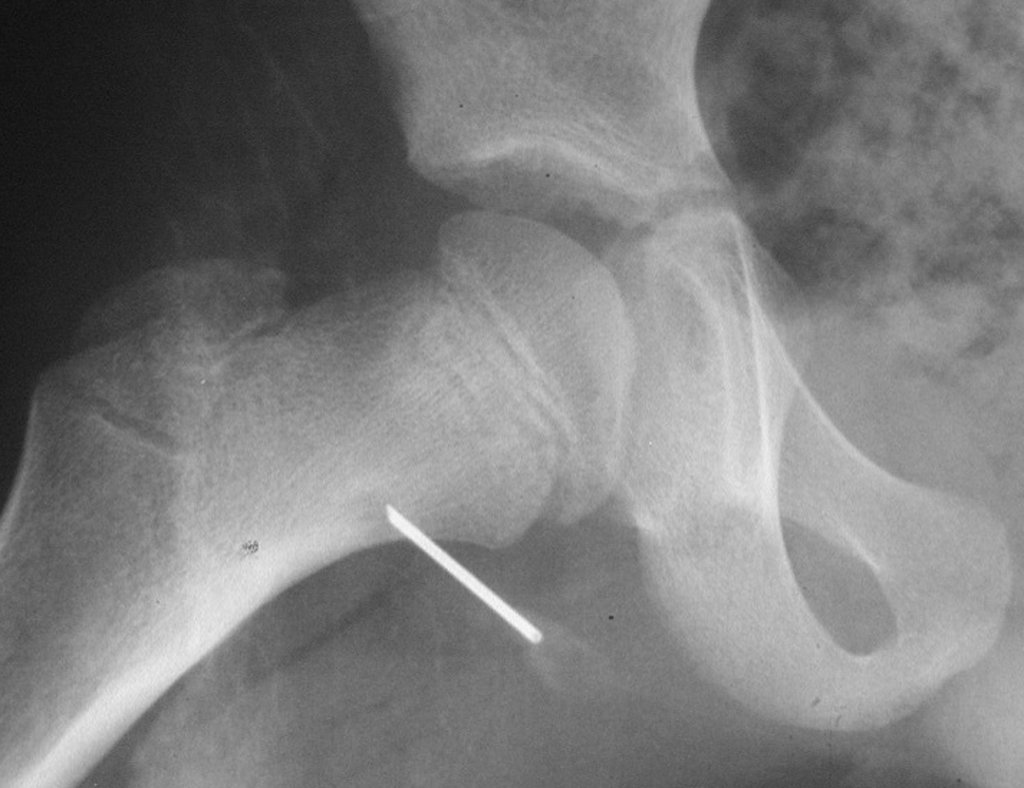
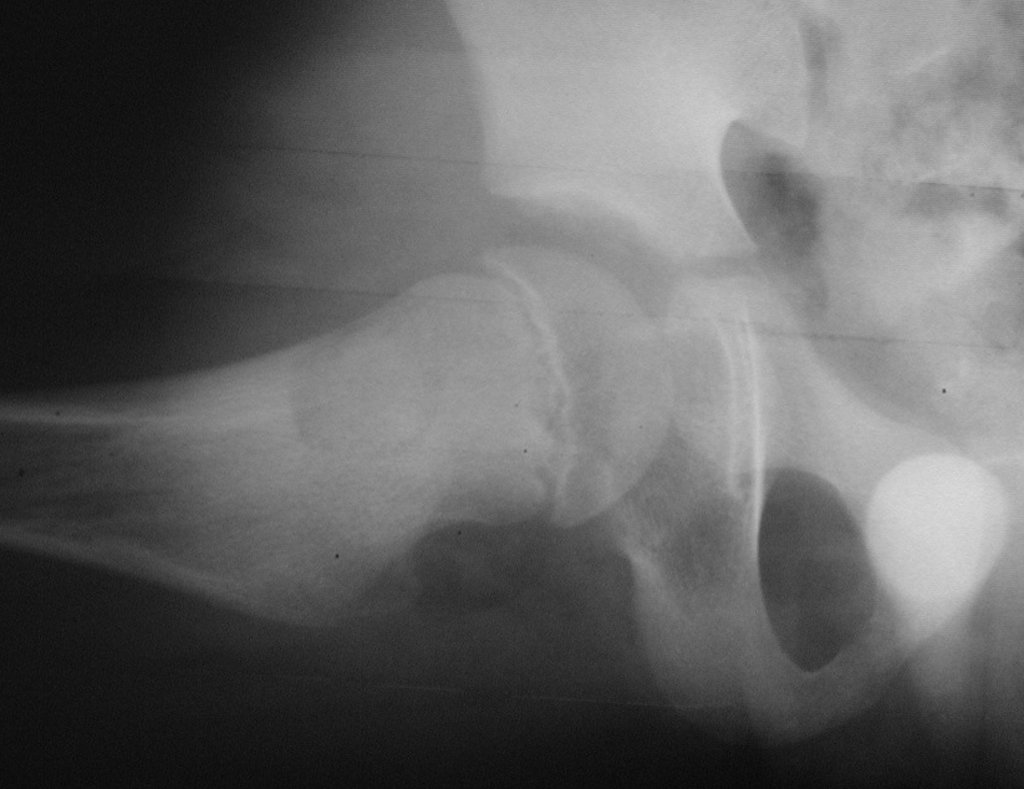
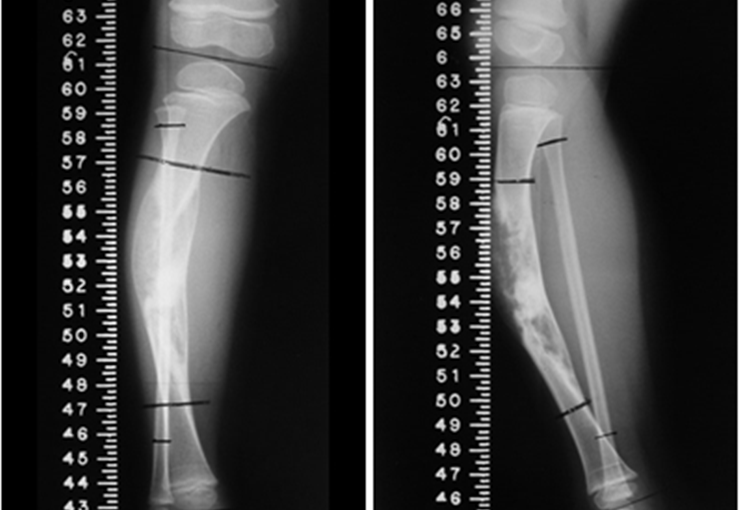
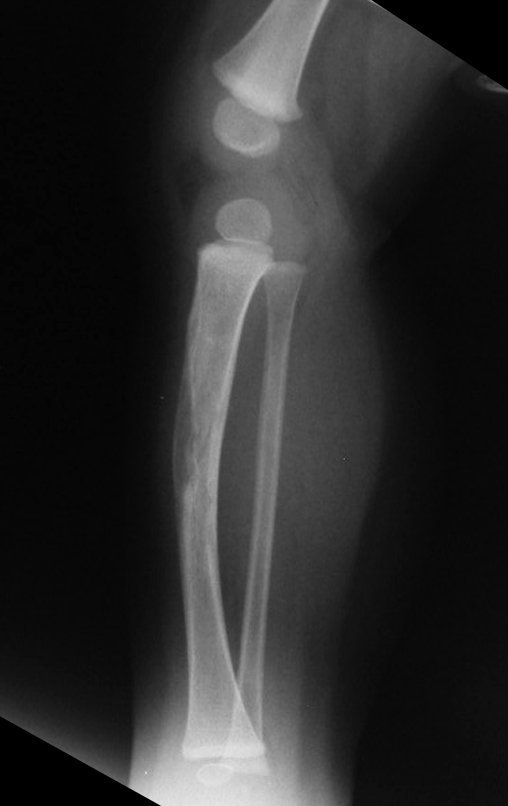
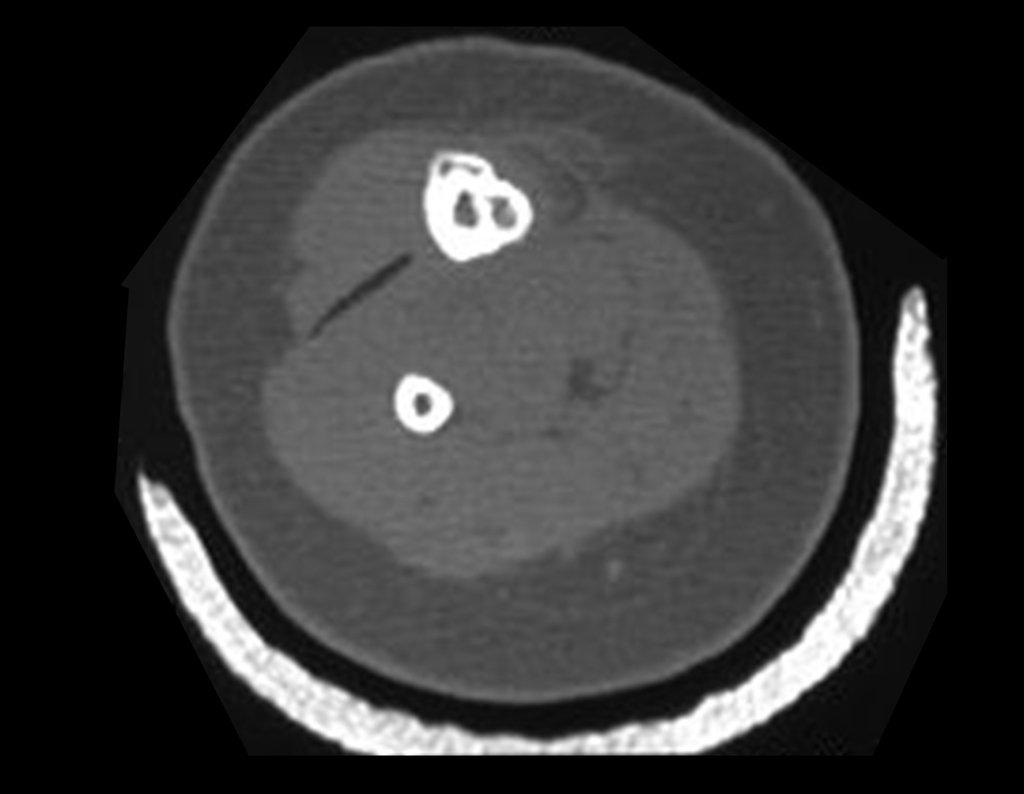
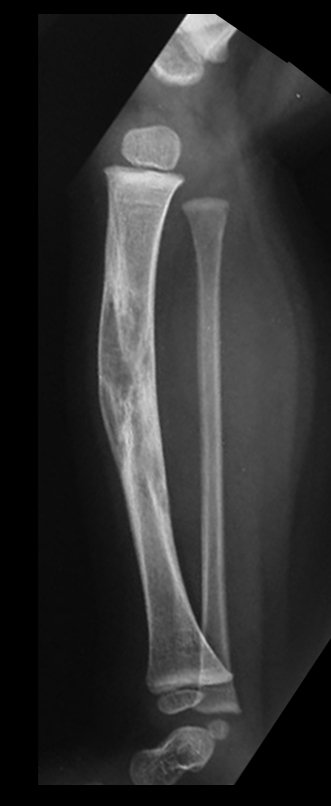
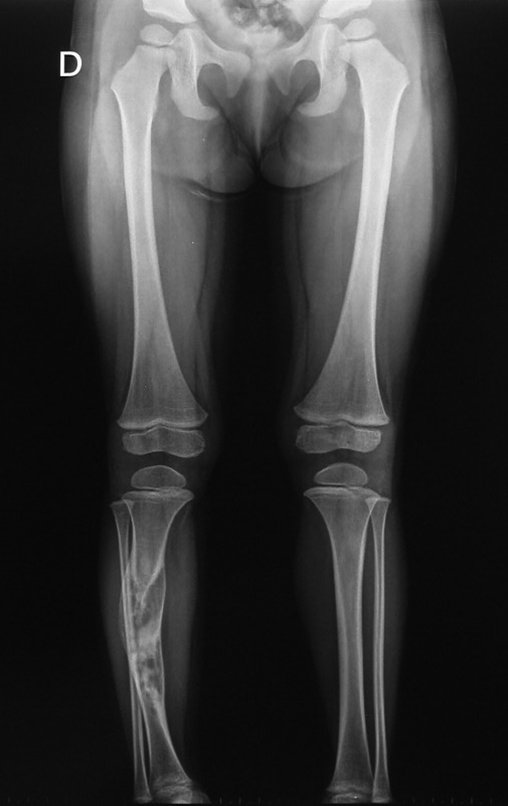
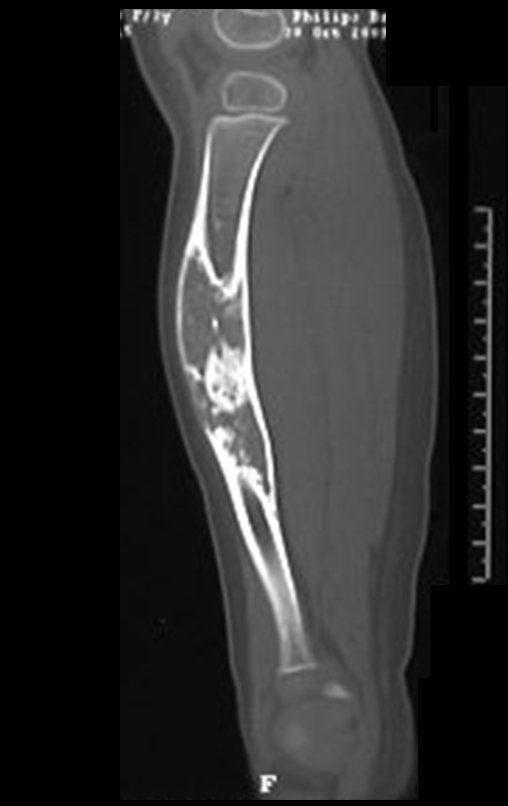
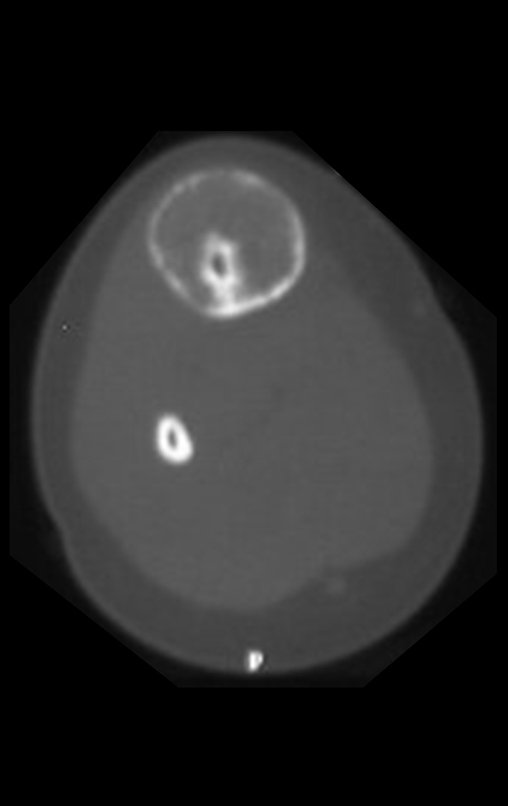
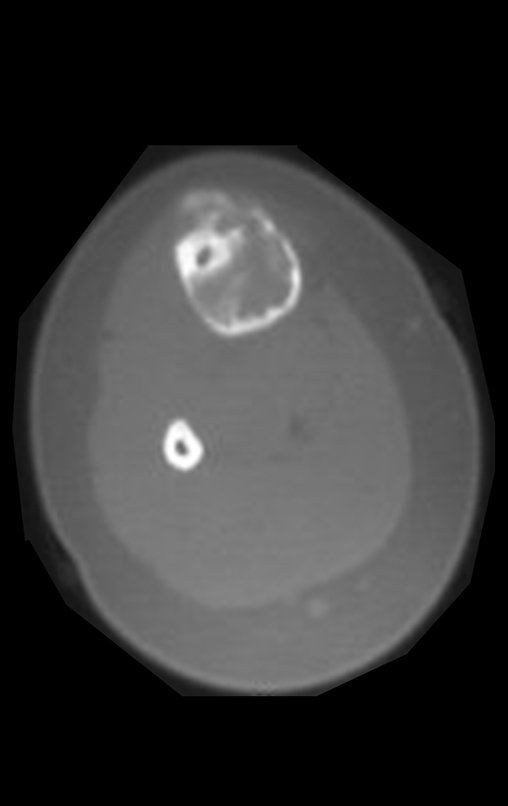
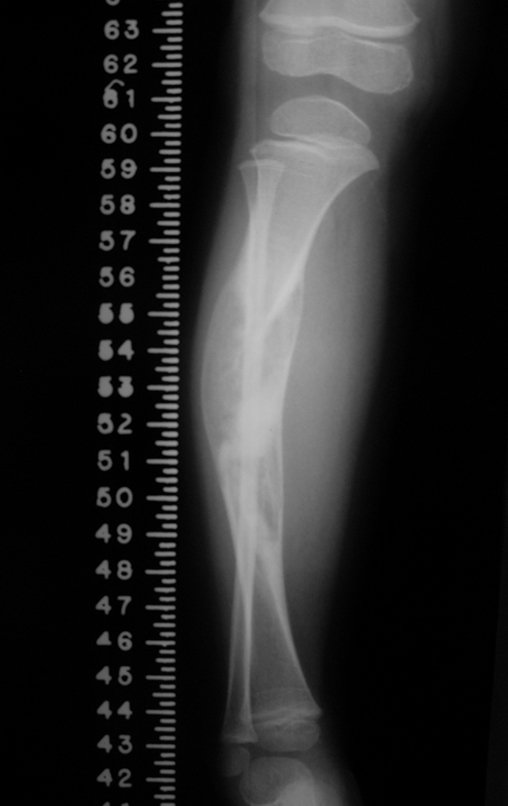
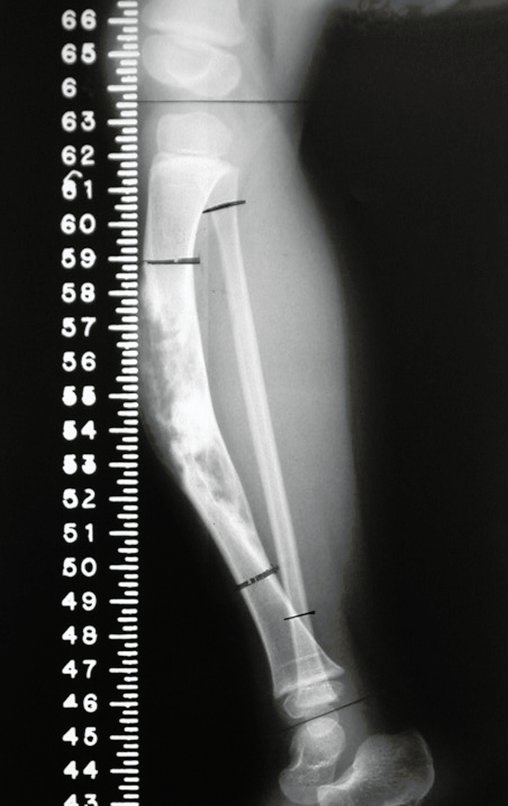
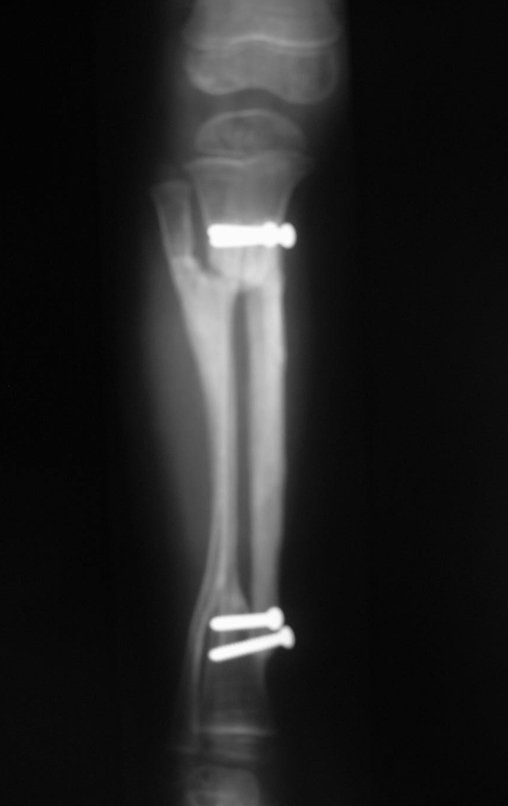
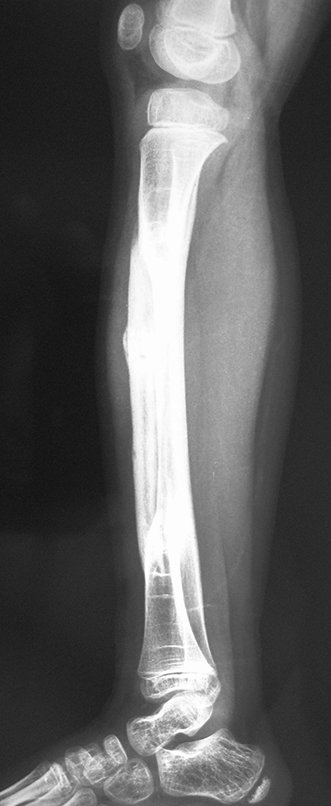
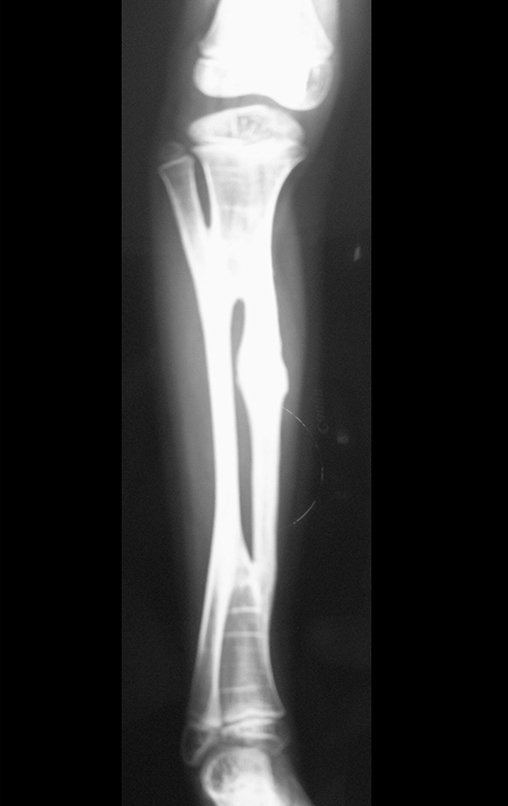
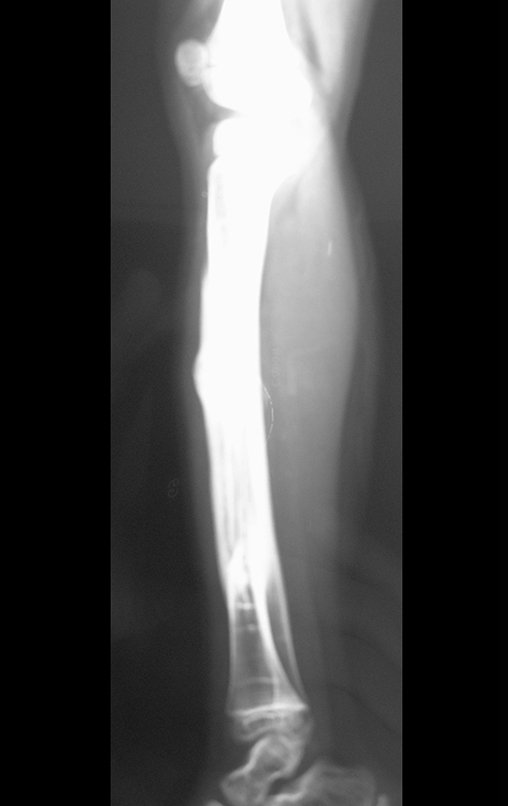
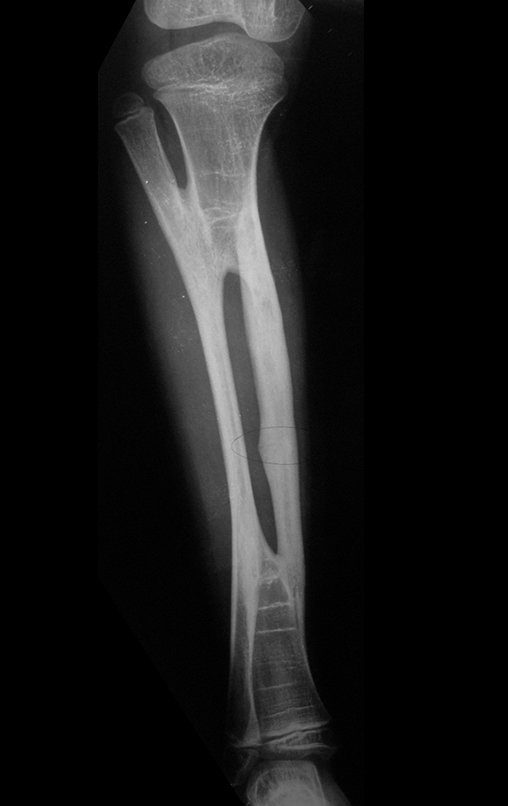
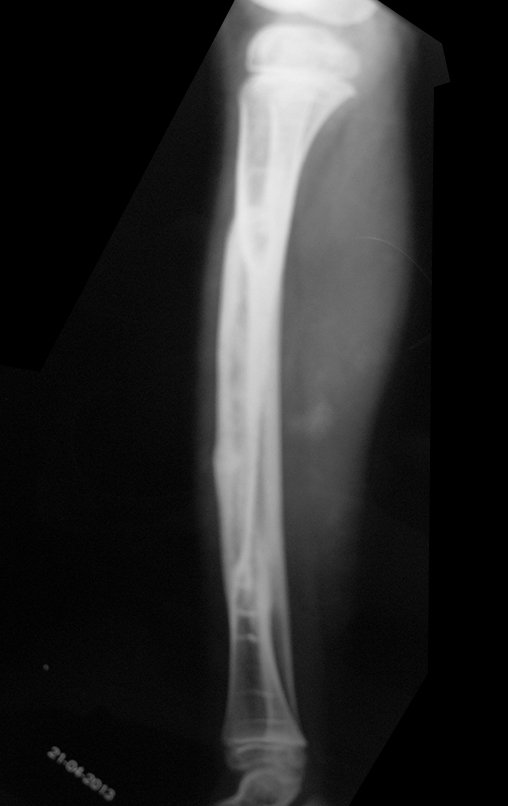
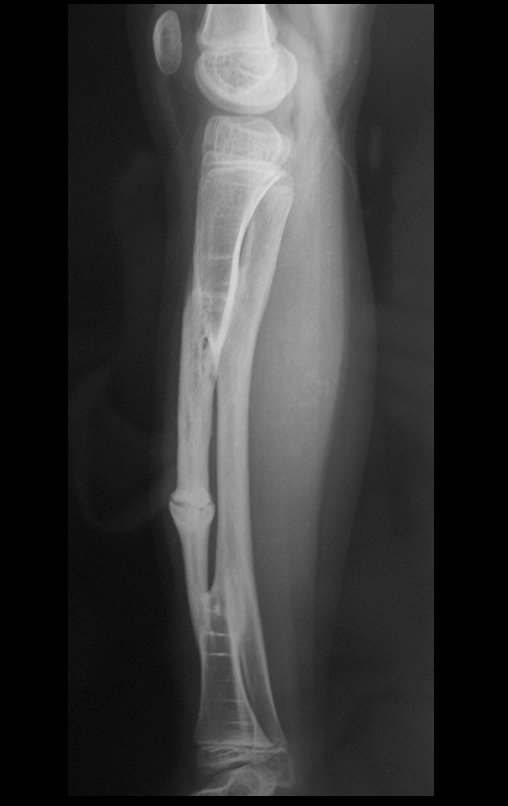
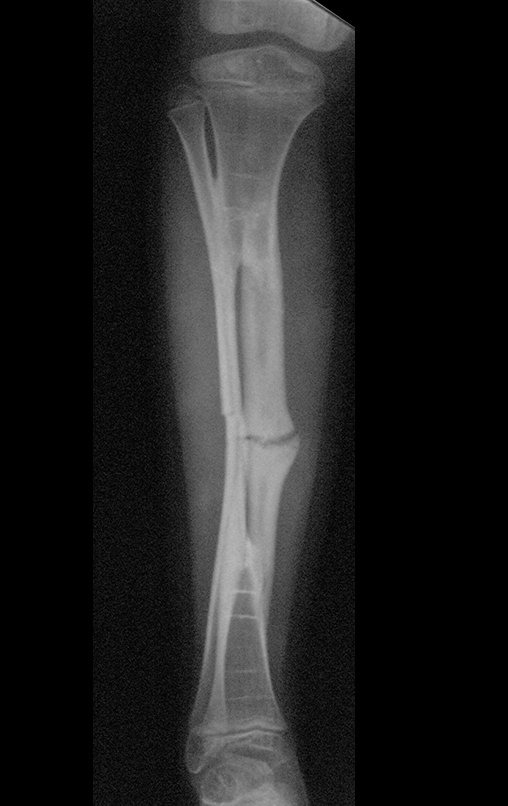
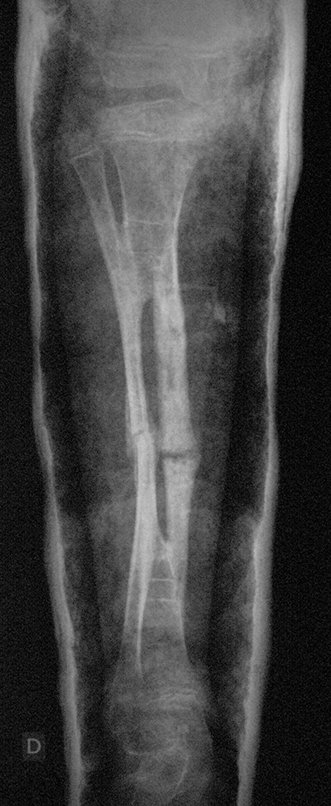
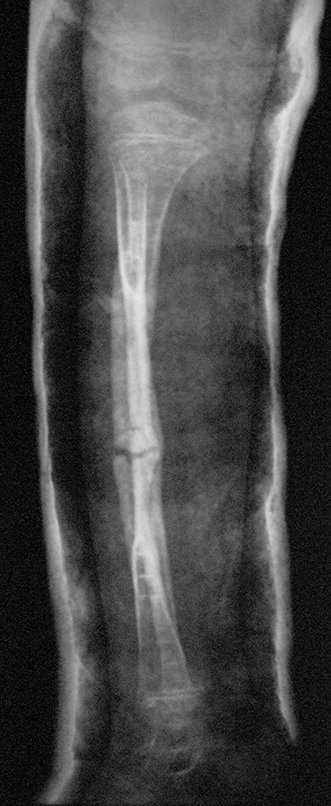
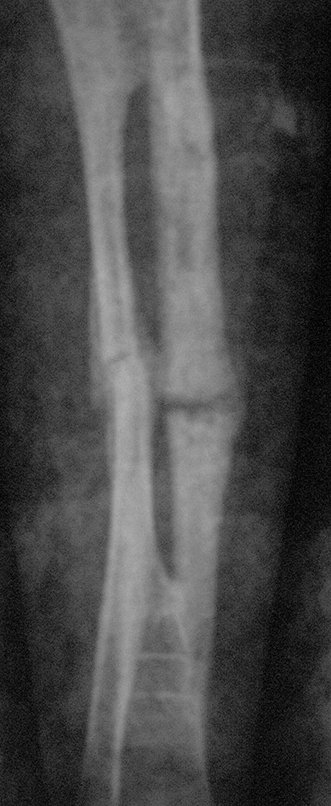
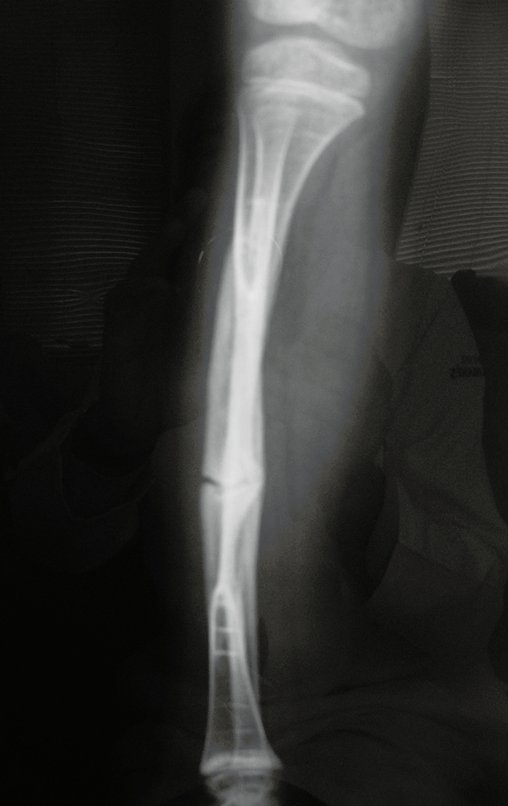
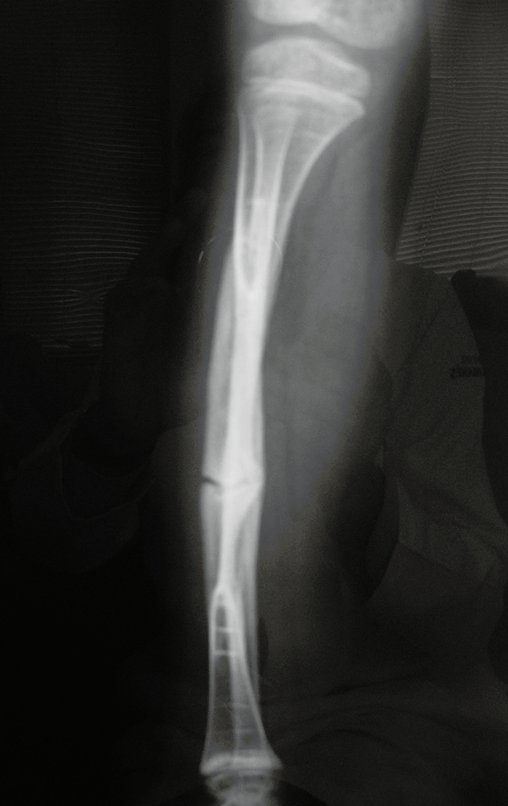
Técnica de Prótesis Total de Húmero en Osteosarcoma. Paciente masculino de 57 años refirió la aparición de dolor lumbar a finales de octubre de 2014, irradiado al MIE. Debido a la progresión de los síntomas se realizó resonancia de columna que reportó la presencia de hernia discal L5-S1. Inició fisioterapia y ante el empeoramiento de los síntomas se le realizó tomografía el 18/02/2015, con reporte de artrosis facetaria L2-L3, L3-L4 y discopatía L5-S1 con protrusión en canal medular y radiografías de pelvis, figuras 1 y 2.
Técnica de Prótesis Total de Húmero en Osteosarcoma.
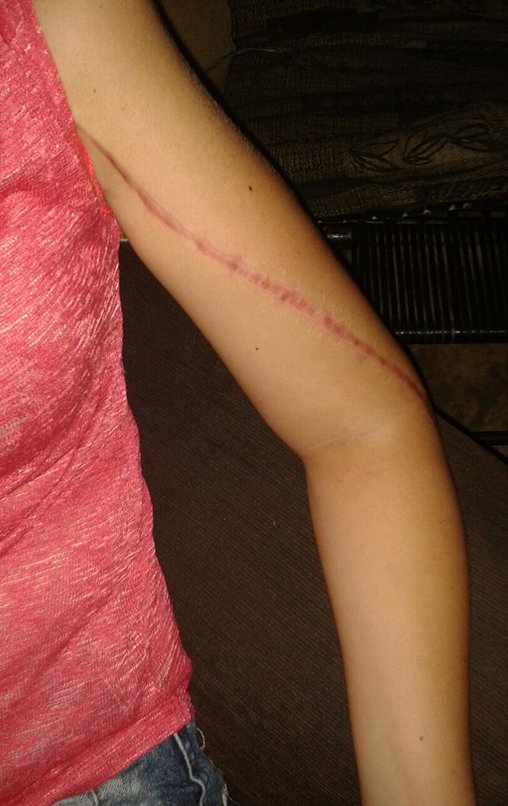
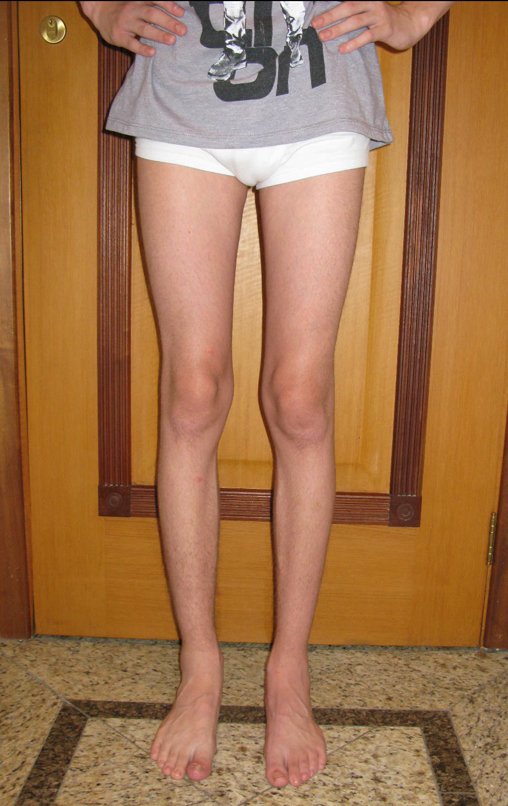
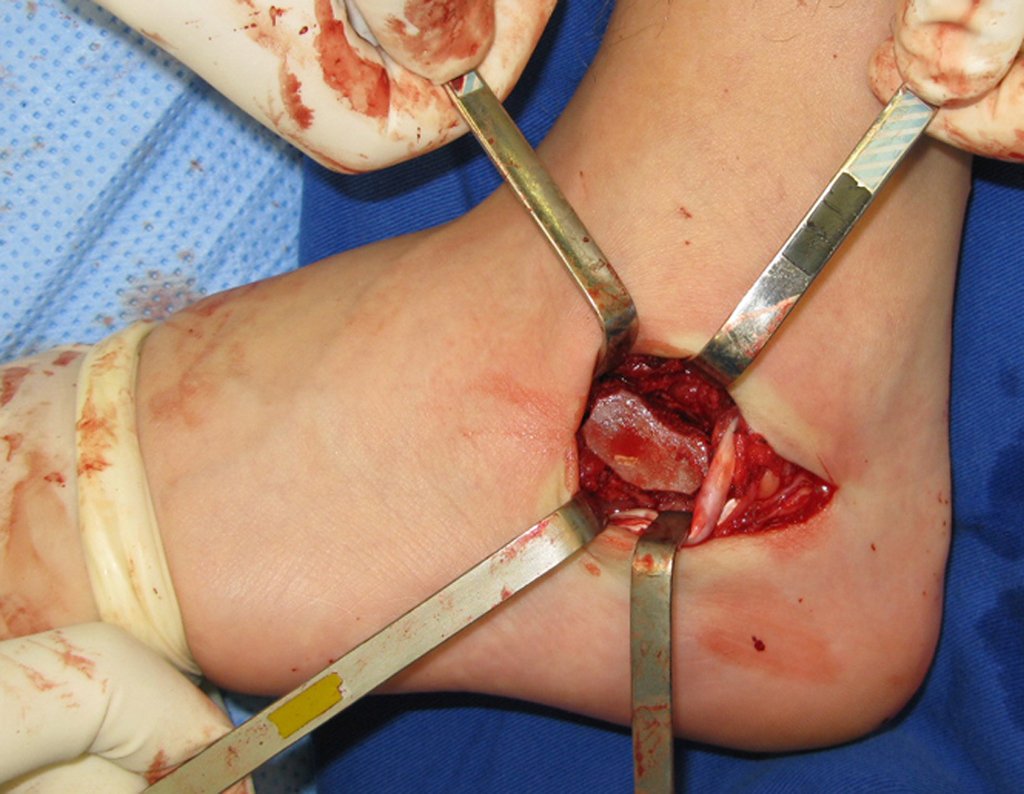
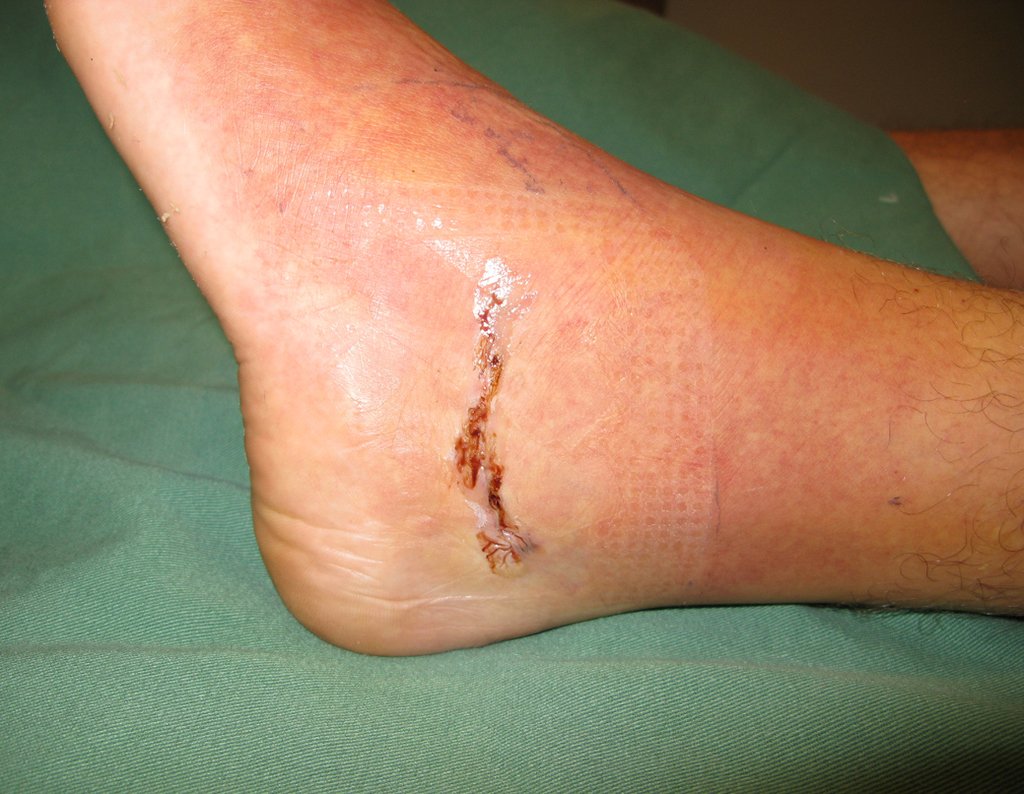
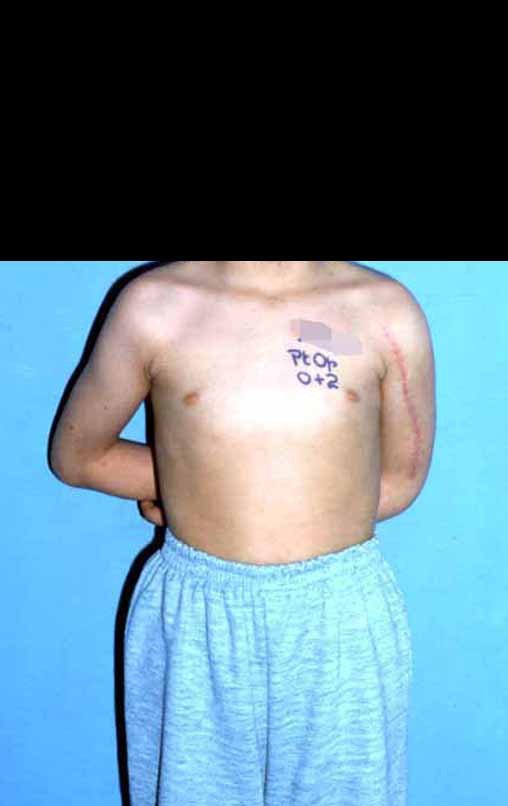
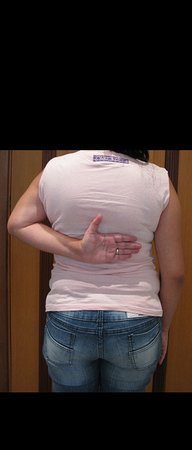
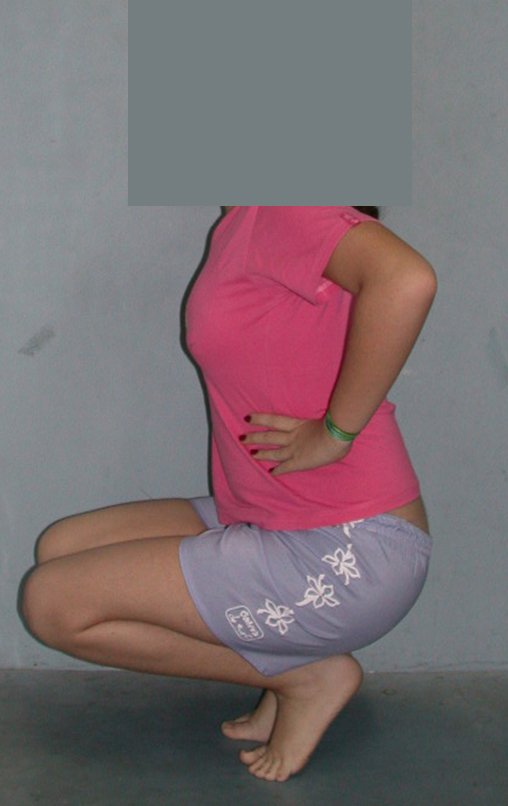
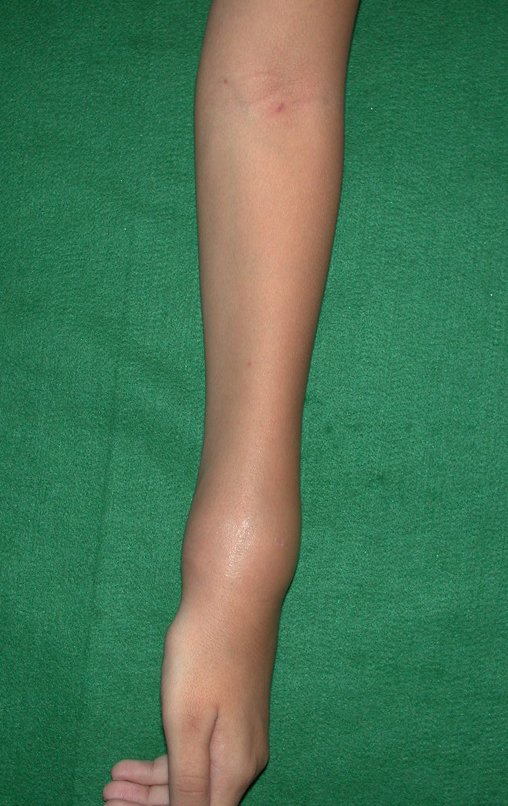
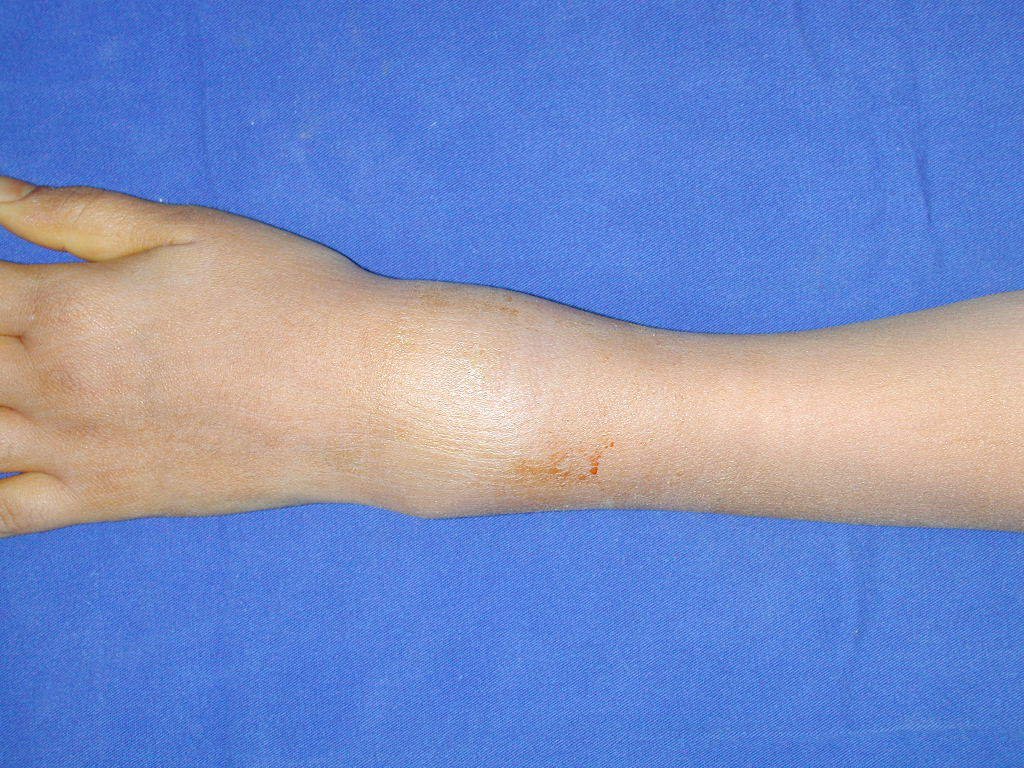
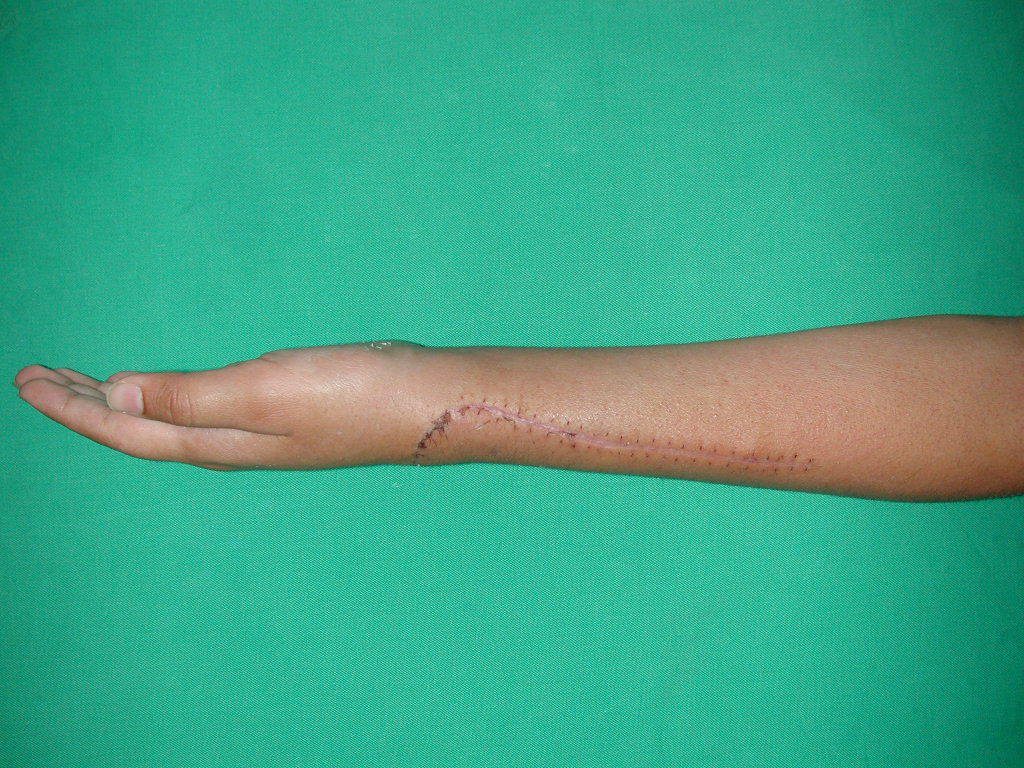
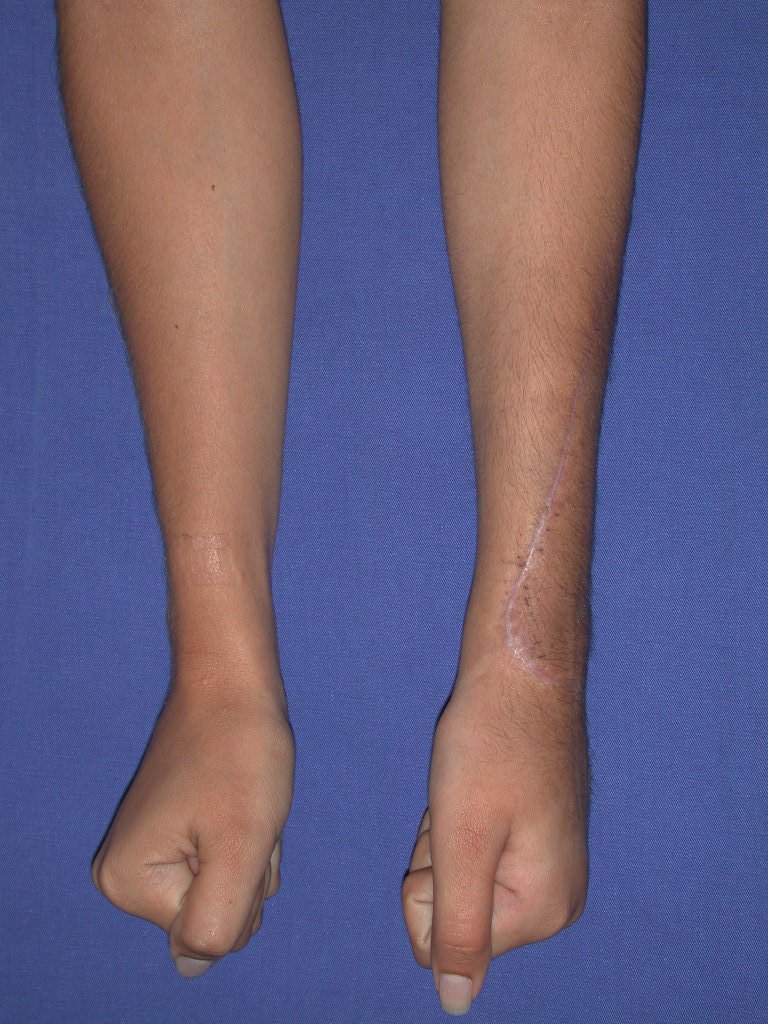
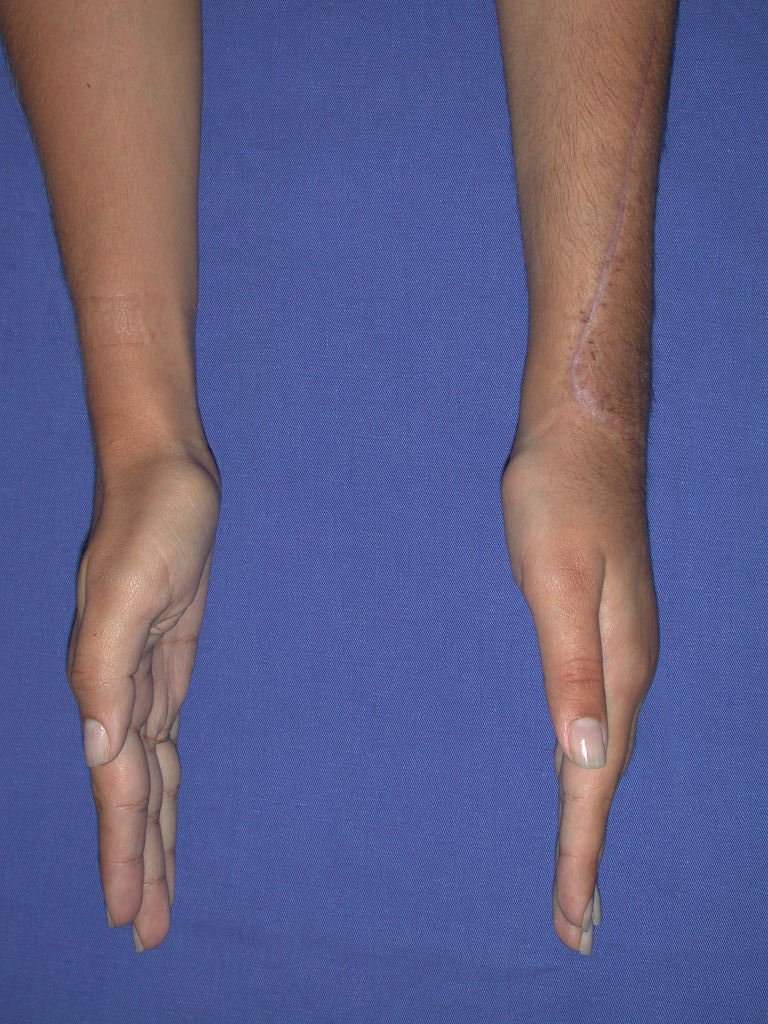
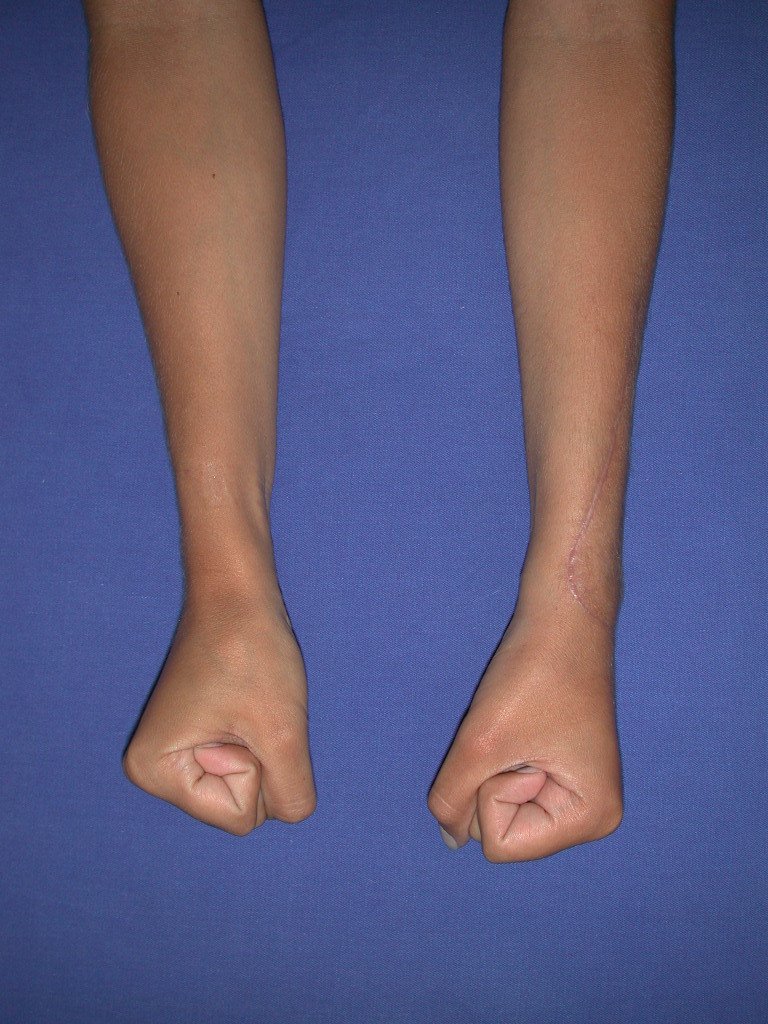
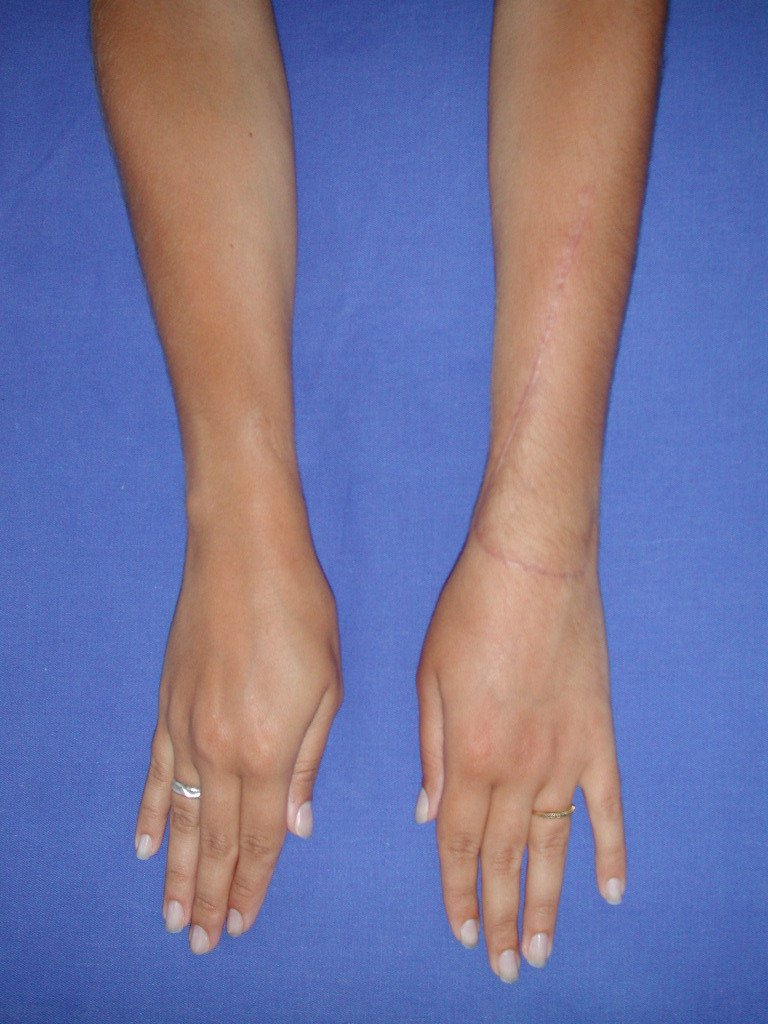
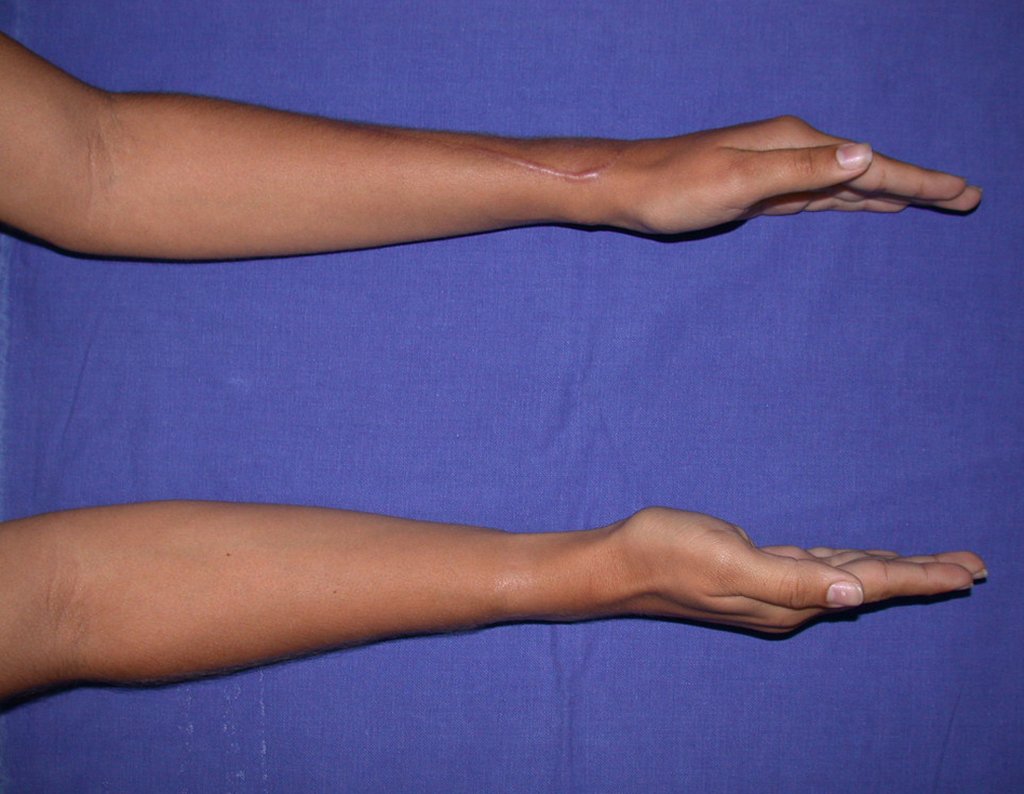
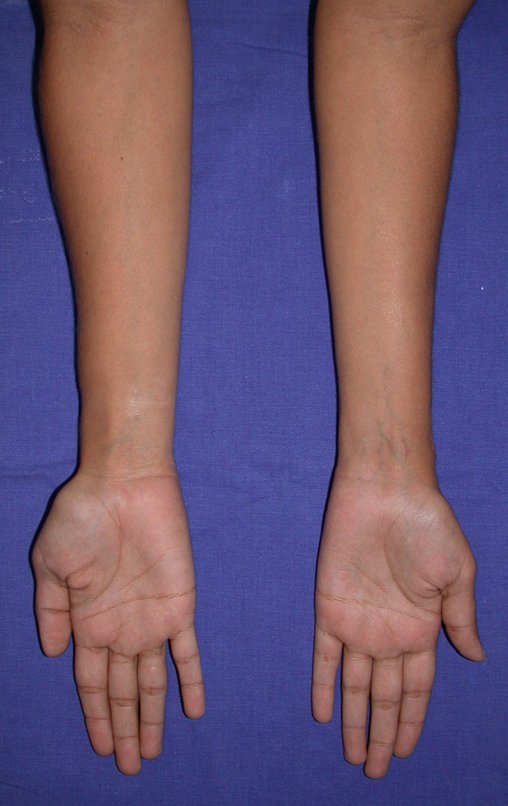
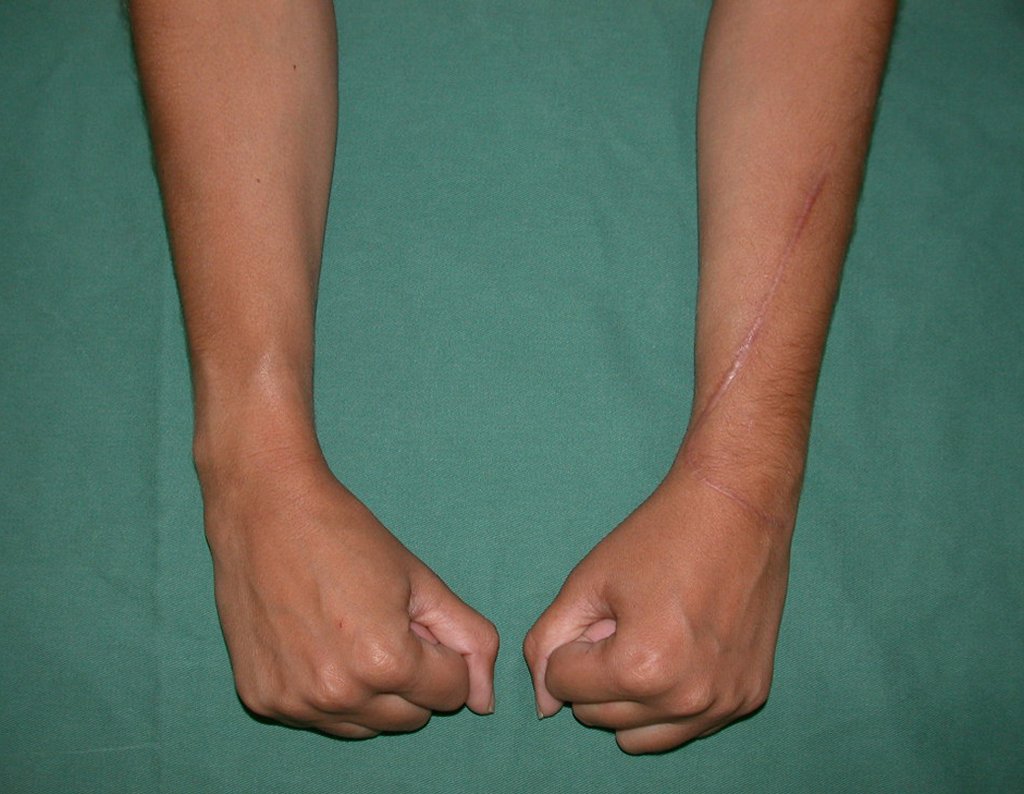
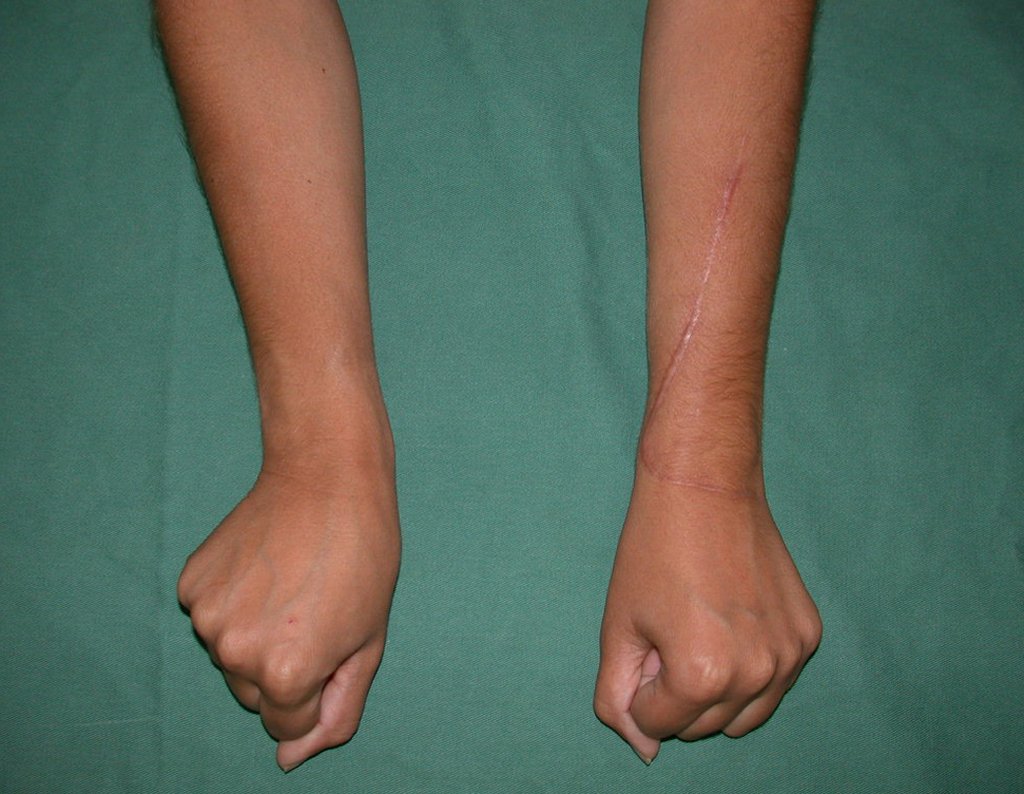
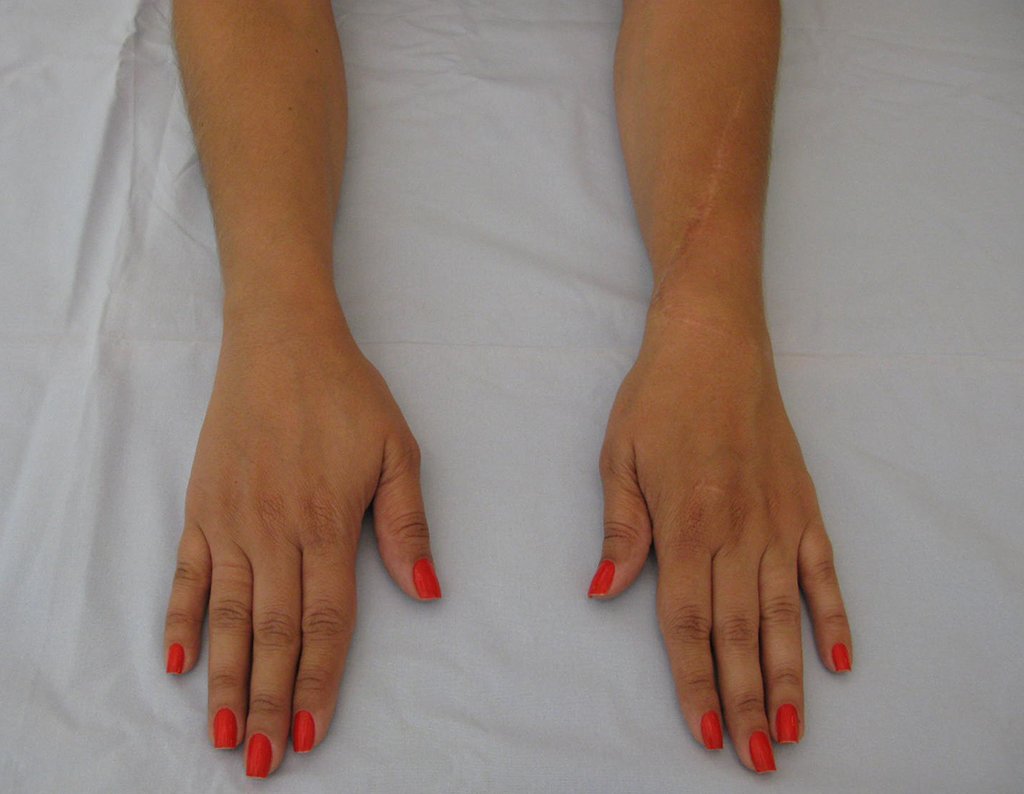
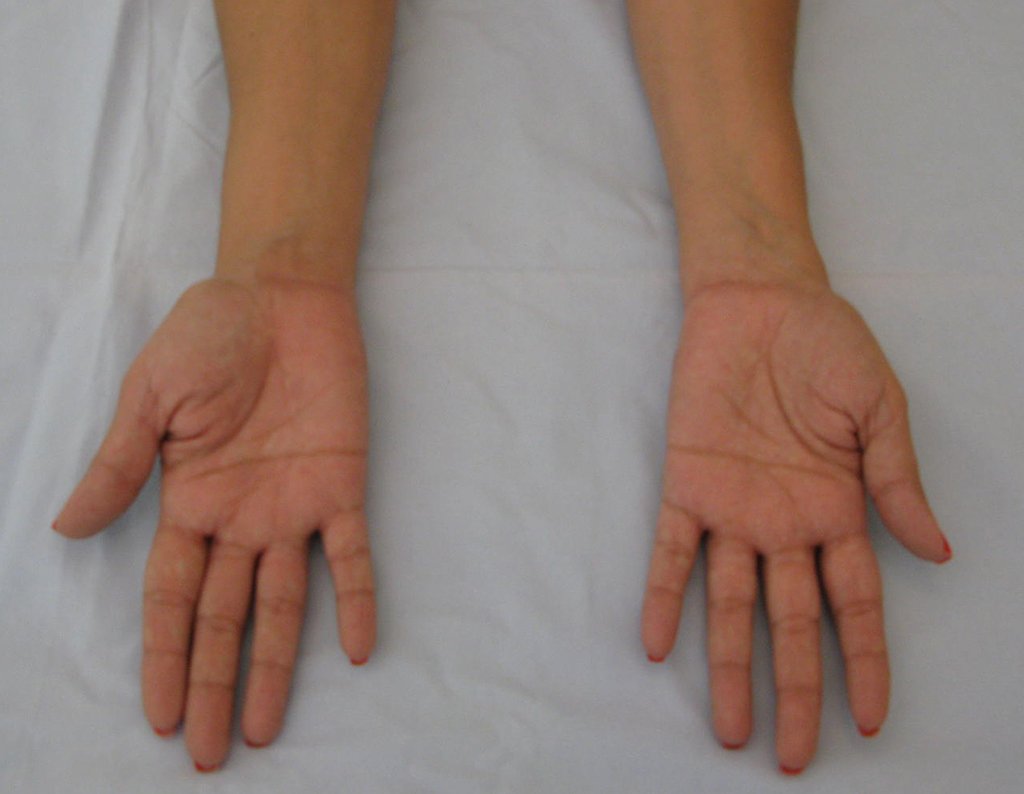
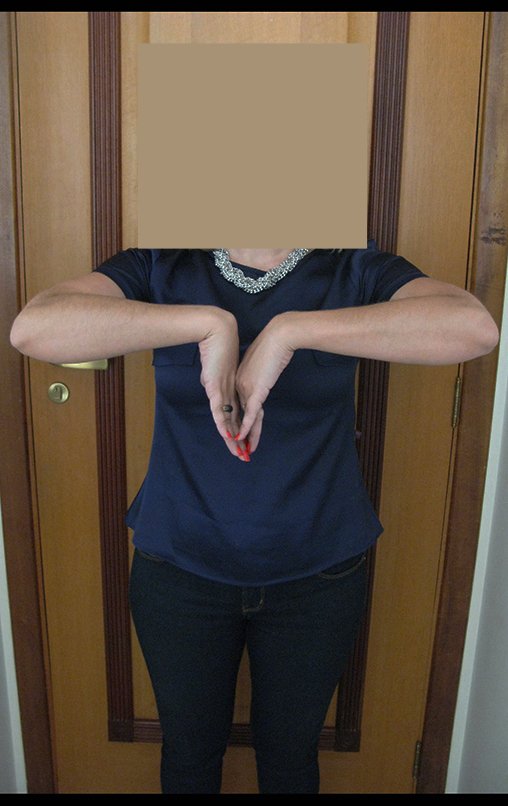
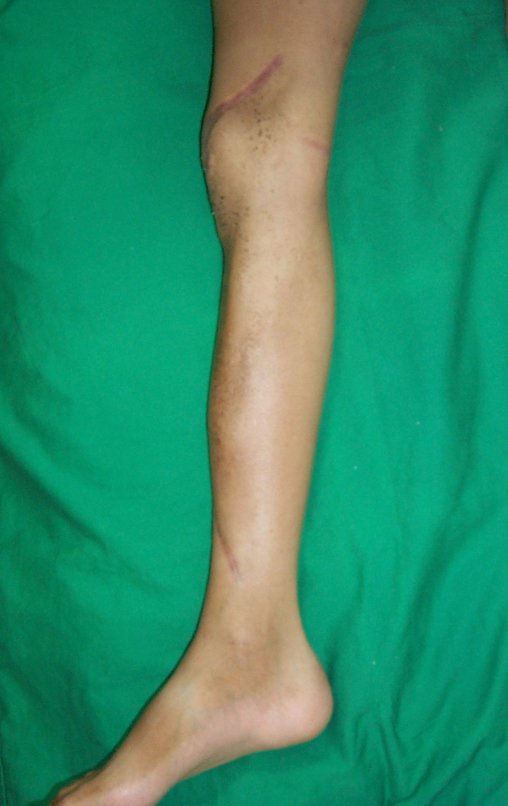
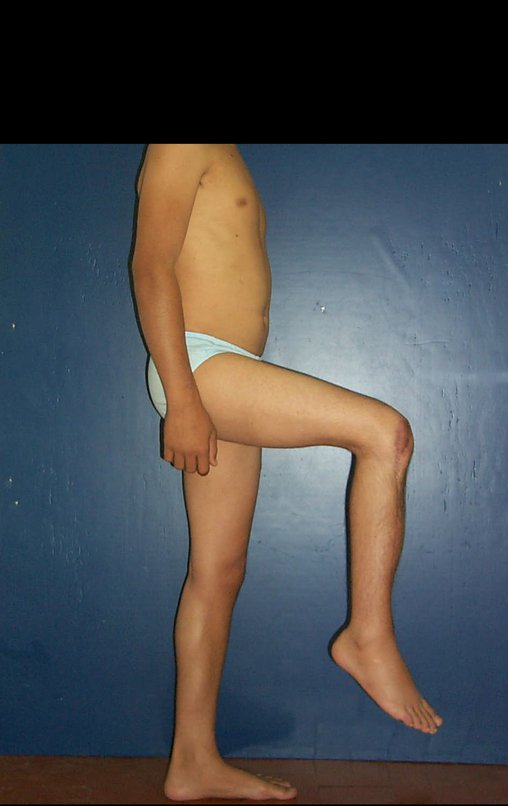
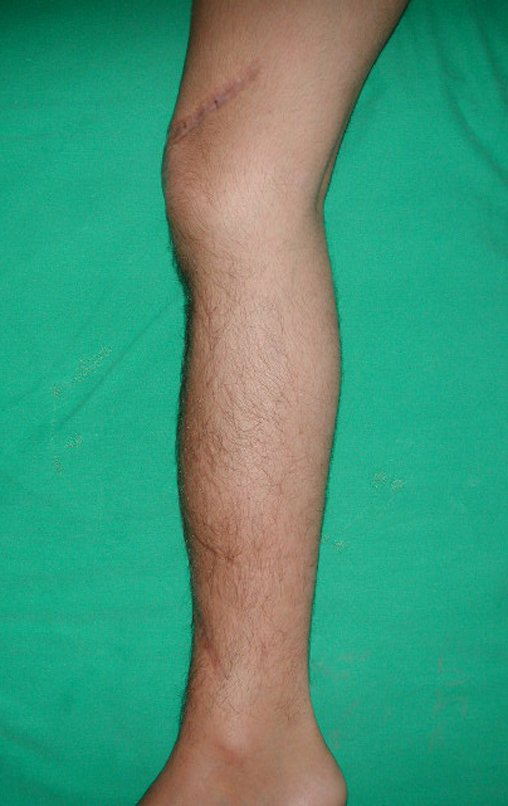
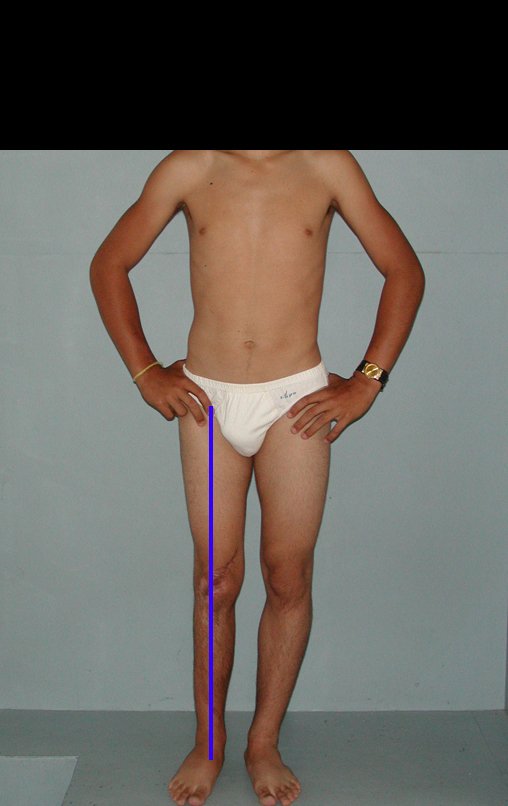
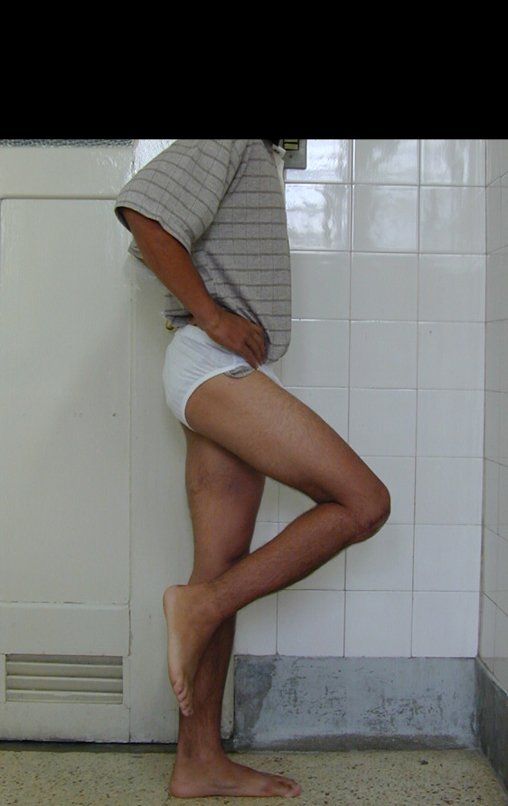
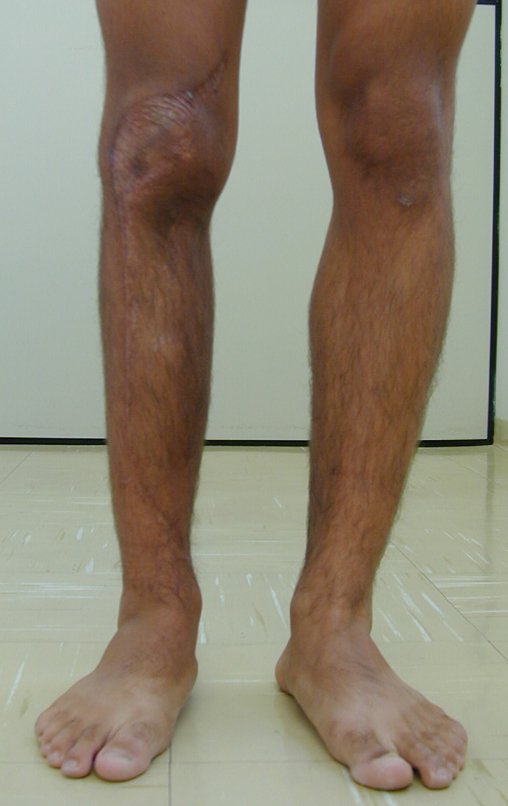
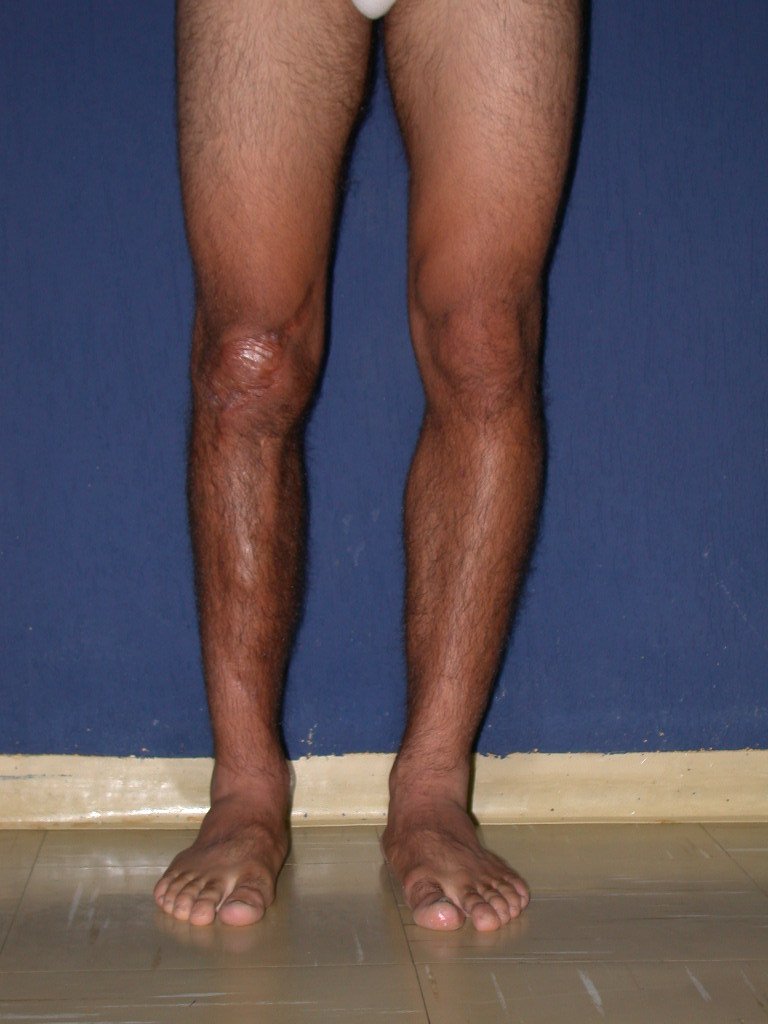
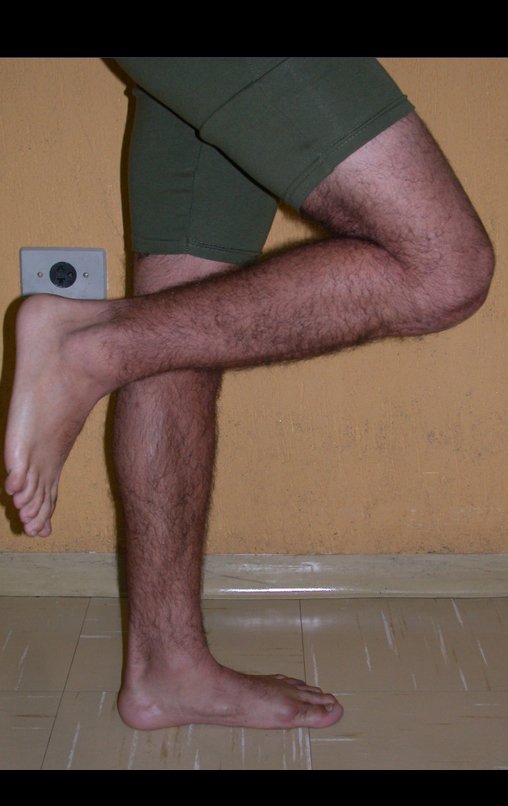
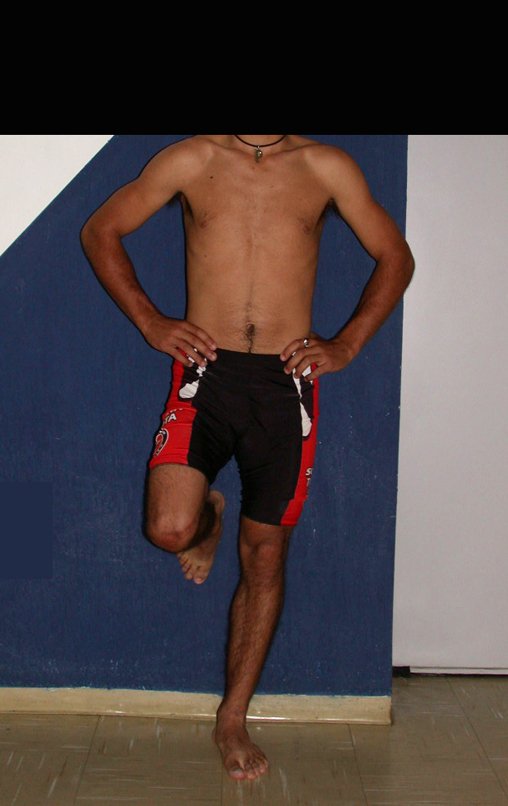
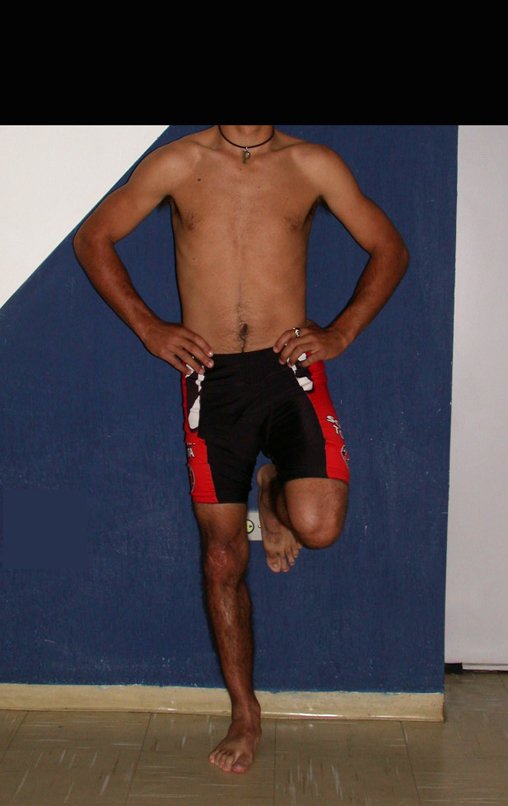
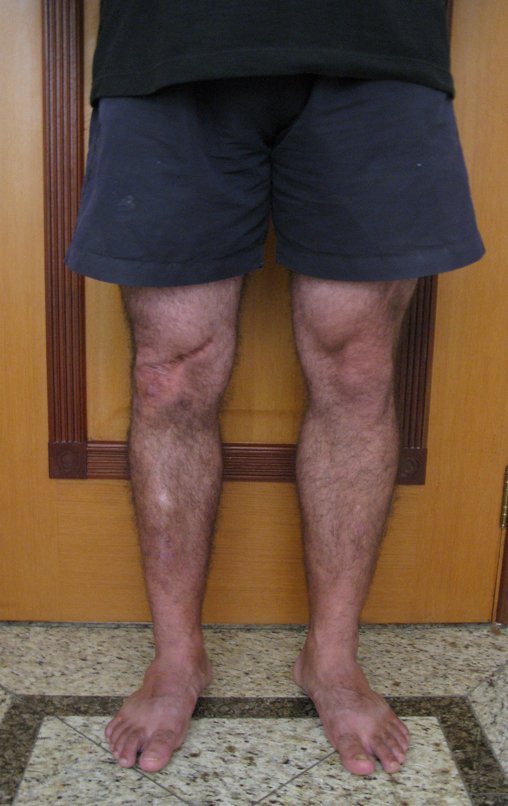
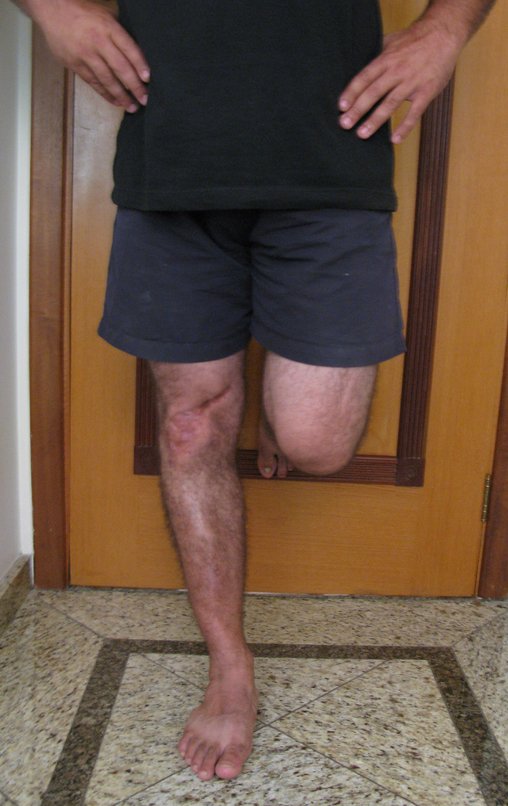
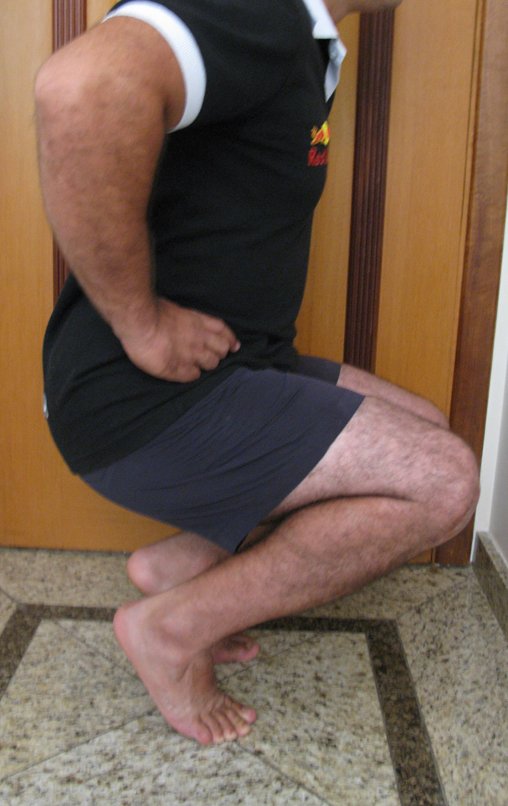
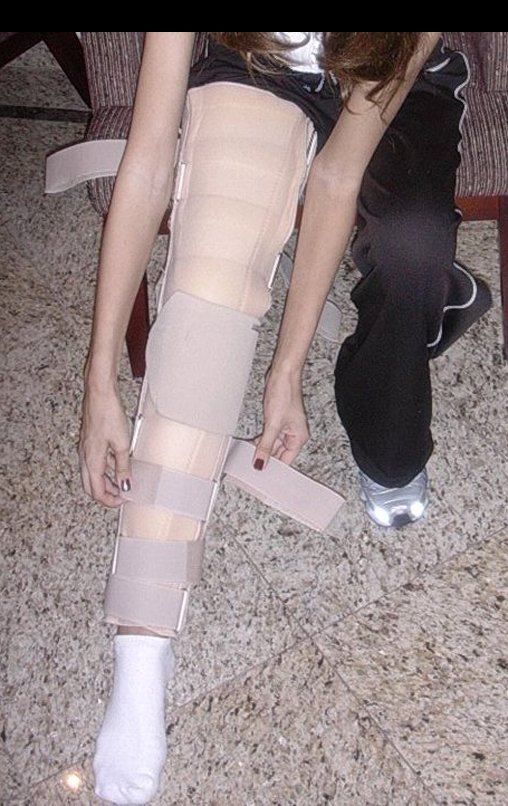
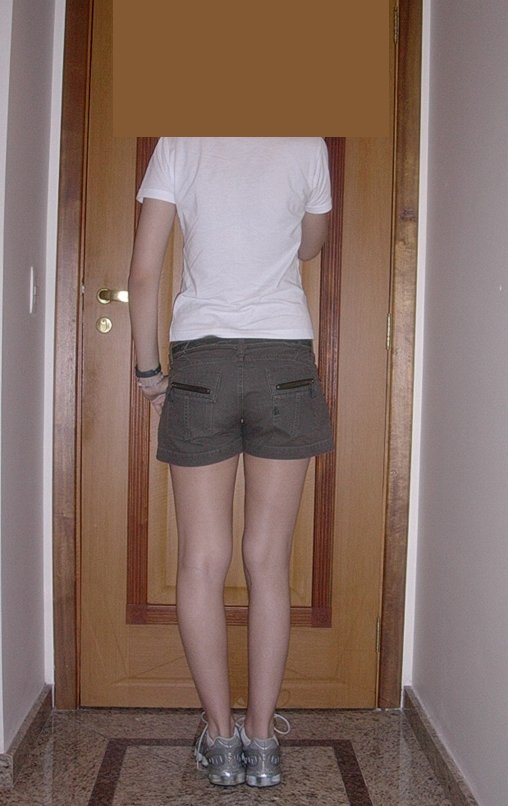
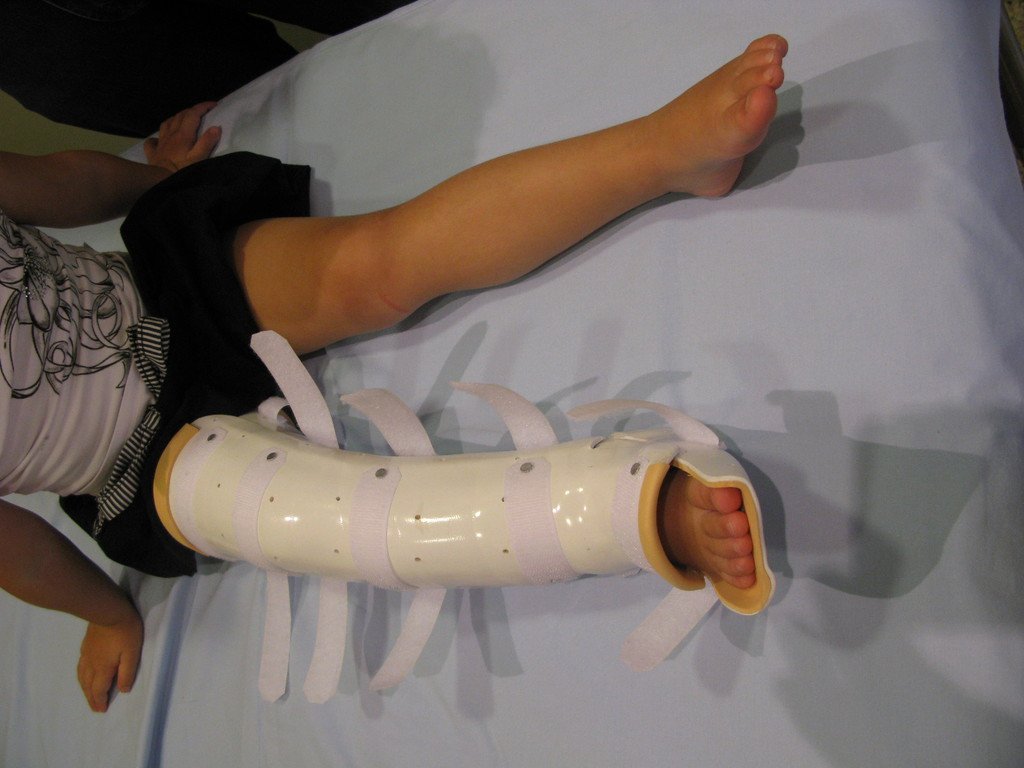
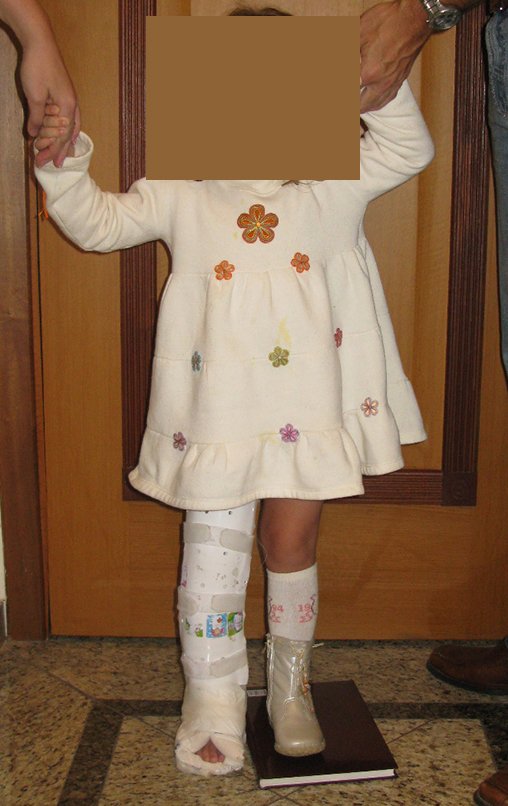
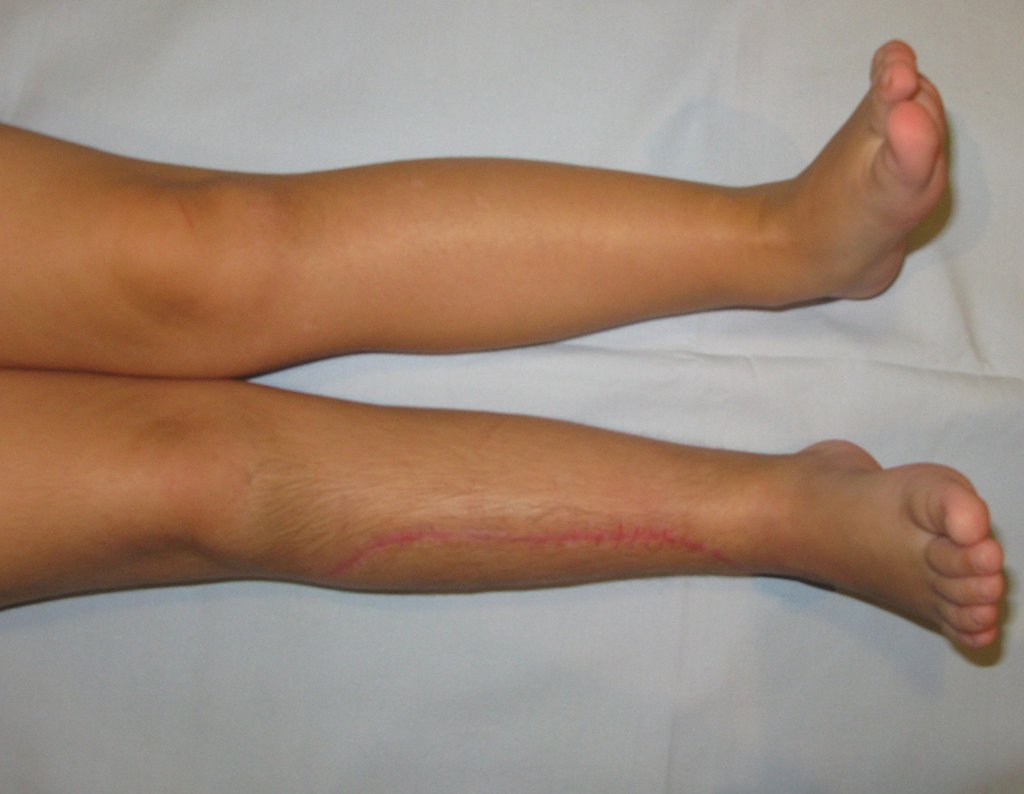
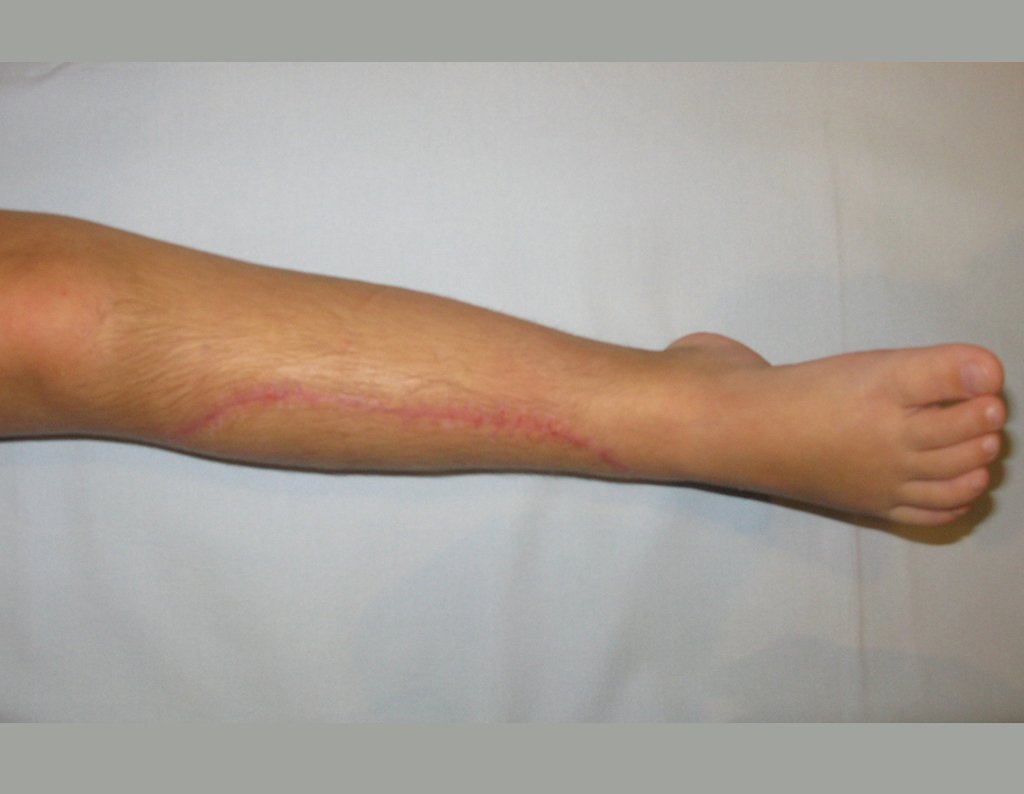
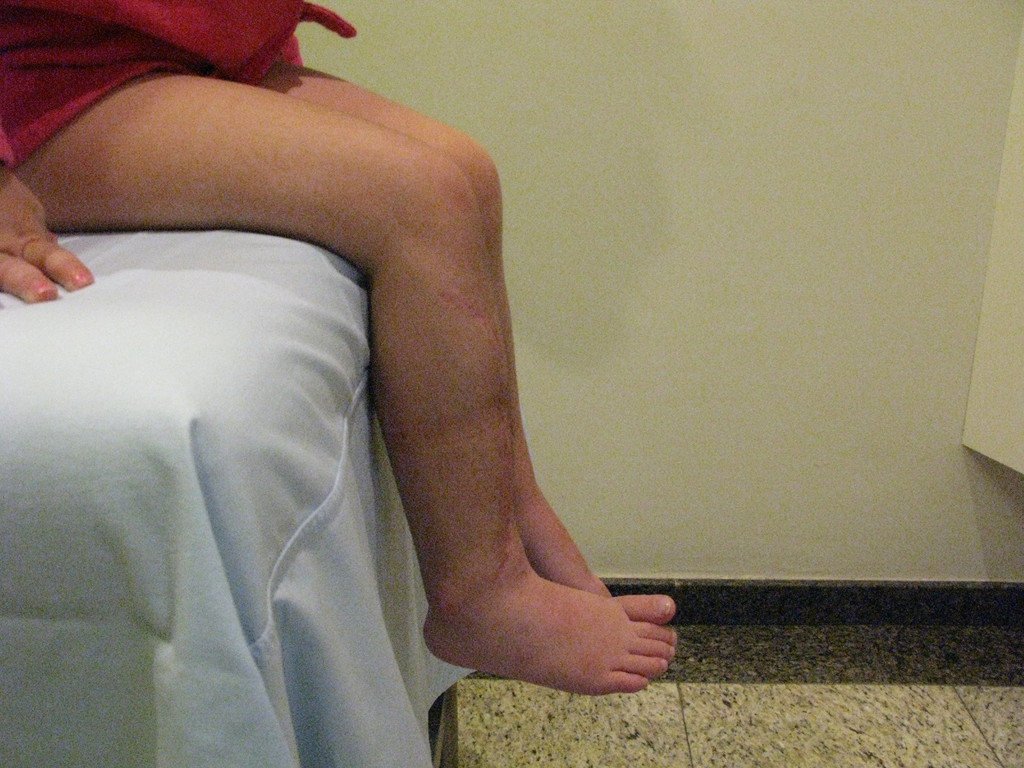
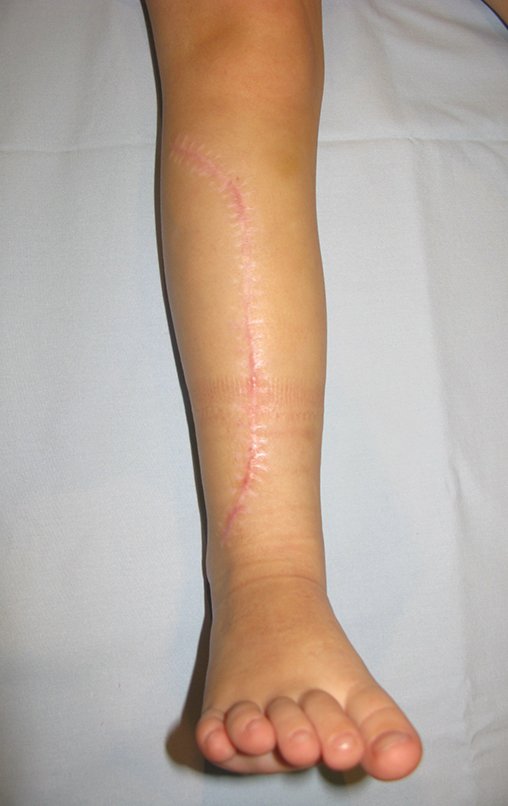
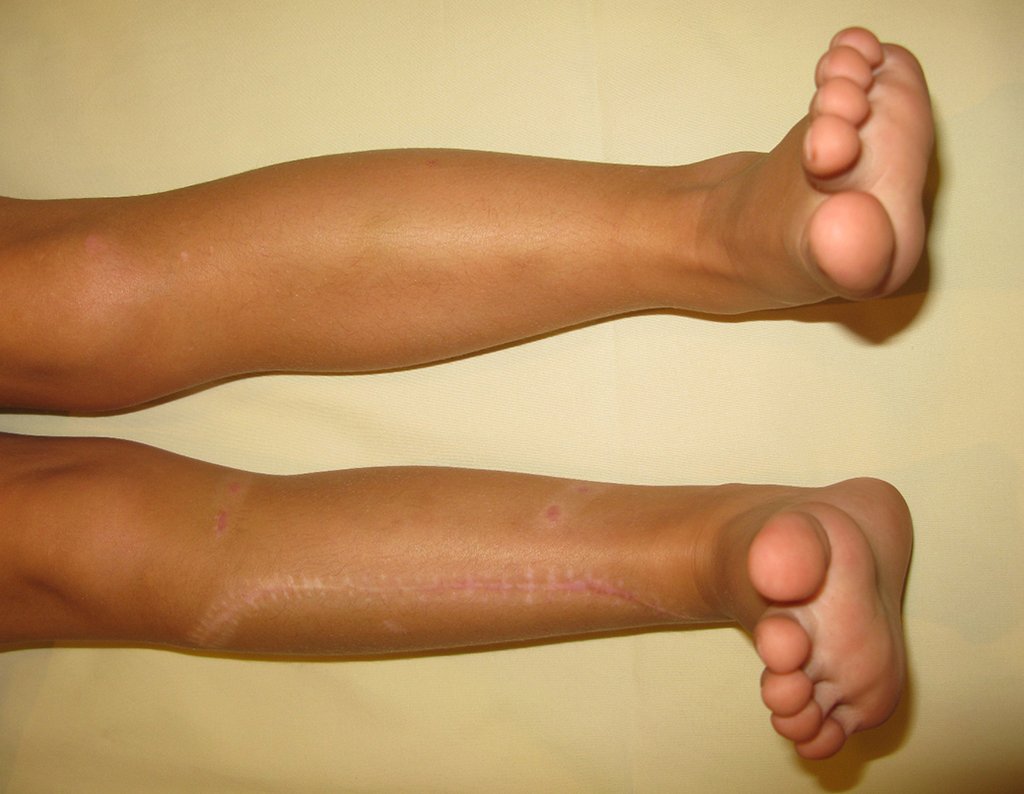
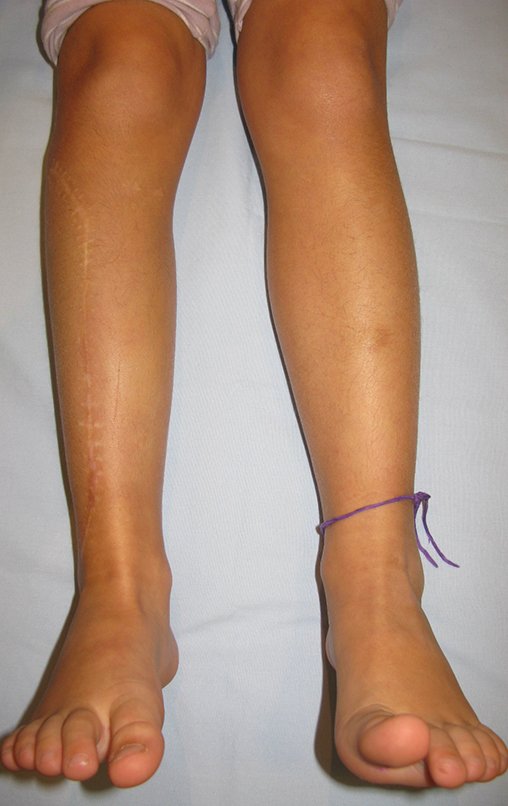
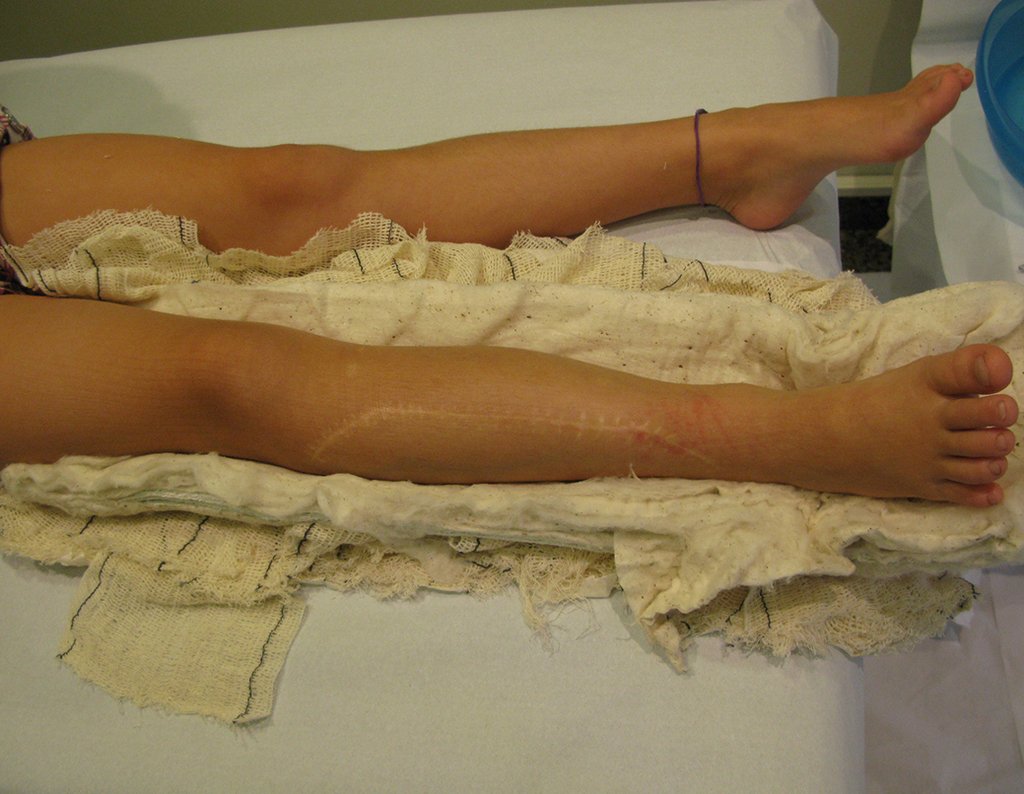
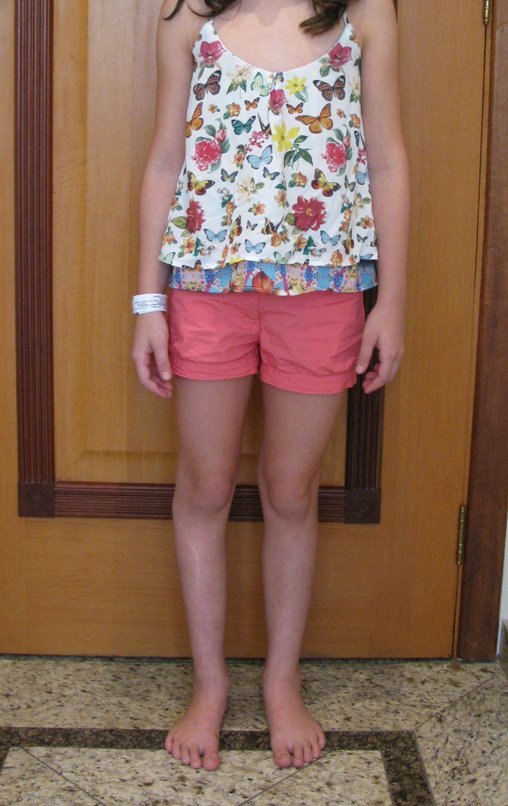
El aspecto clínico y la función del miembro superior izquierdo se pueden observar en las figuras 27 a 29.
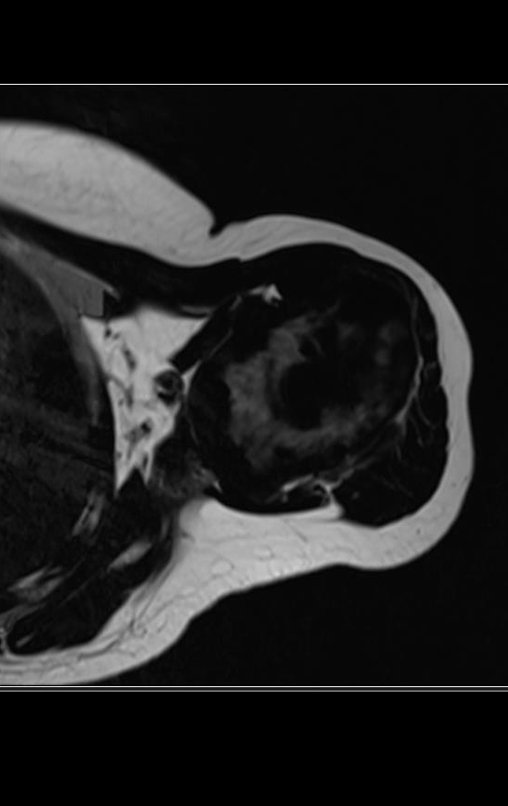
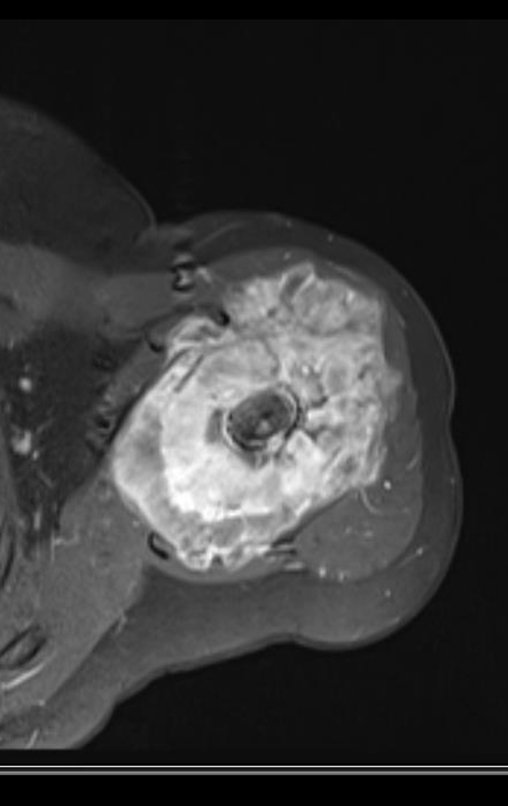
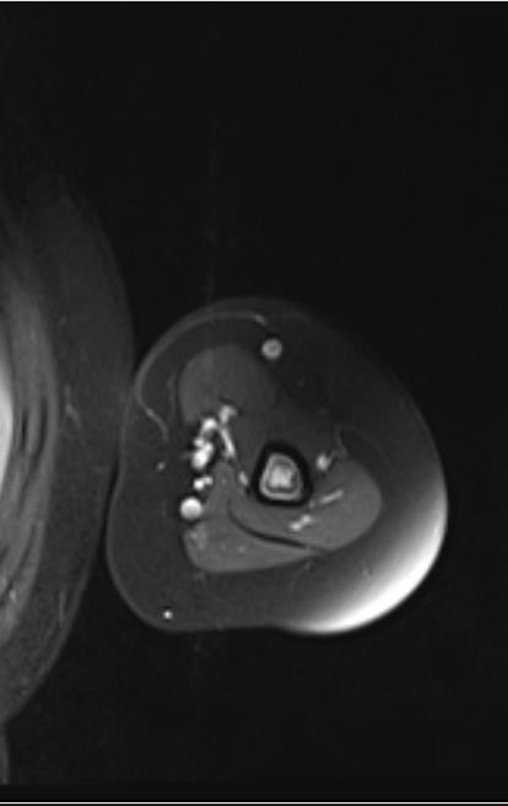
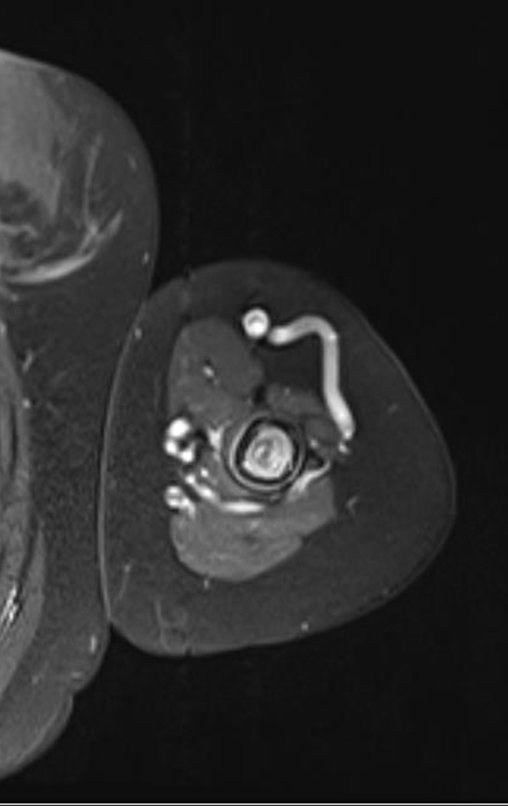
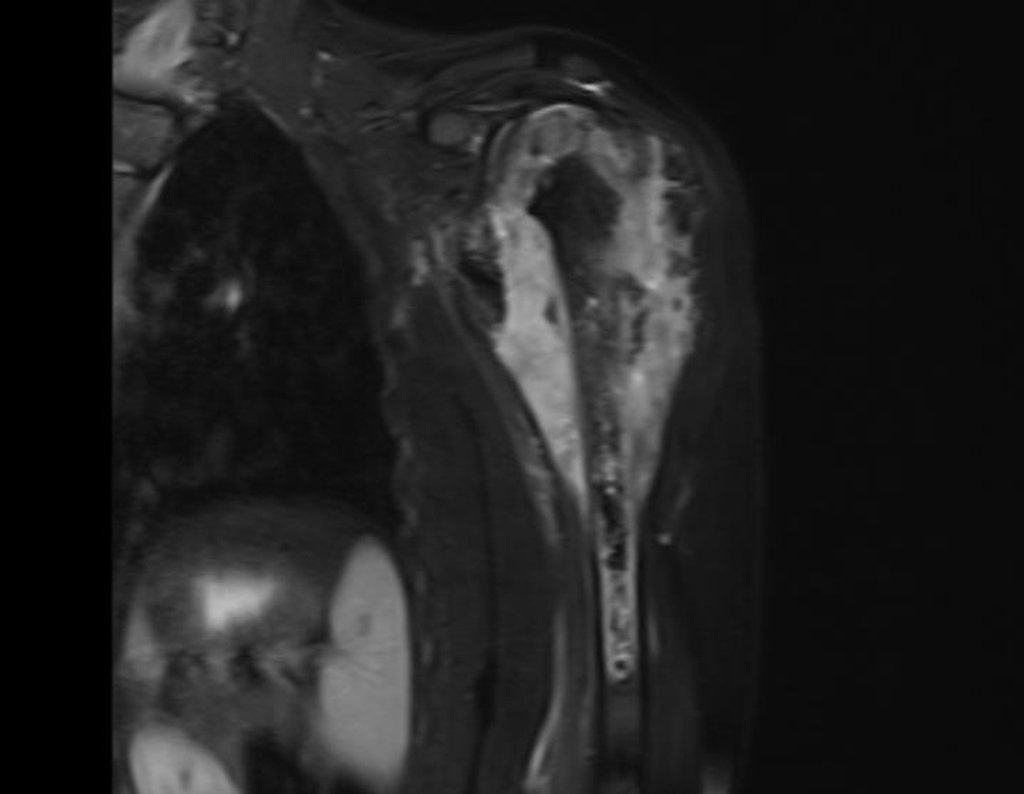
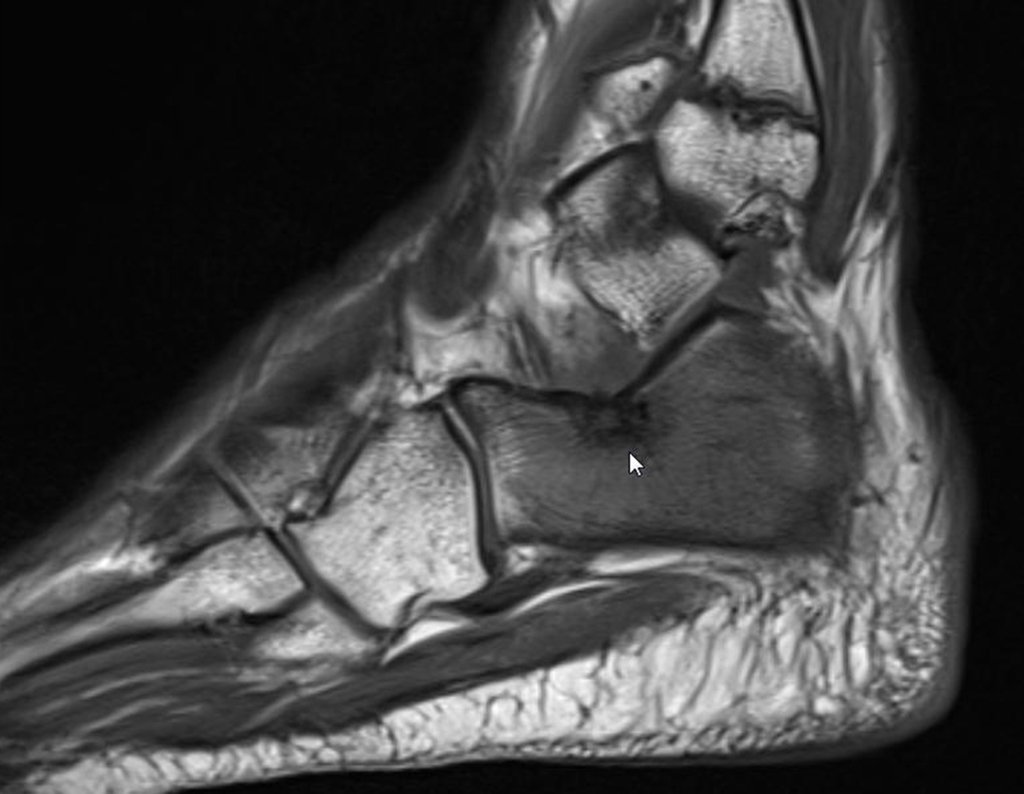
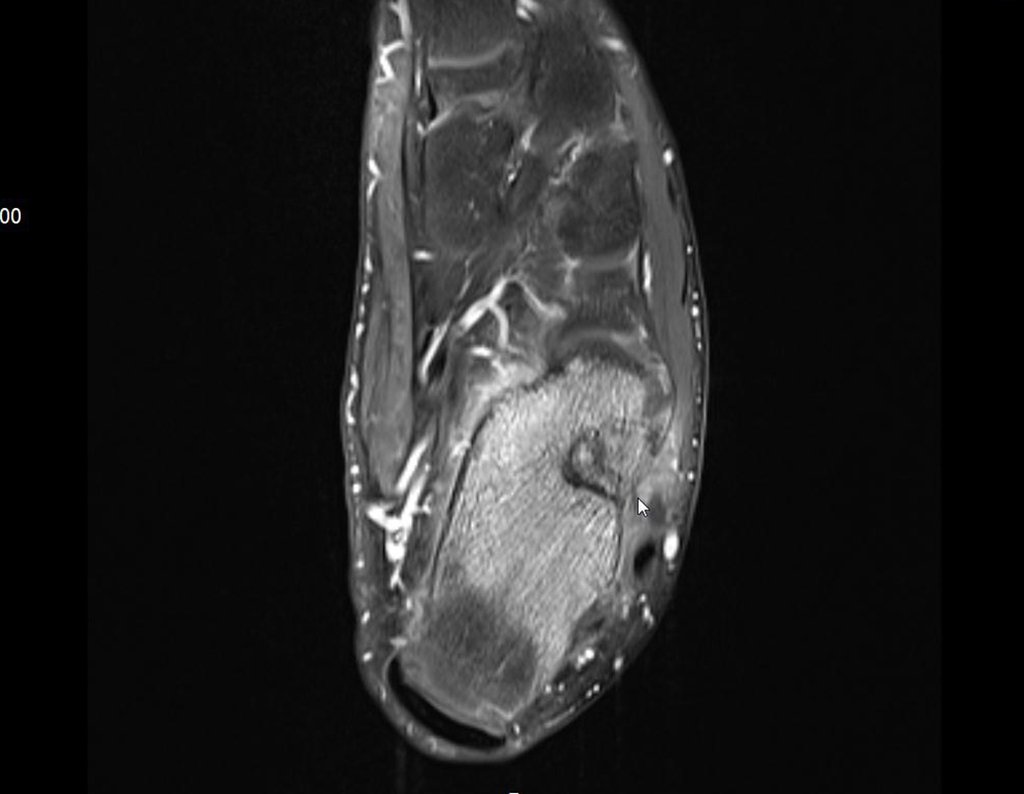
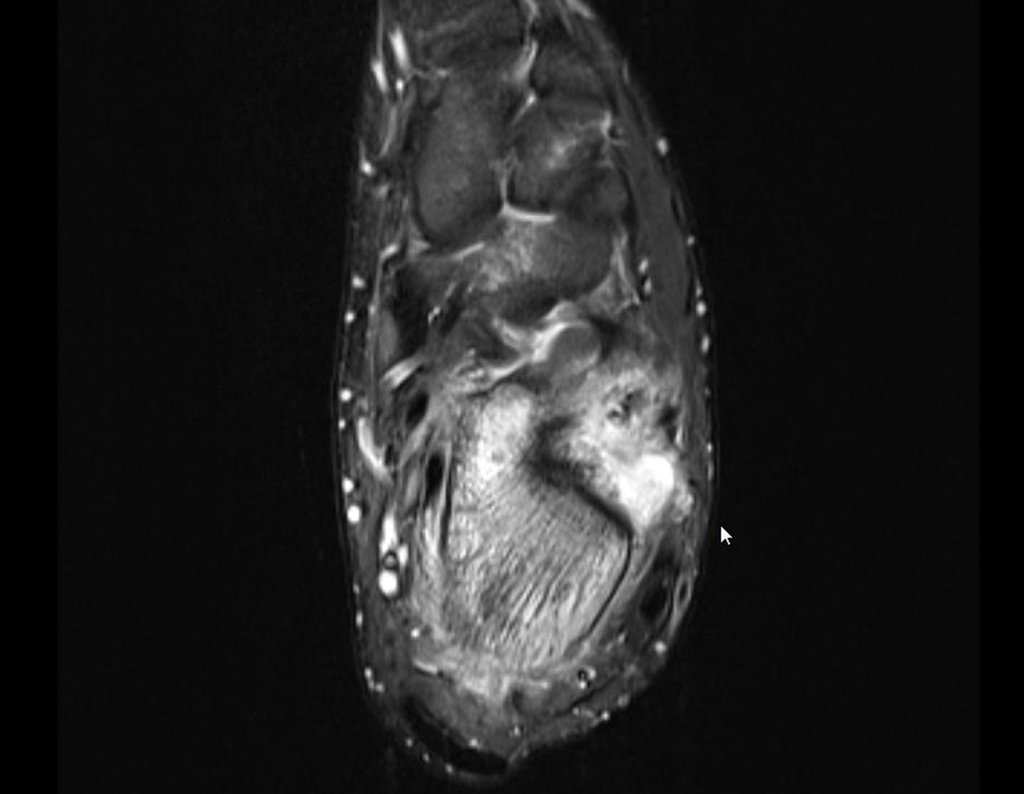
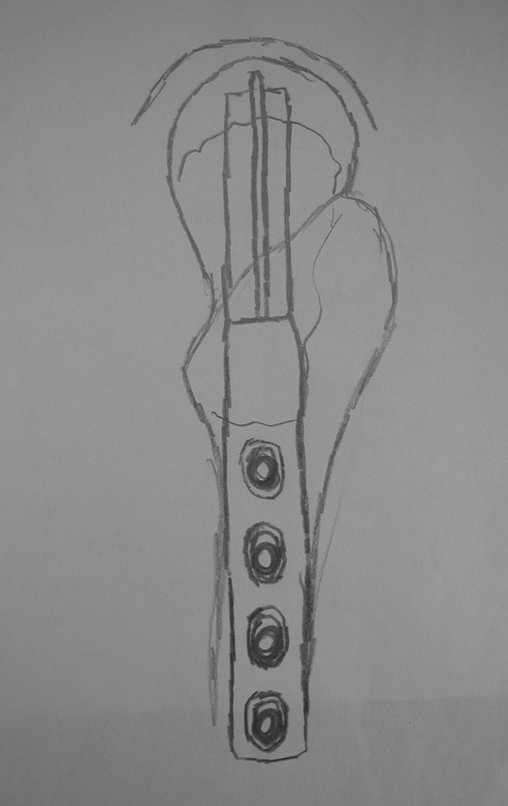
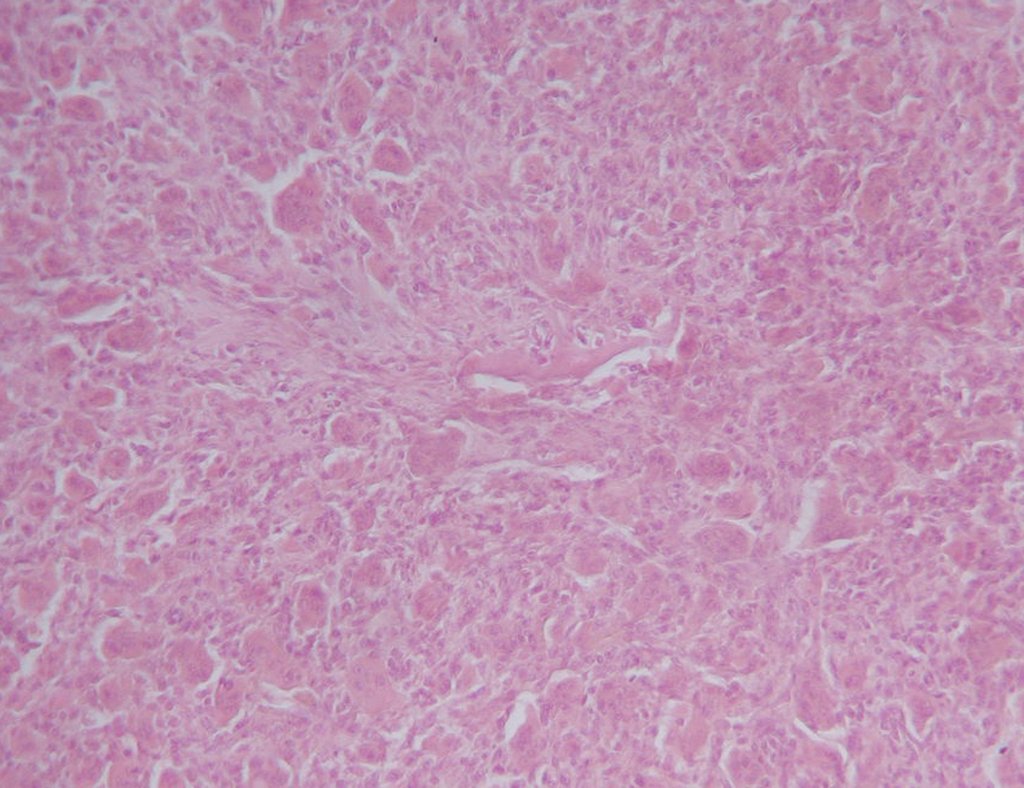
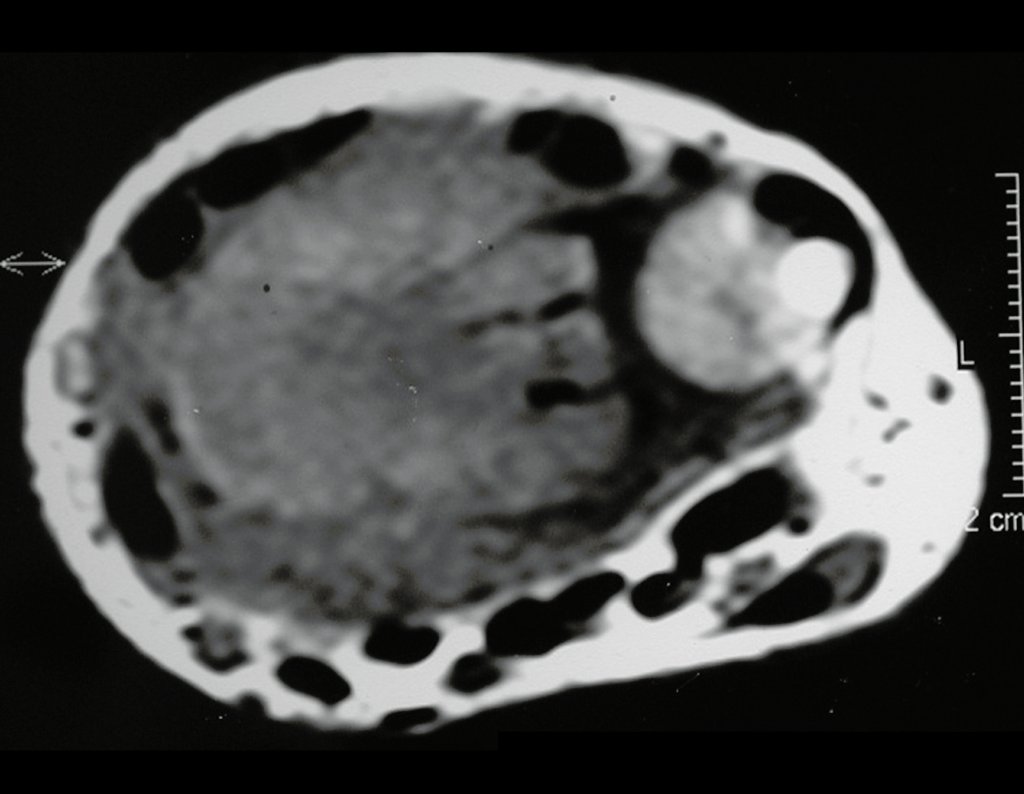
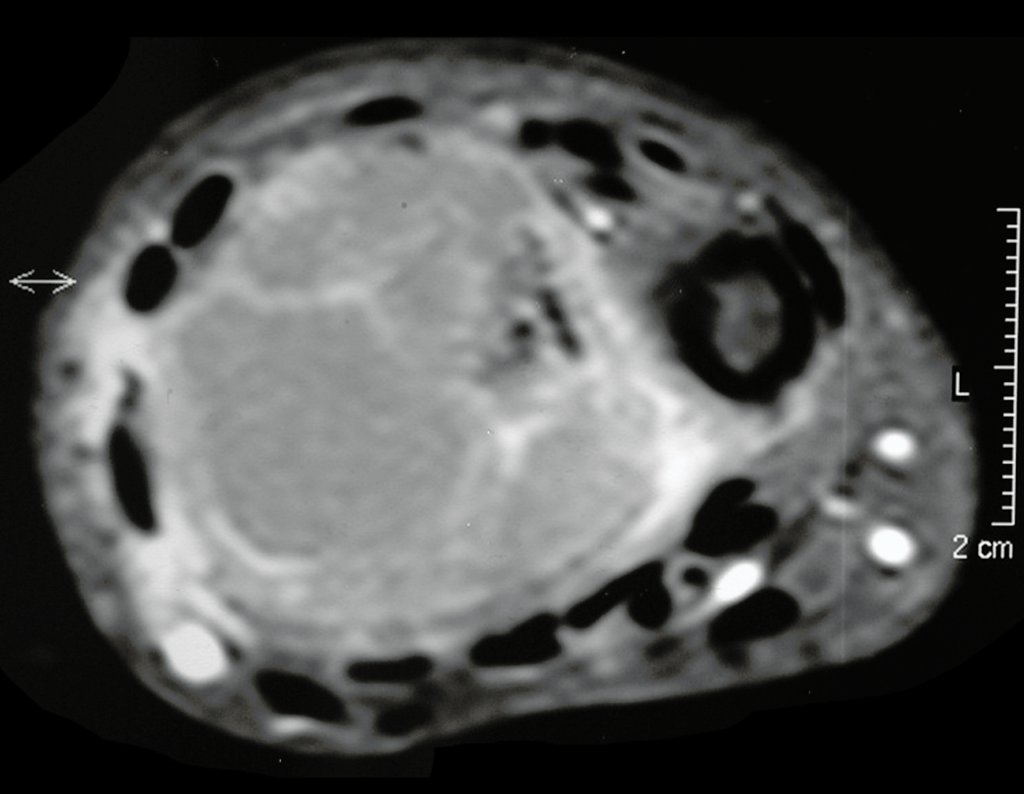
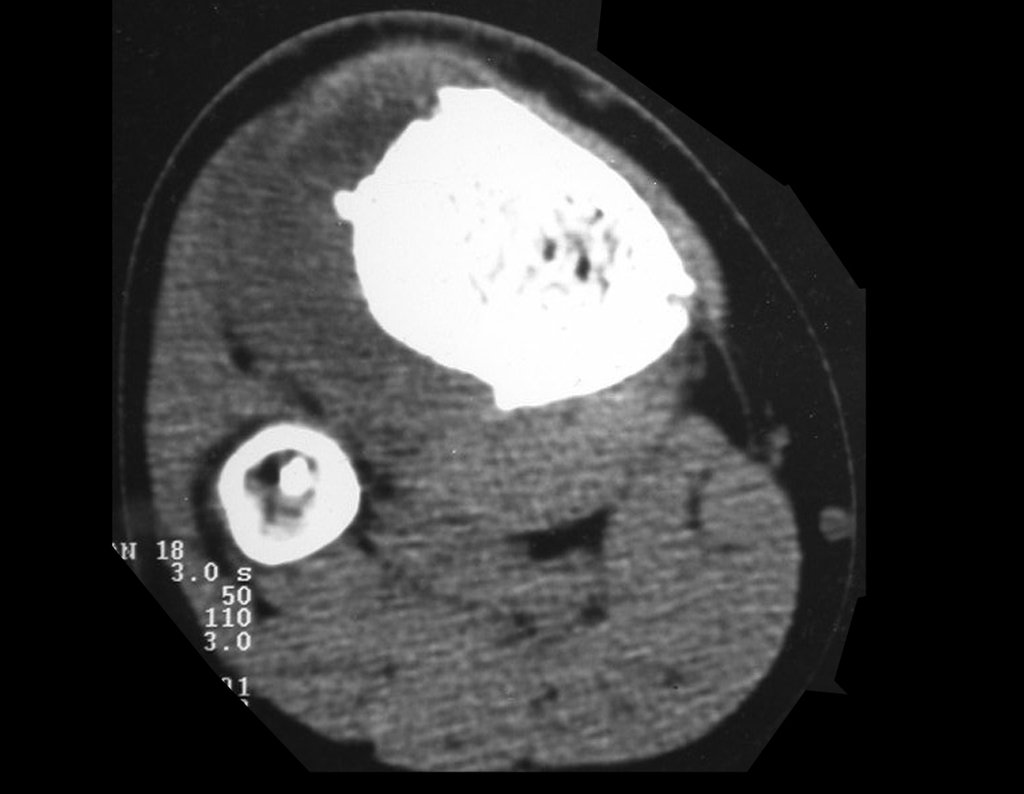
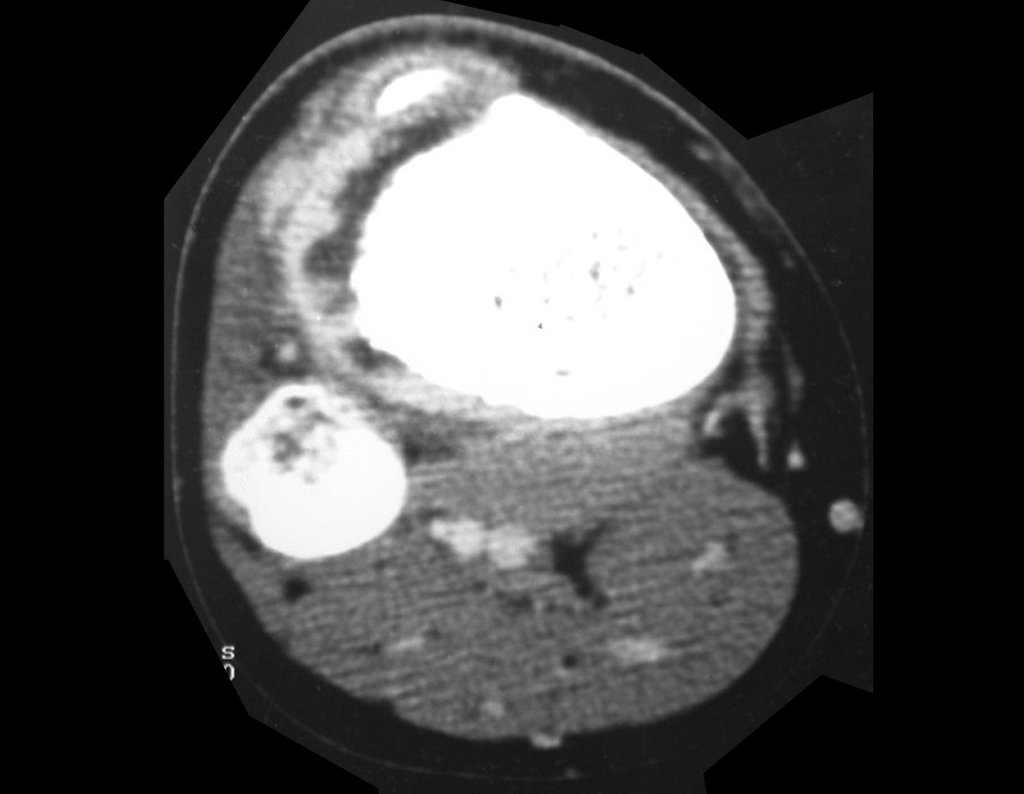
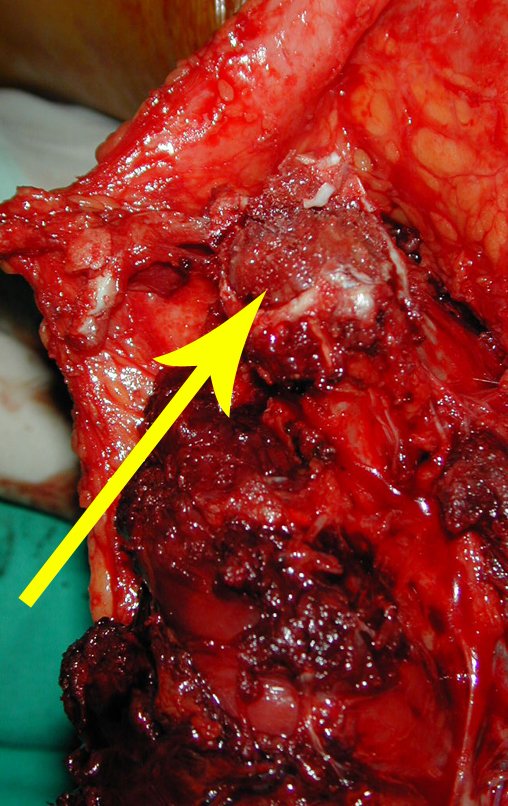
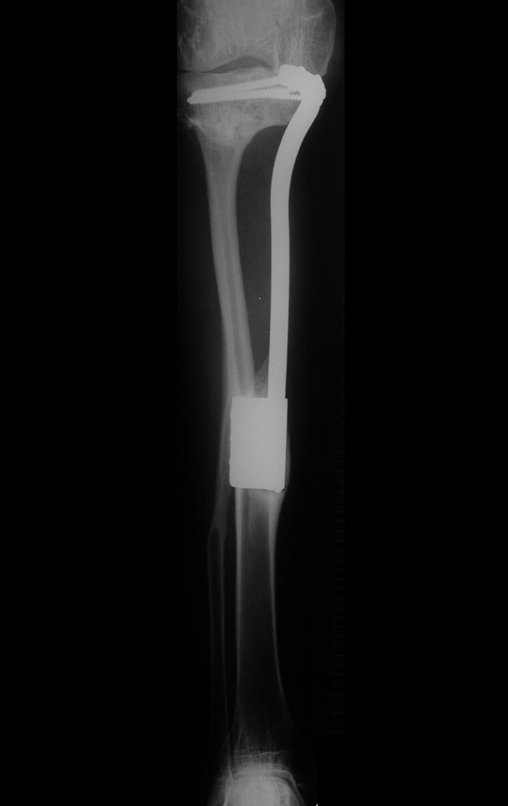
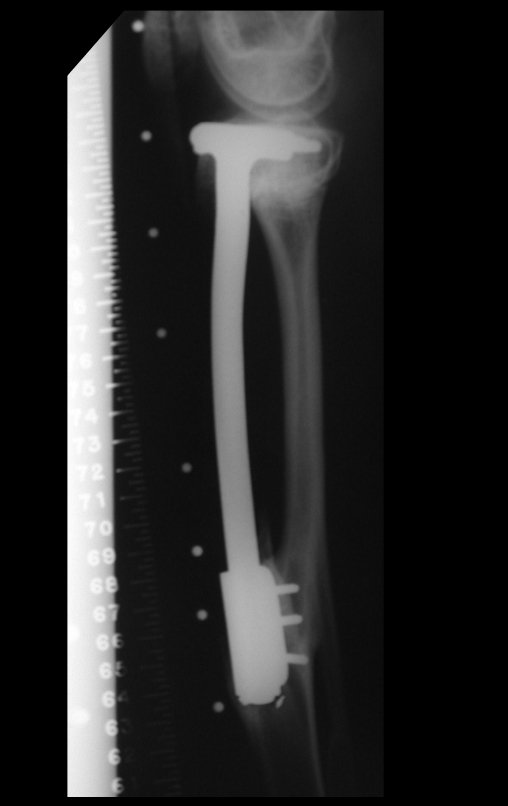
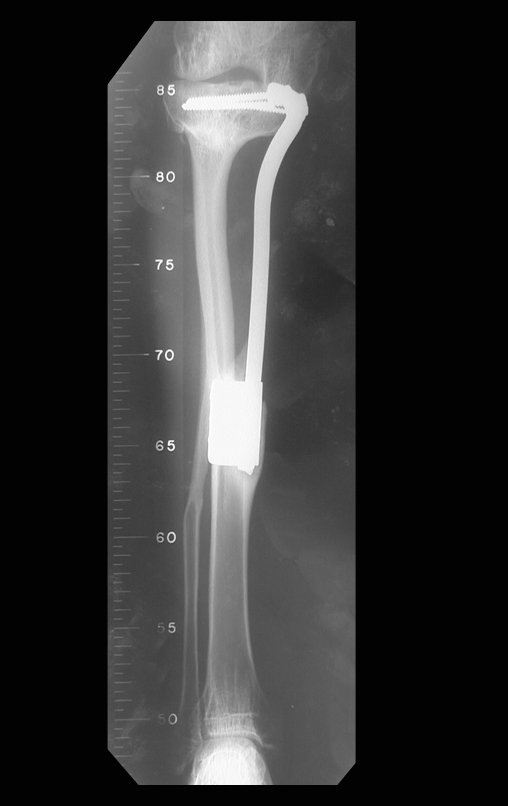
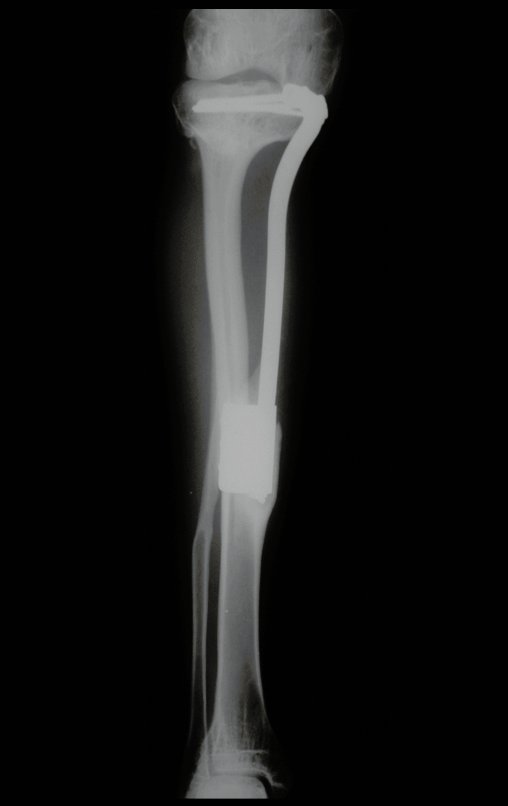
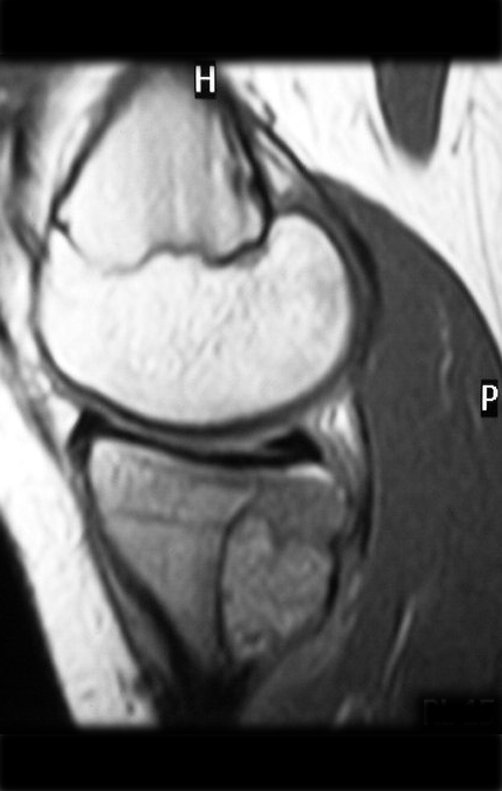
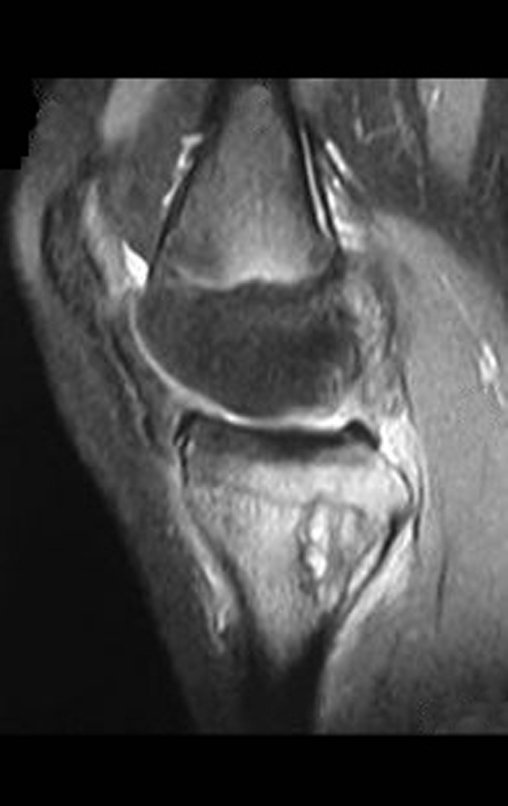
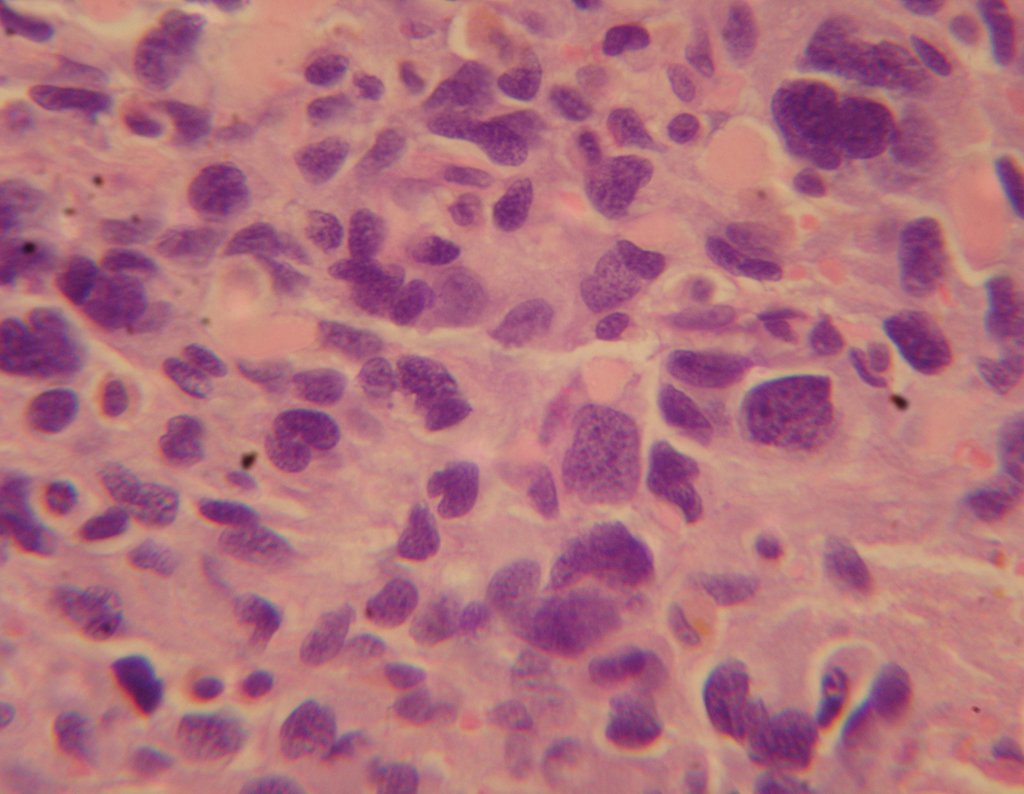
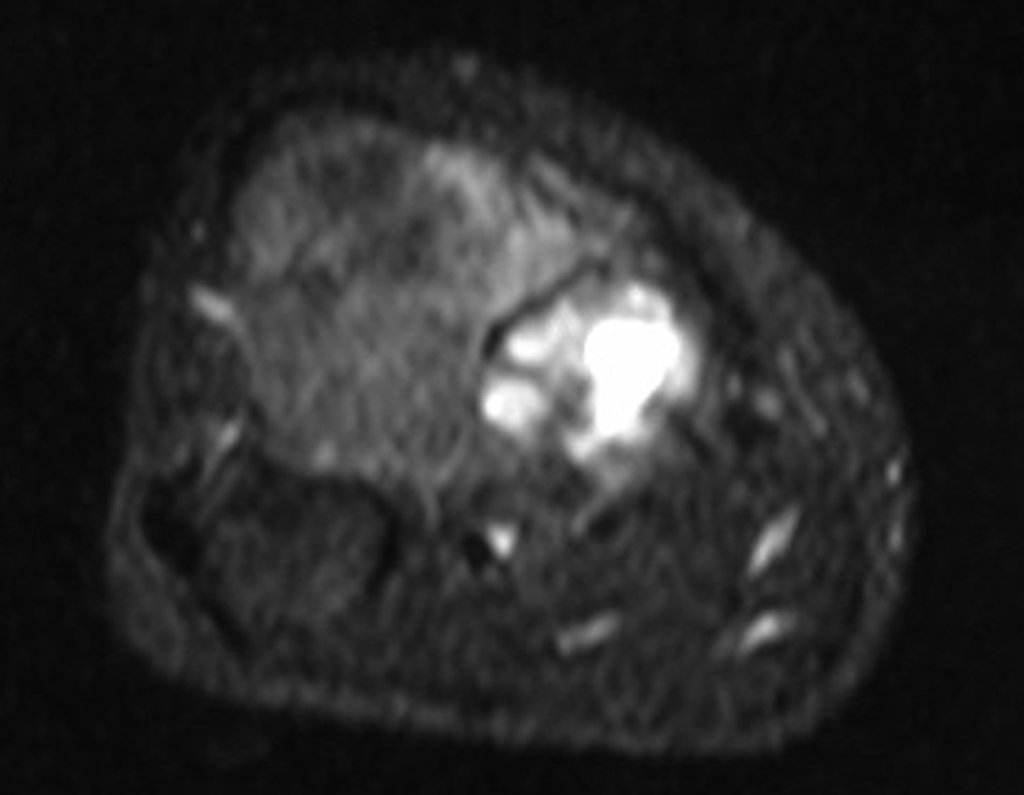
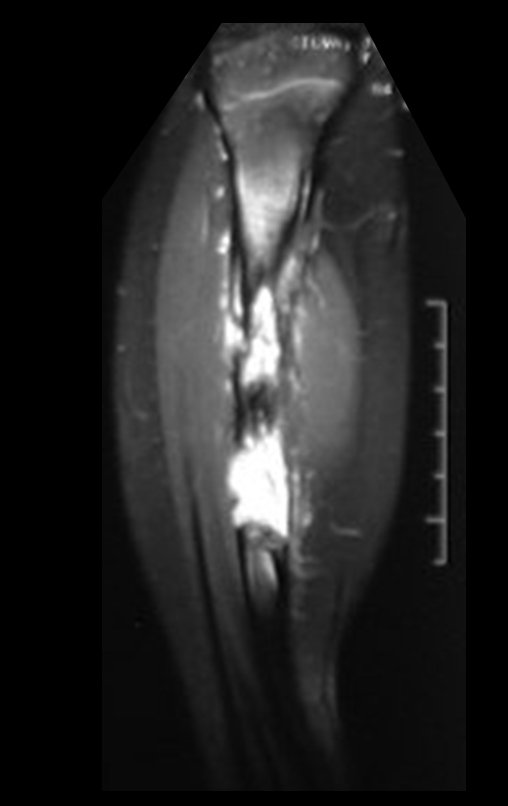
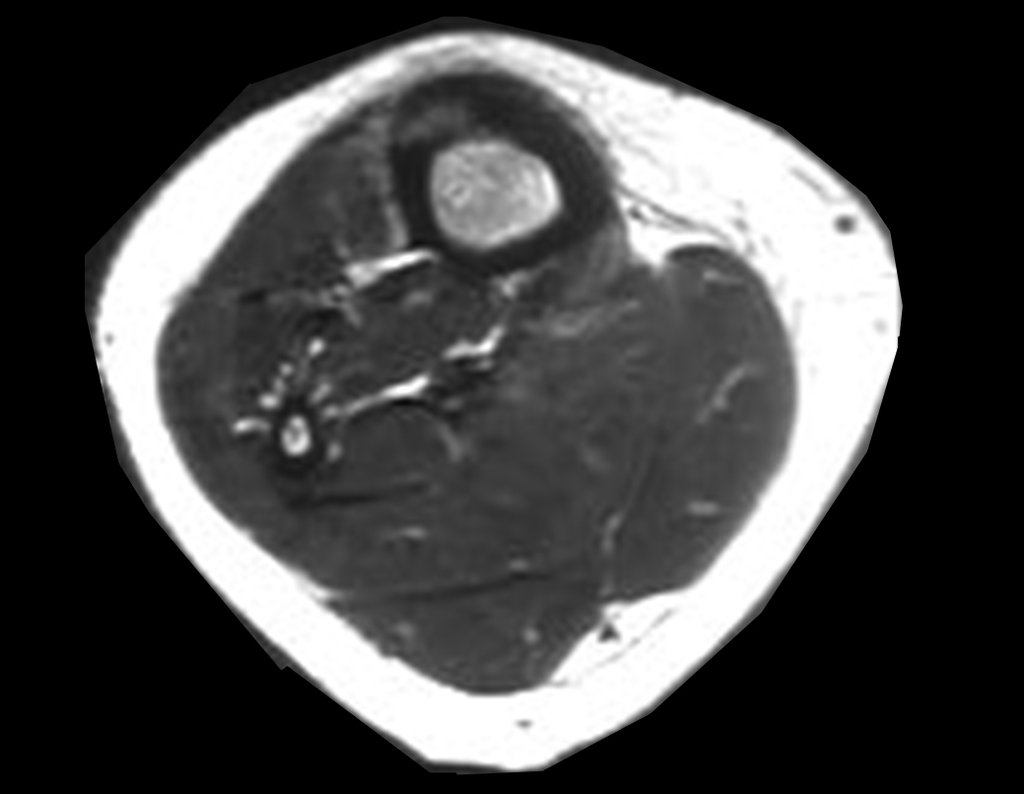
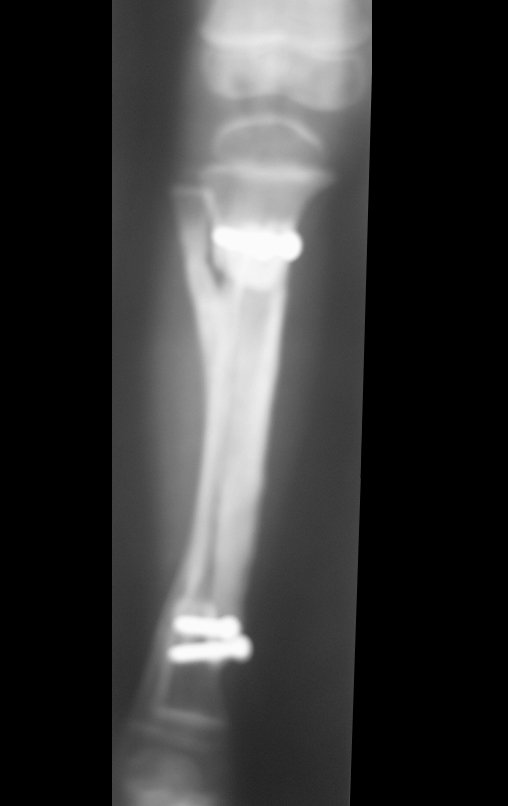
El estudio de las imágenes y el análisis del examen clínico mostraron la afectación del músculo deltoides, pero con la factibilidad de una cirugía conservadora, con margen, siempre y cuando se reseque completamente el músculo involucrado y se reemplace completamente el húmero con un polietileno modular. endoprótesis.
A pesar de la necesidad de sacrificio funcional parcial del hombro, y de la necesidad de reconstrucción artroplástica, con malla Marlex para cobertura proximal de la prótesis y estabilidad del hombro, la preservación del miembro superior fue nuestra indicación, con el objetivo de ofrecer un resto estético y funcional. aspecto del hombro.
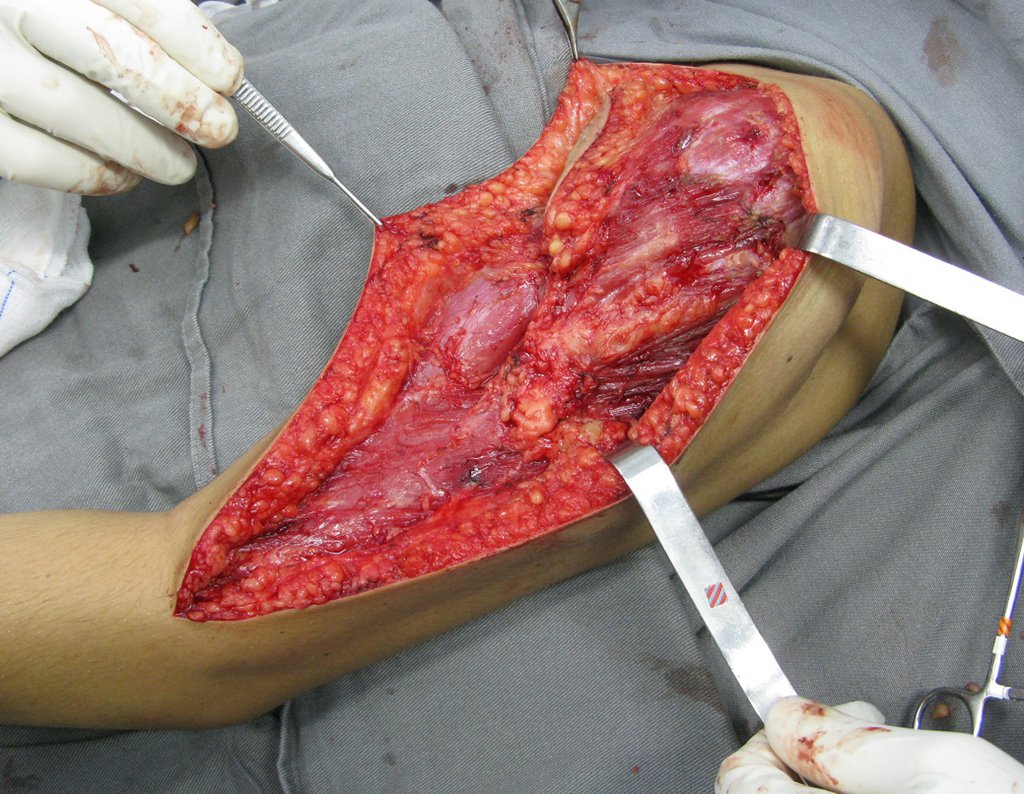
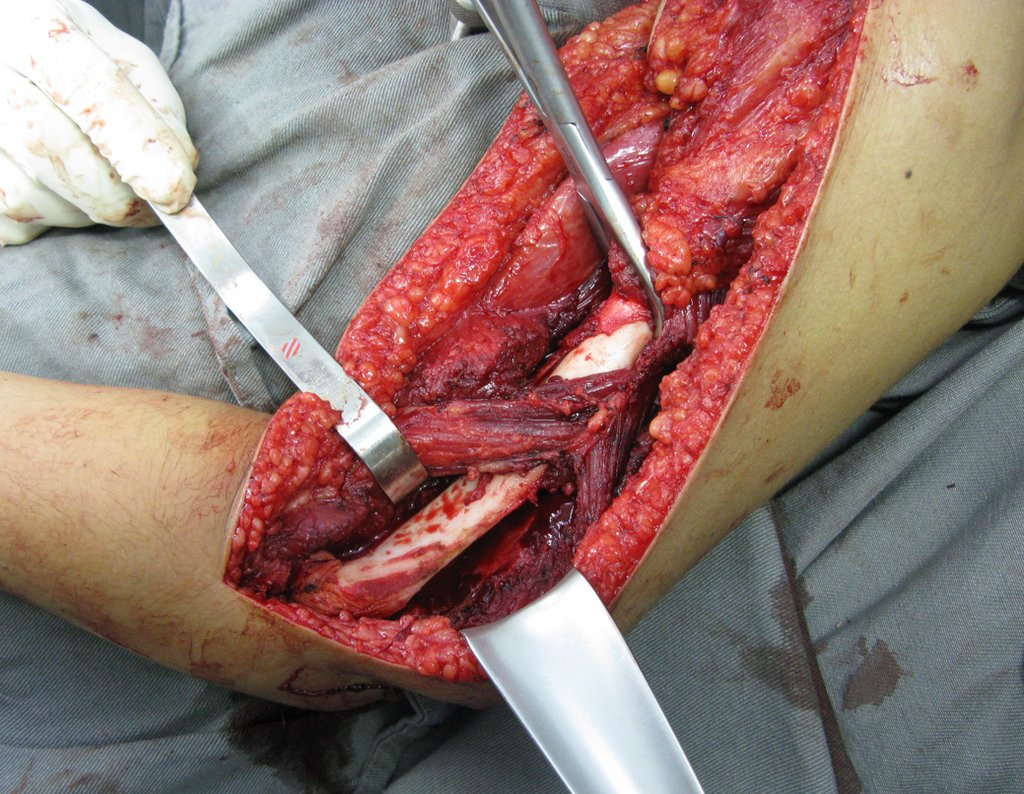
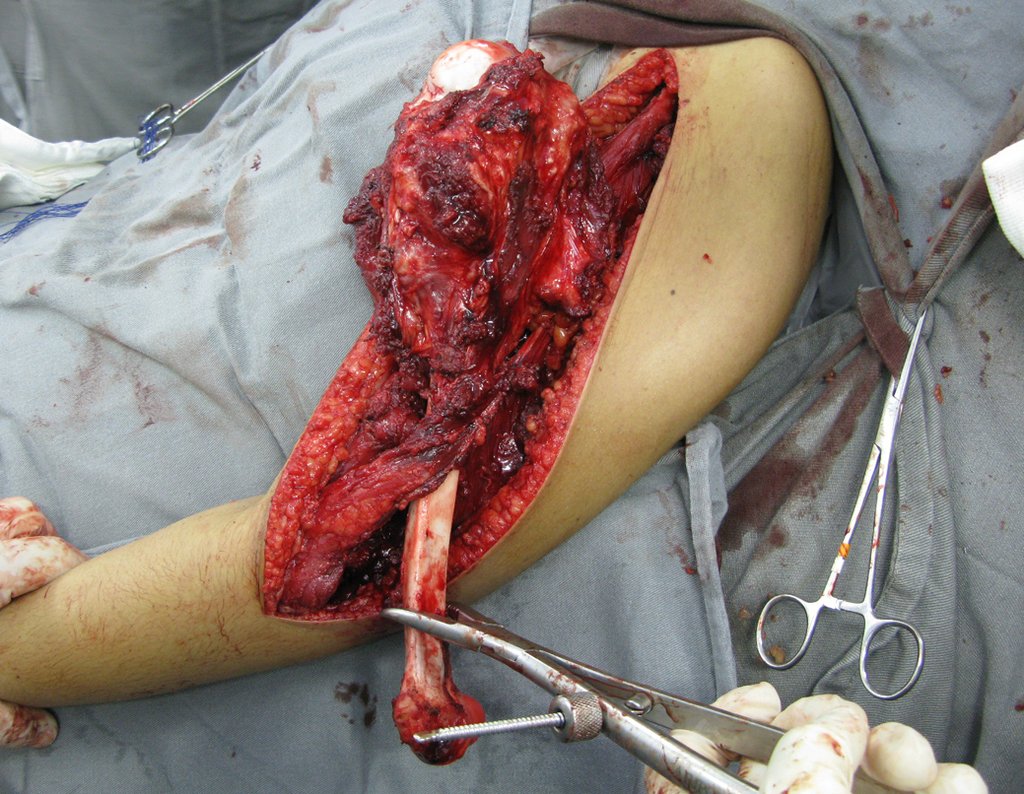
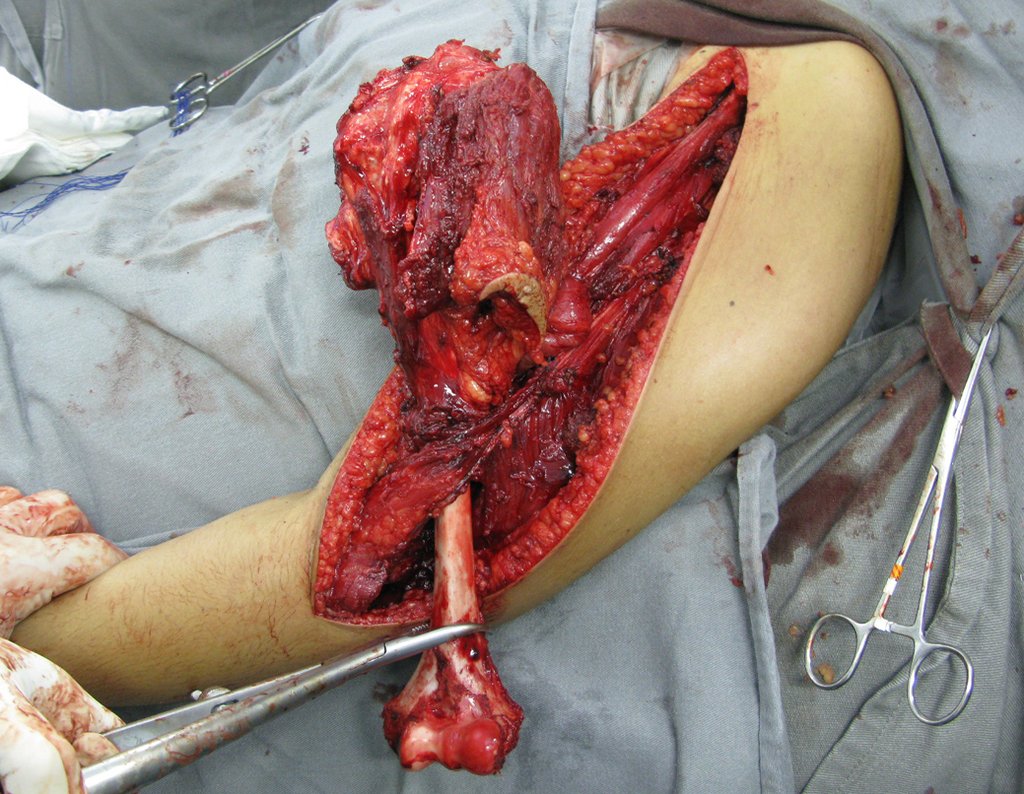
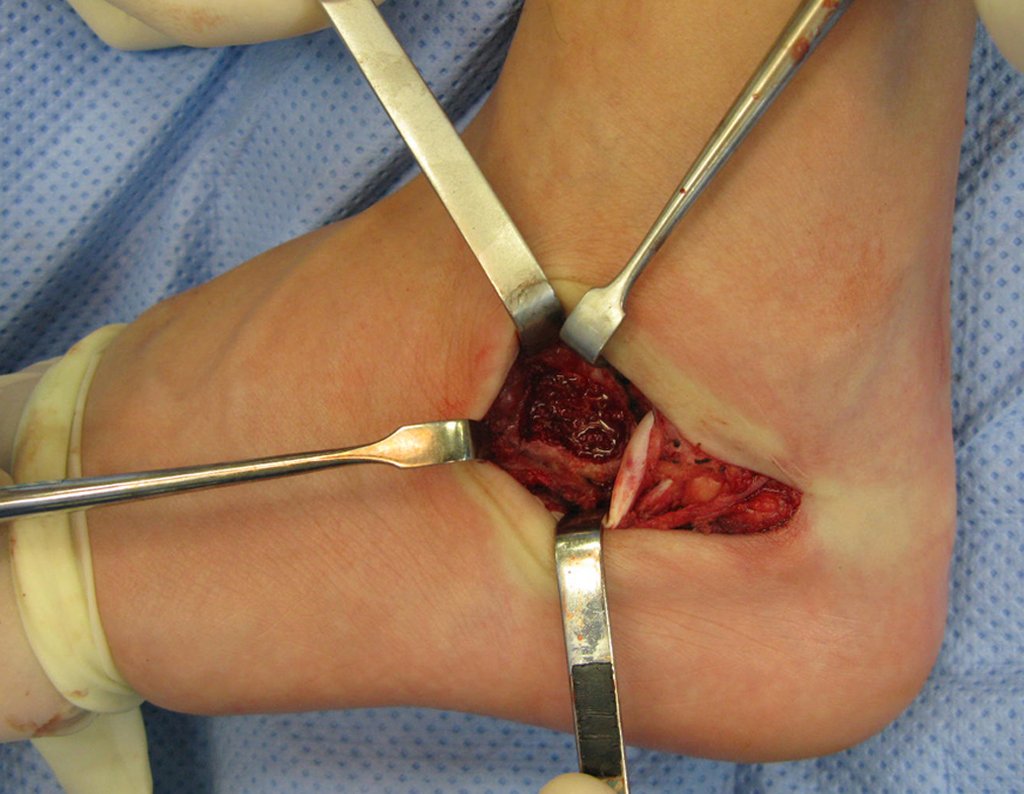
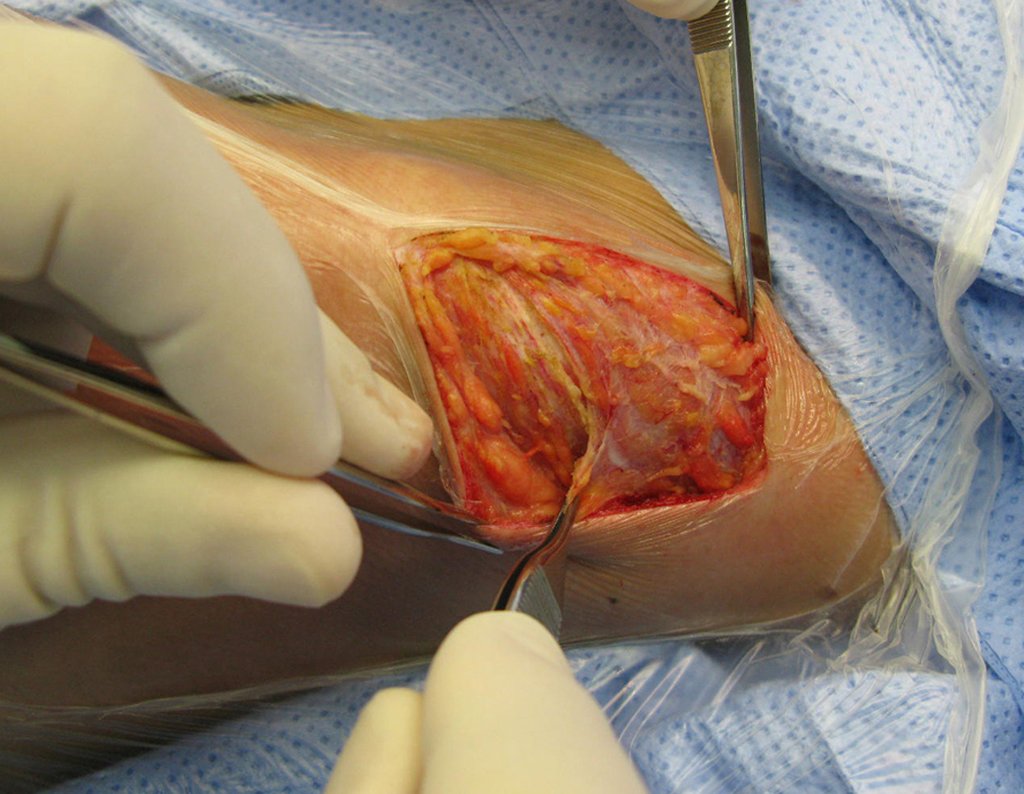
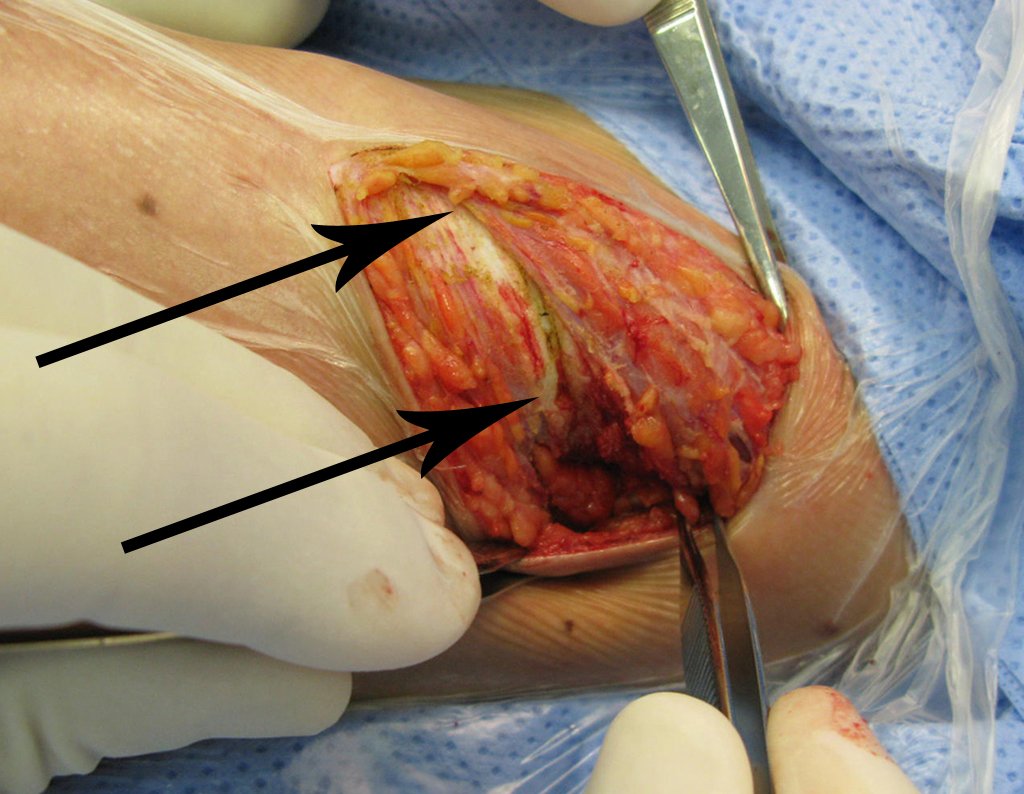
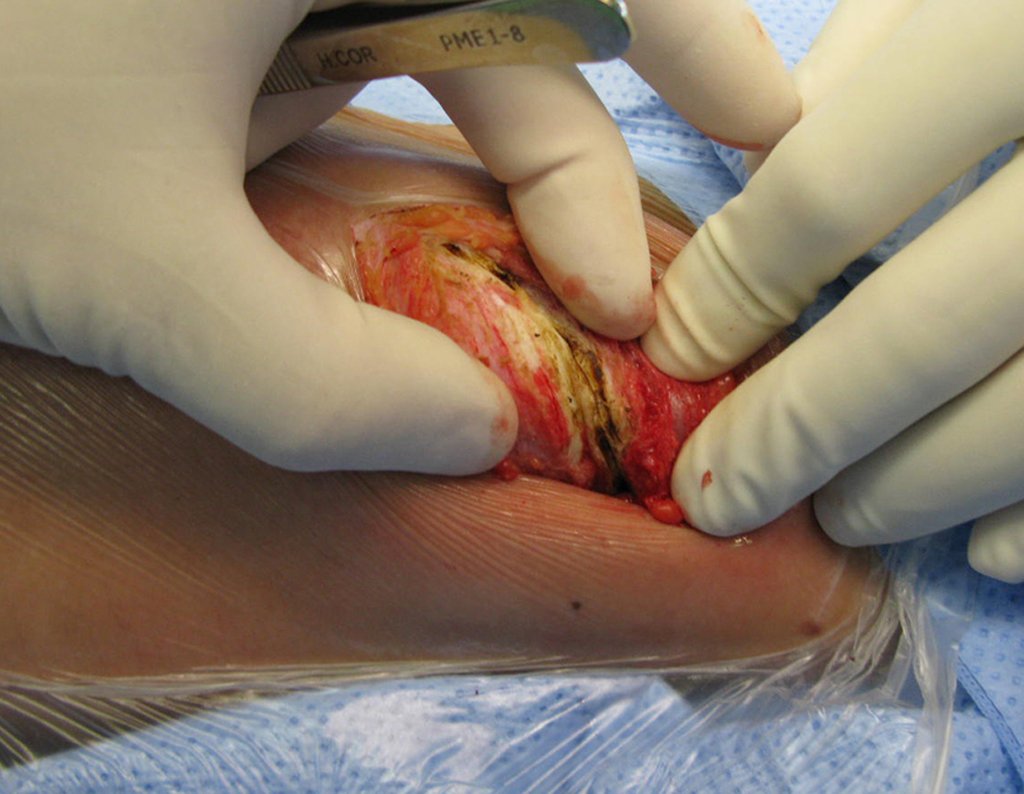
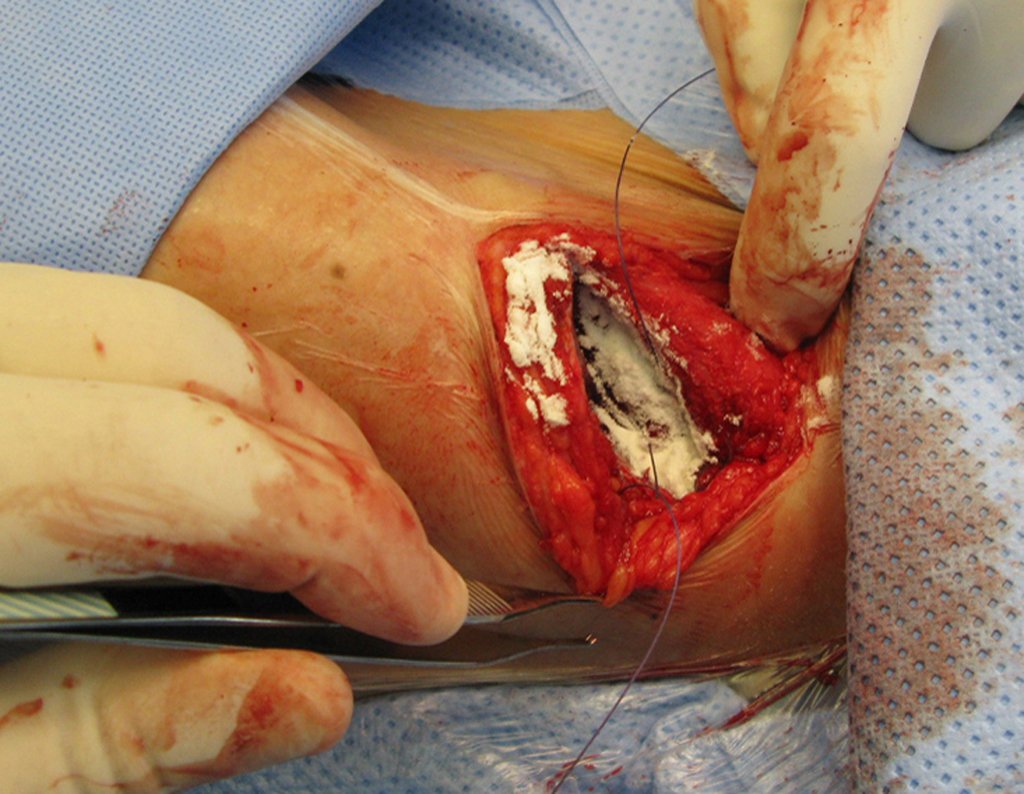
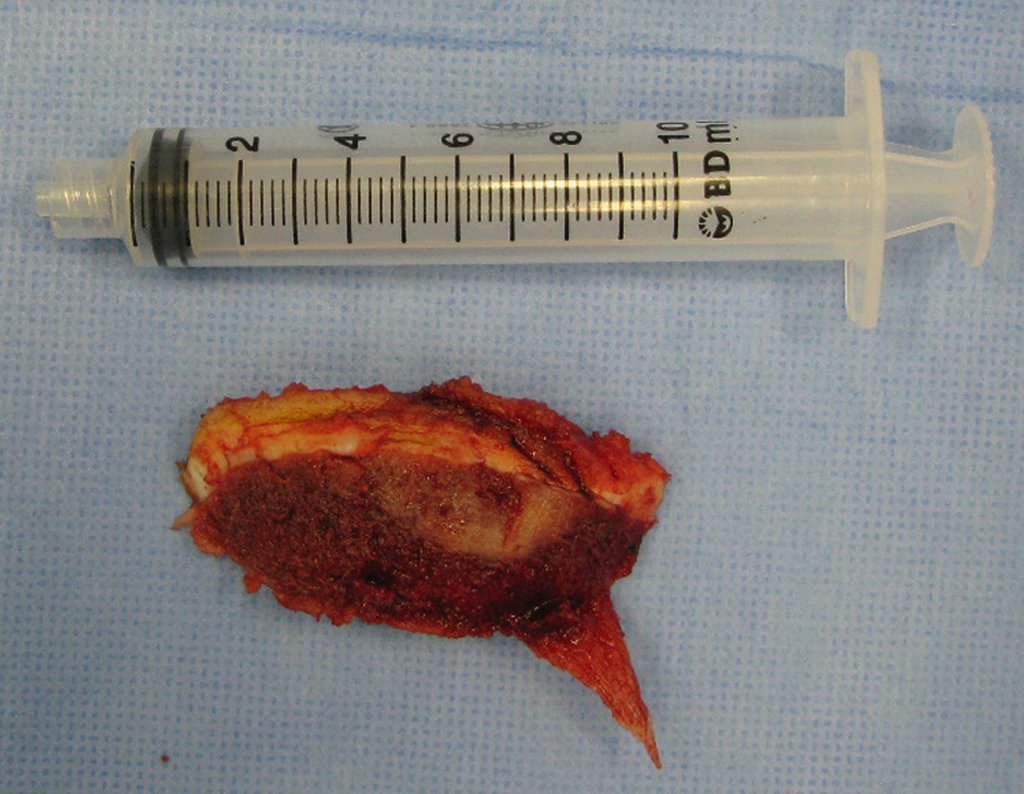
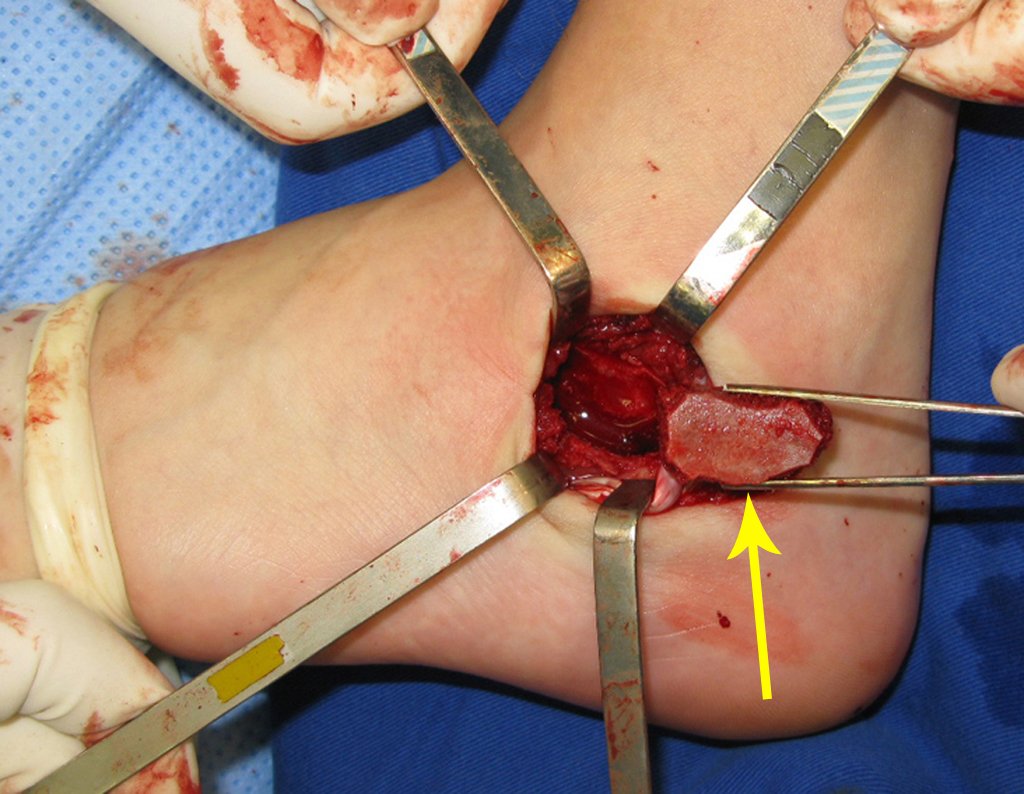
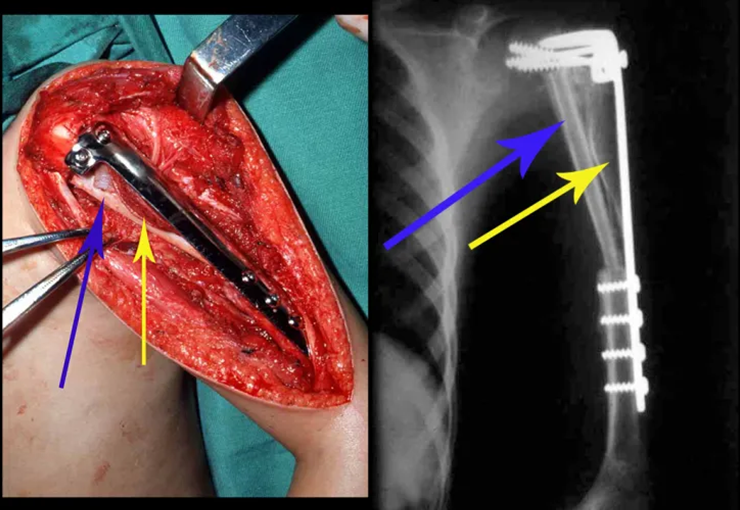
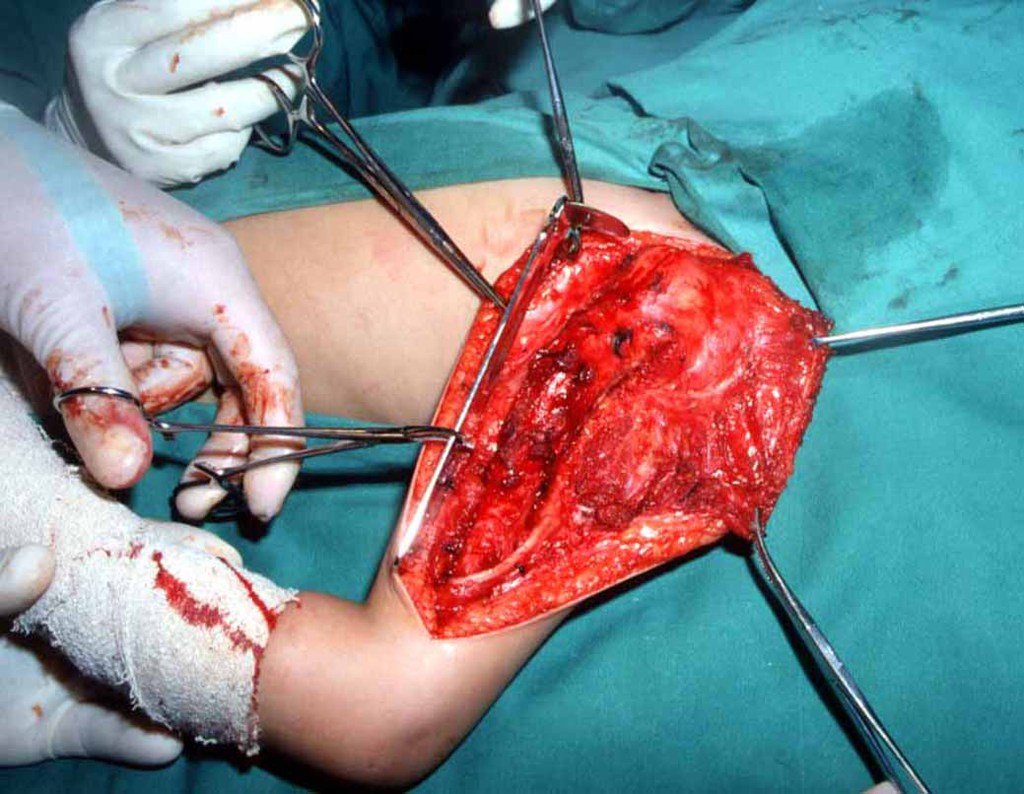
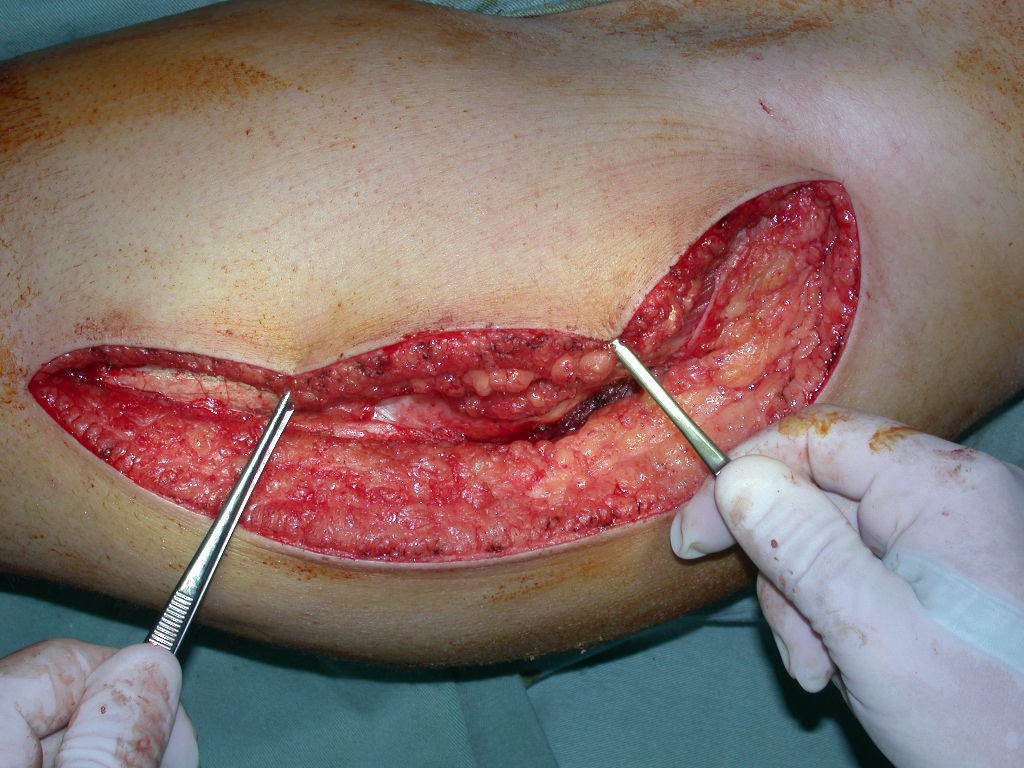
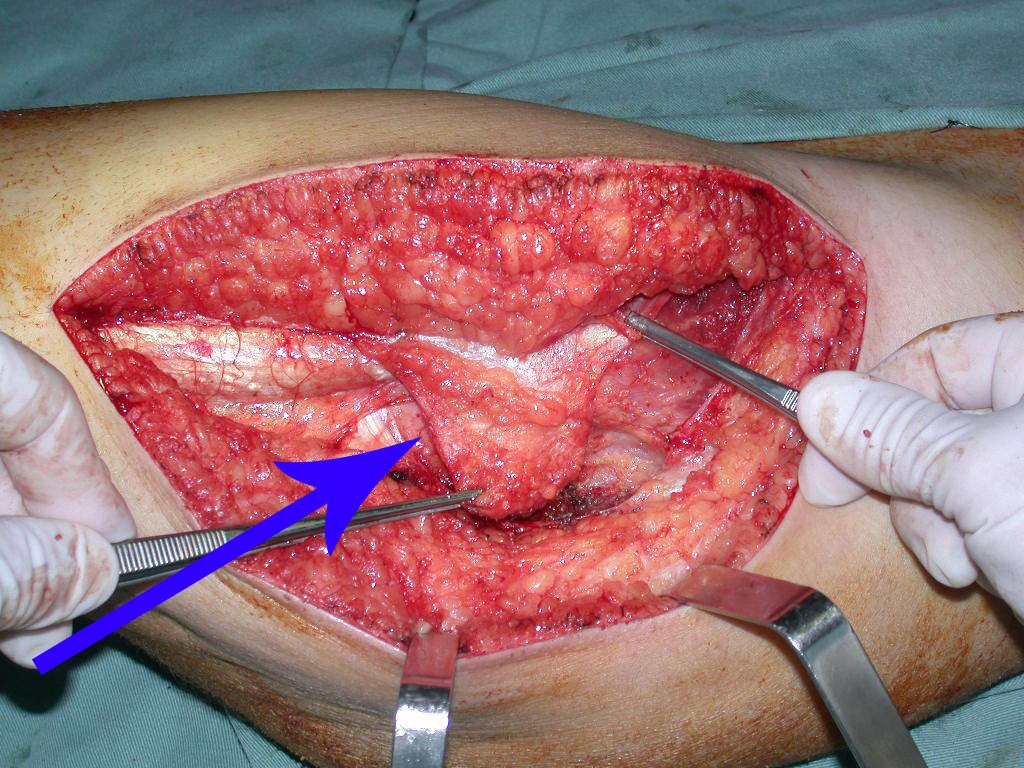
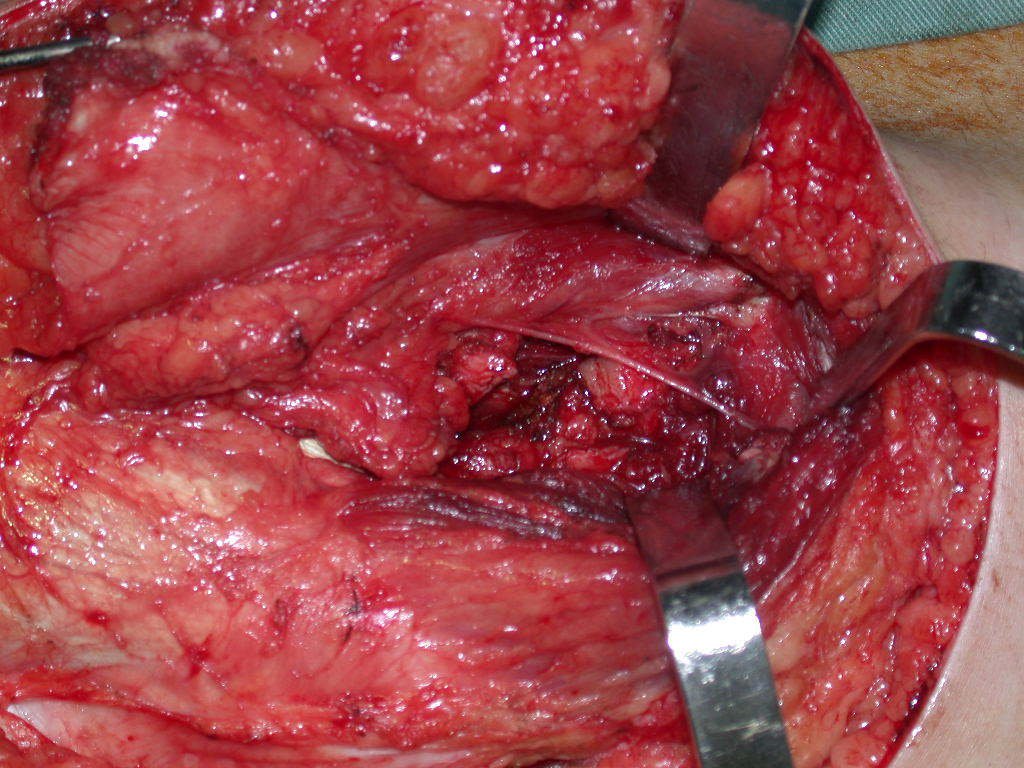
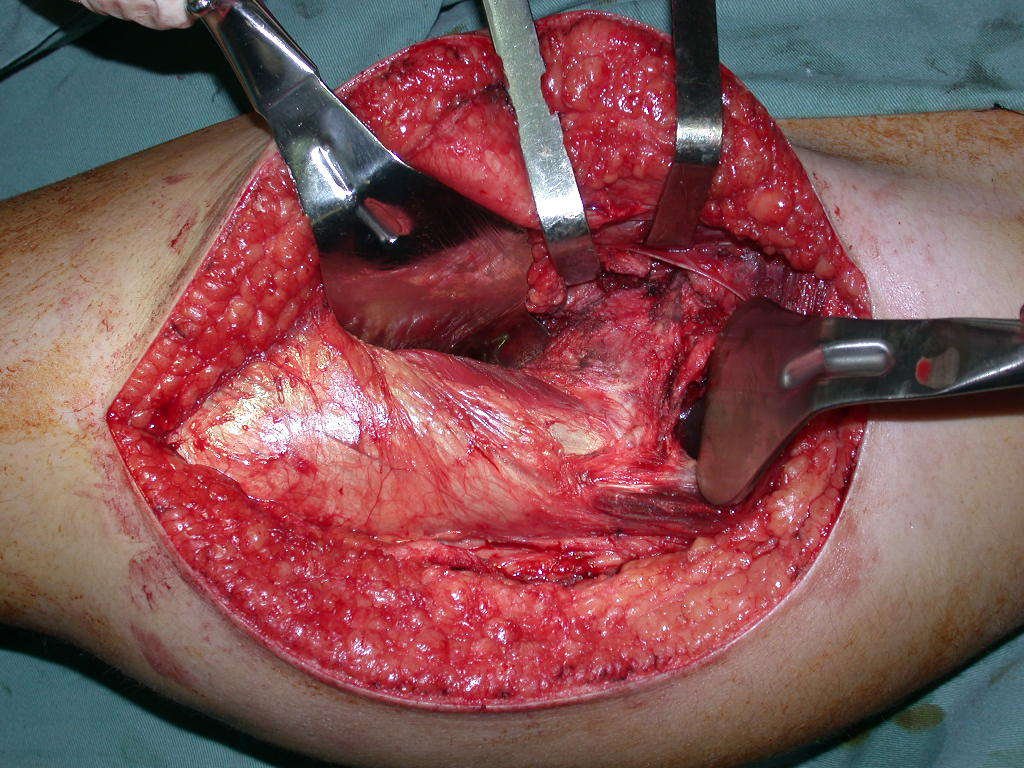
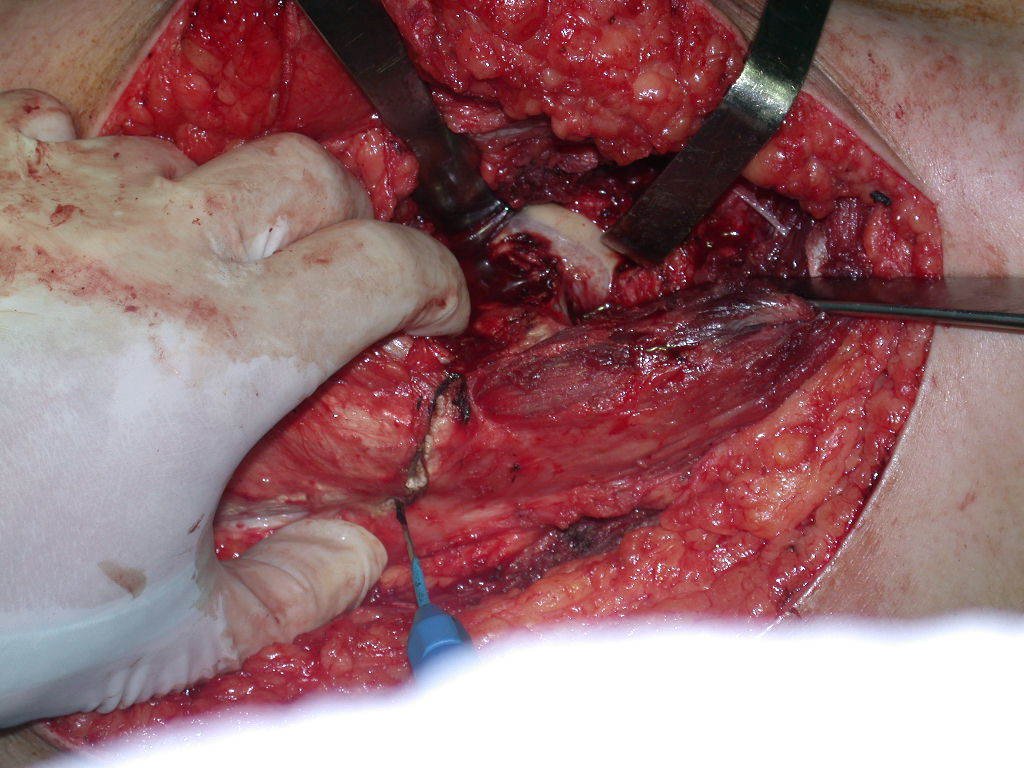
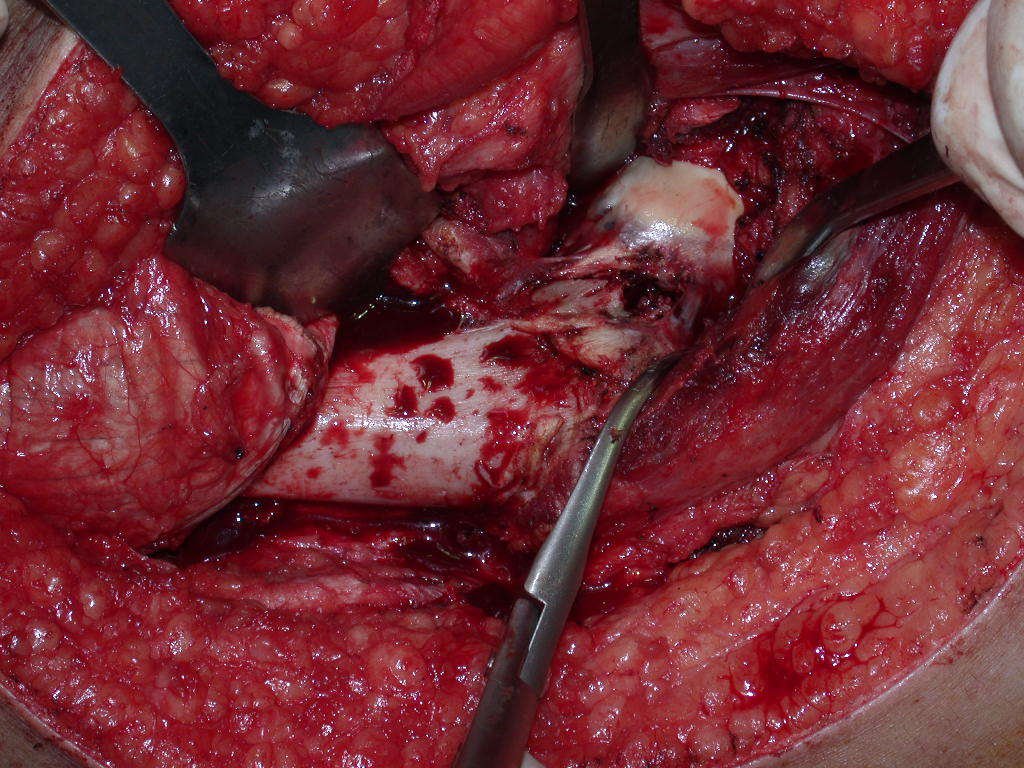
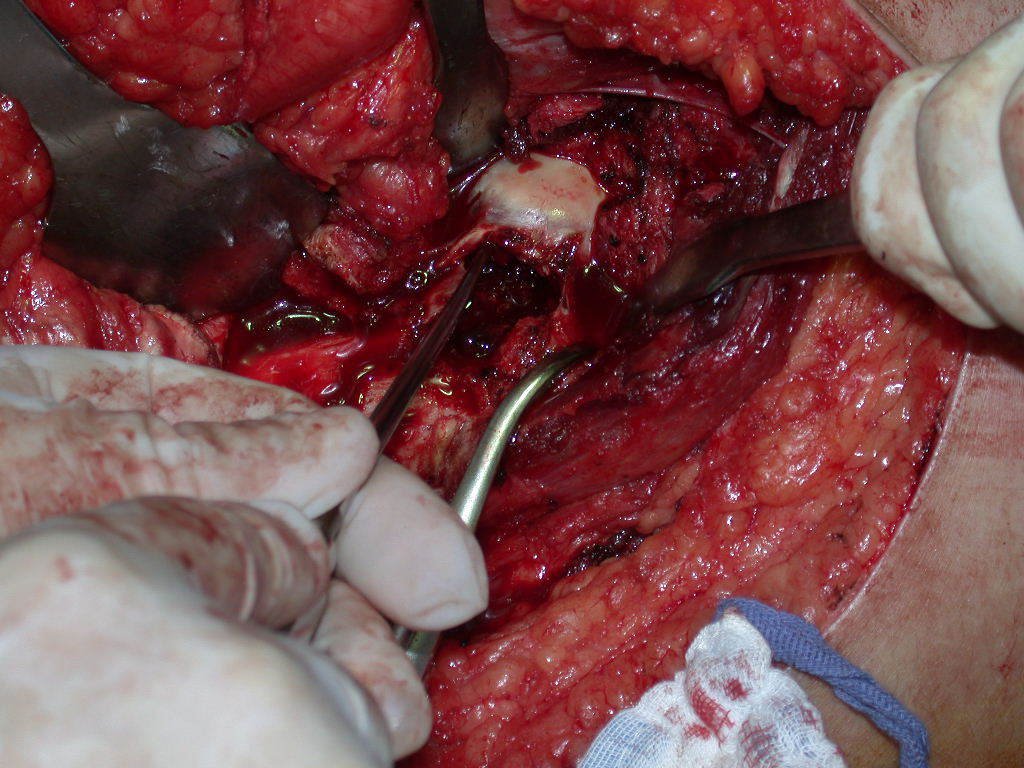
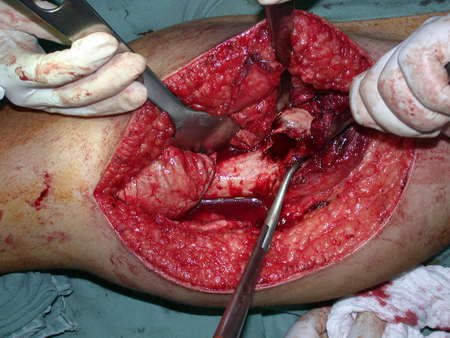
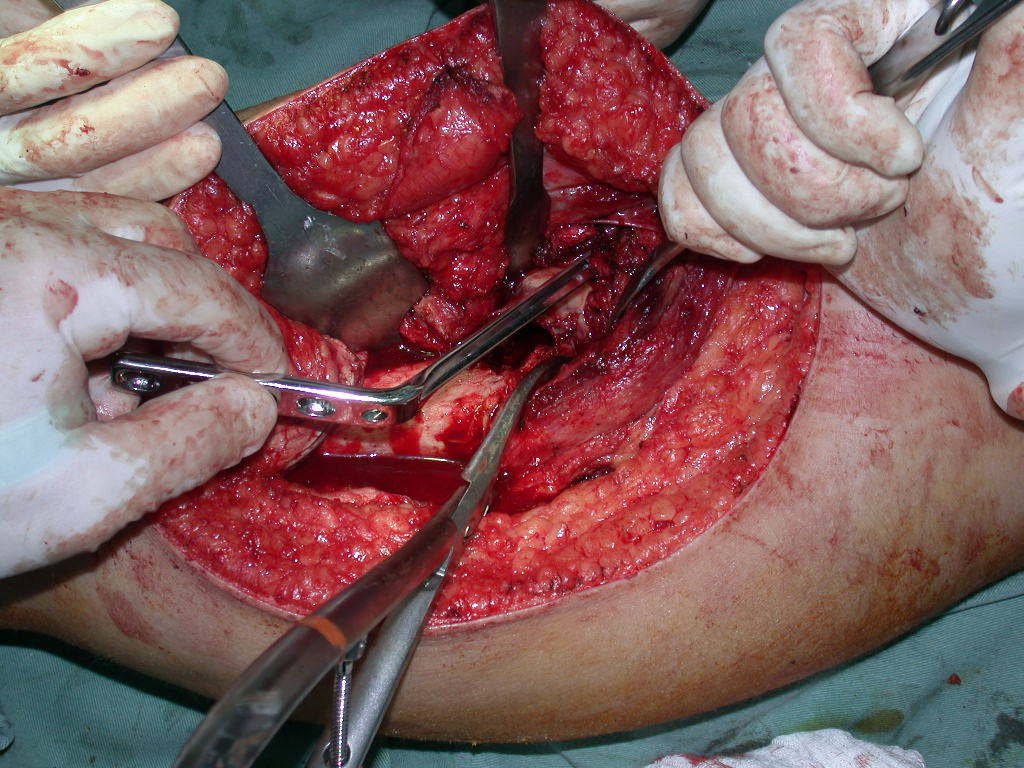
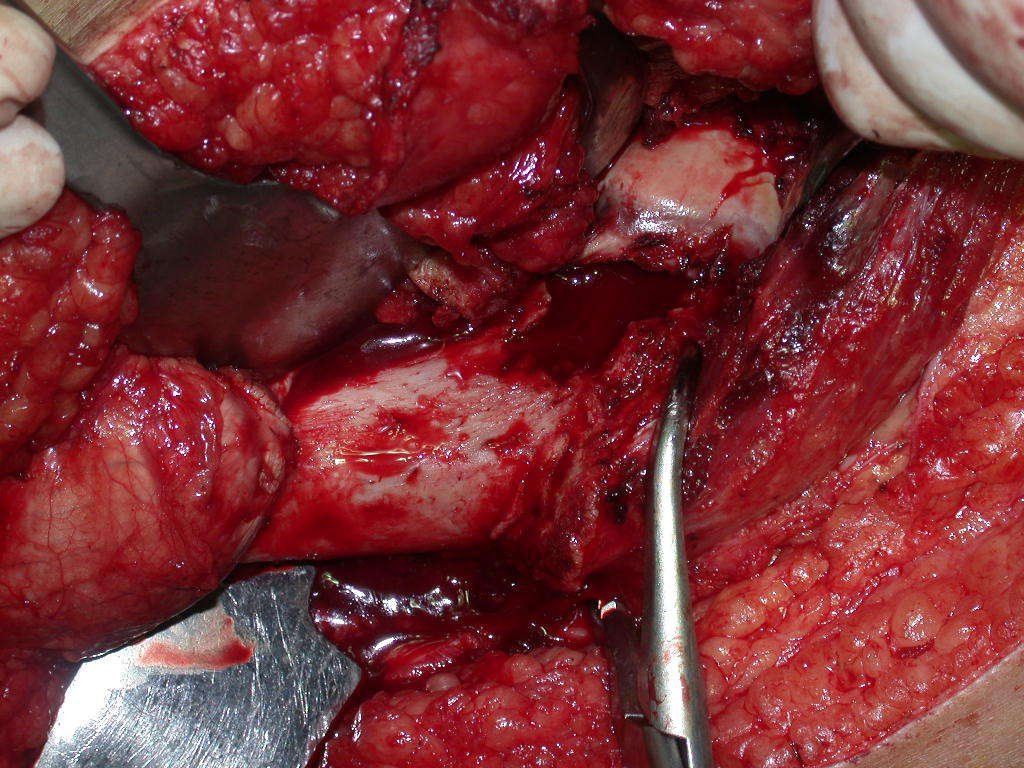
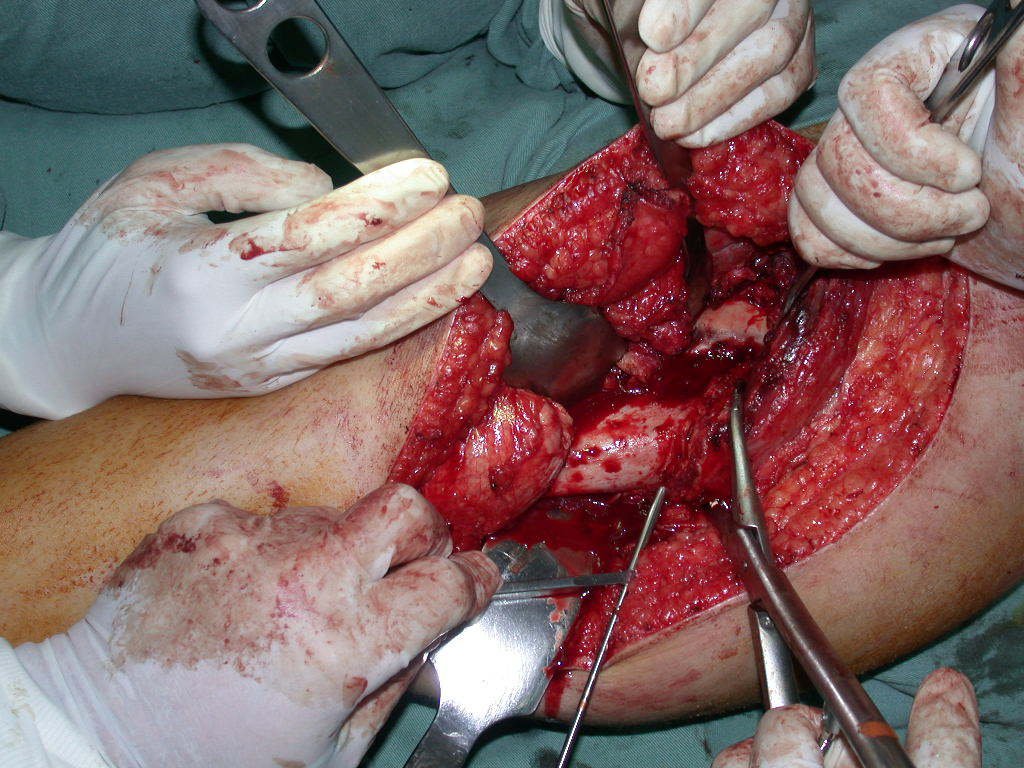
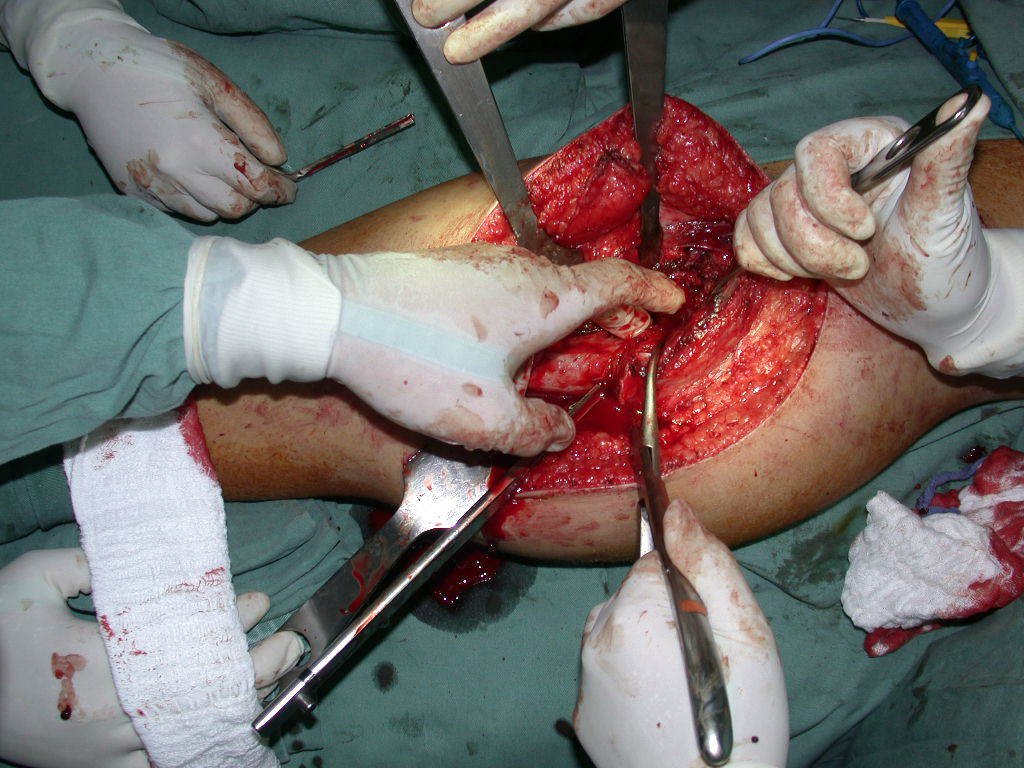
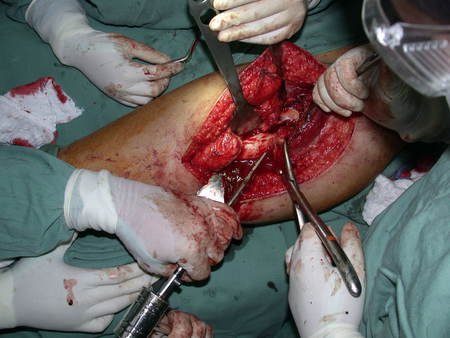
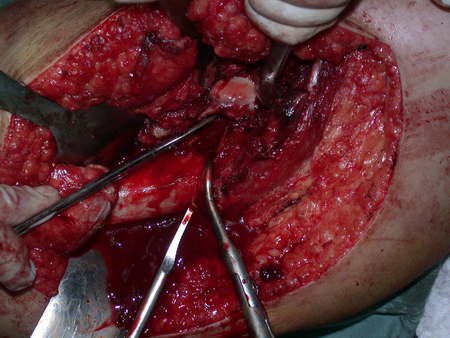
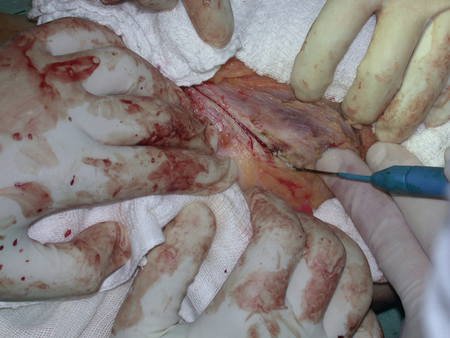
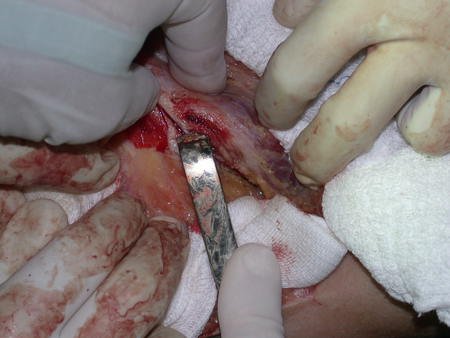
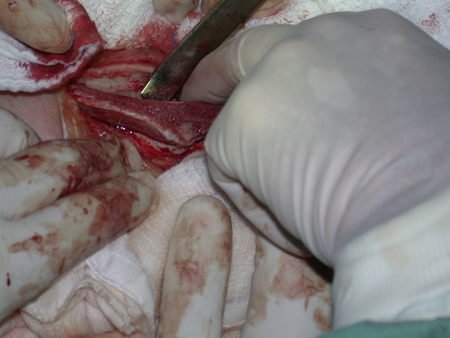
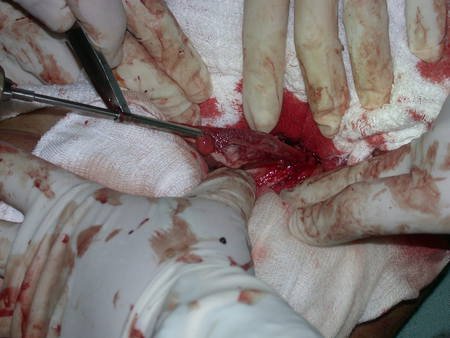
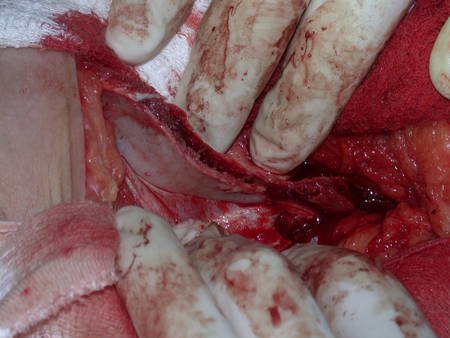
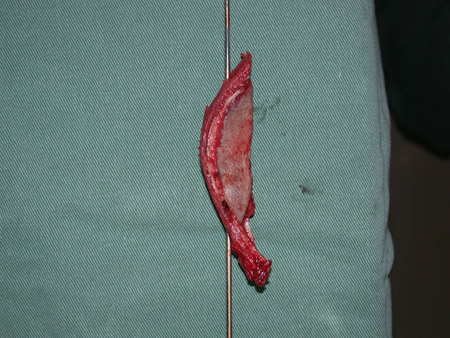
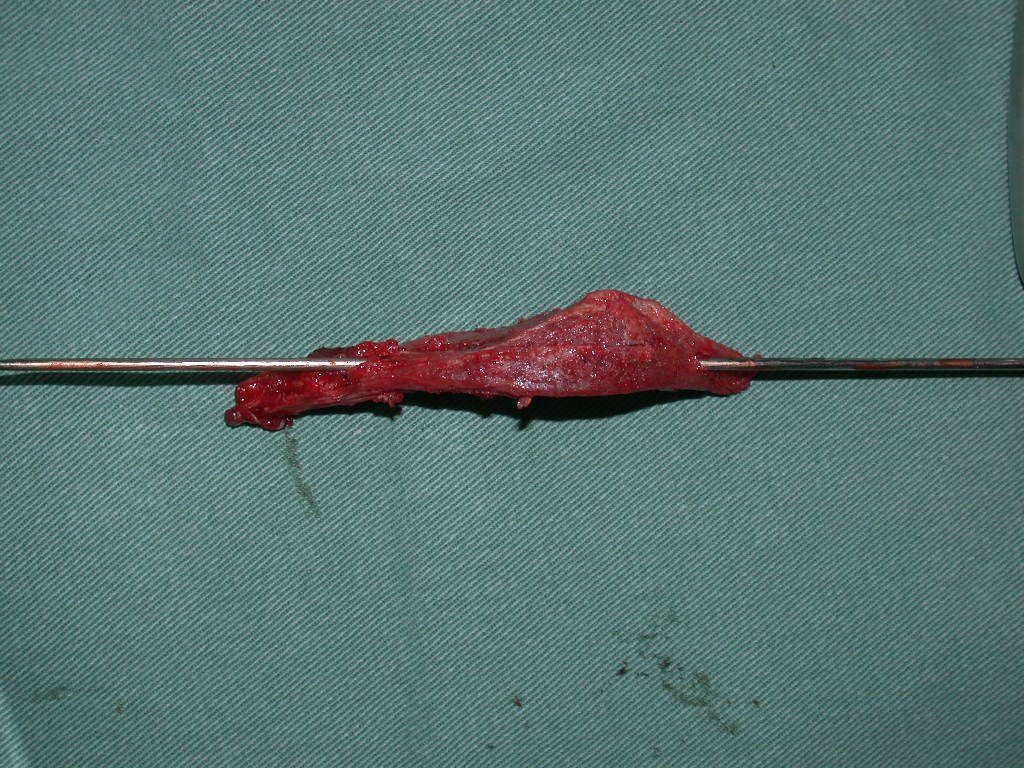
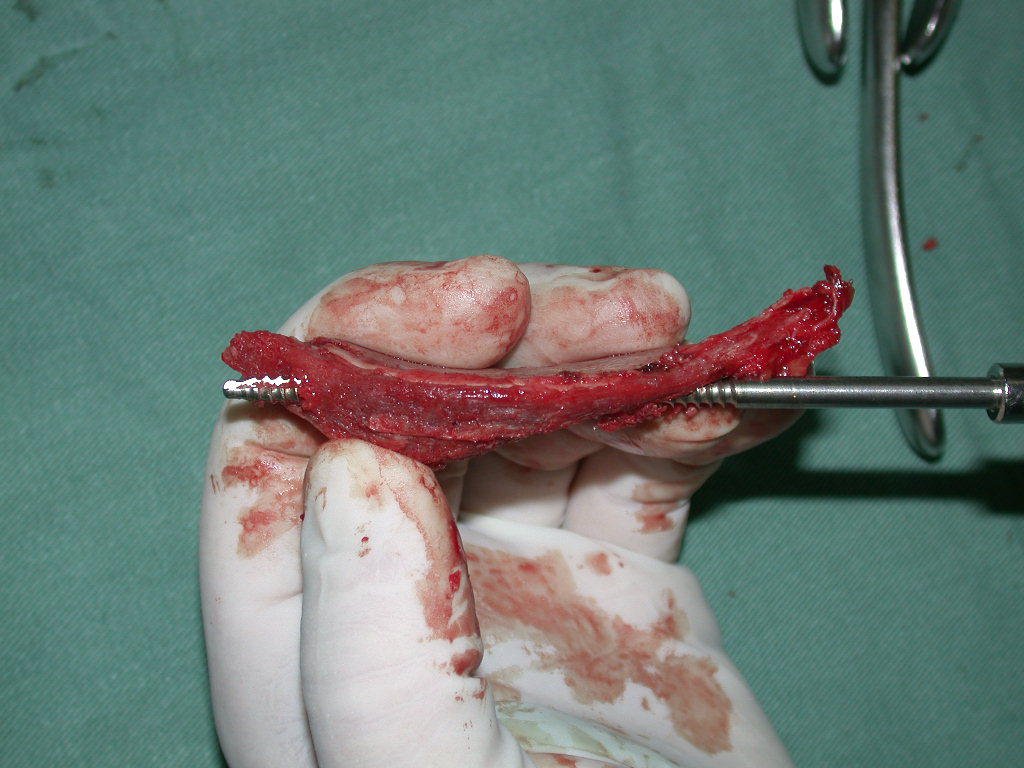
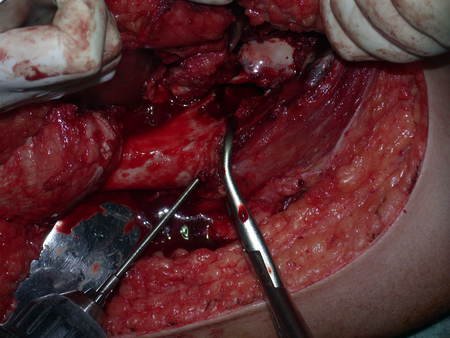
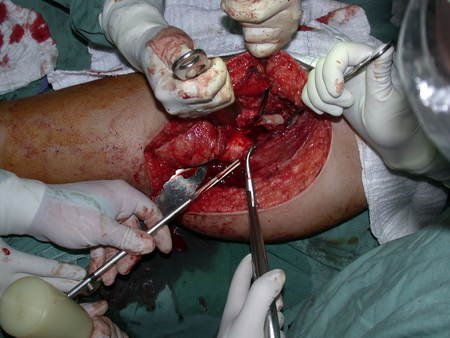
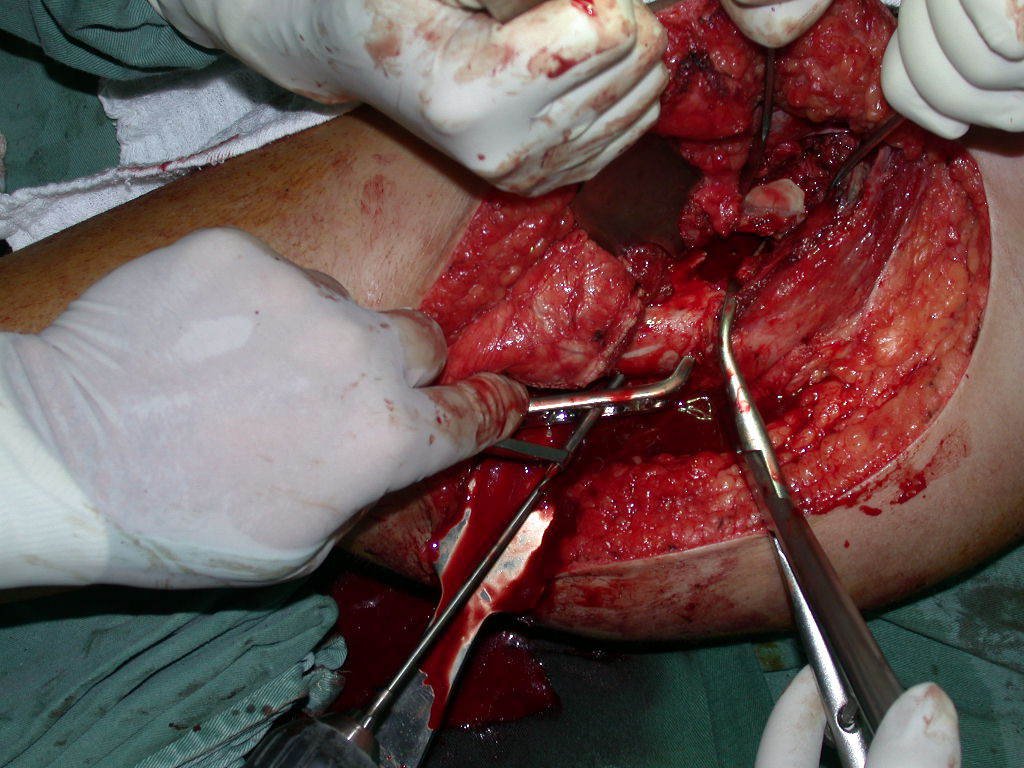
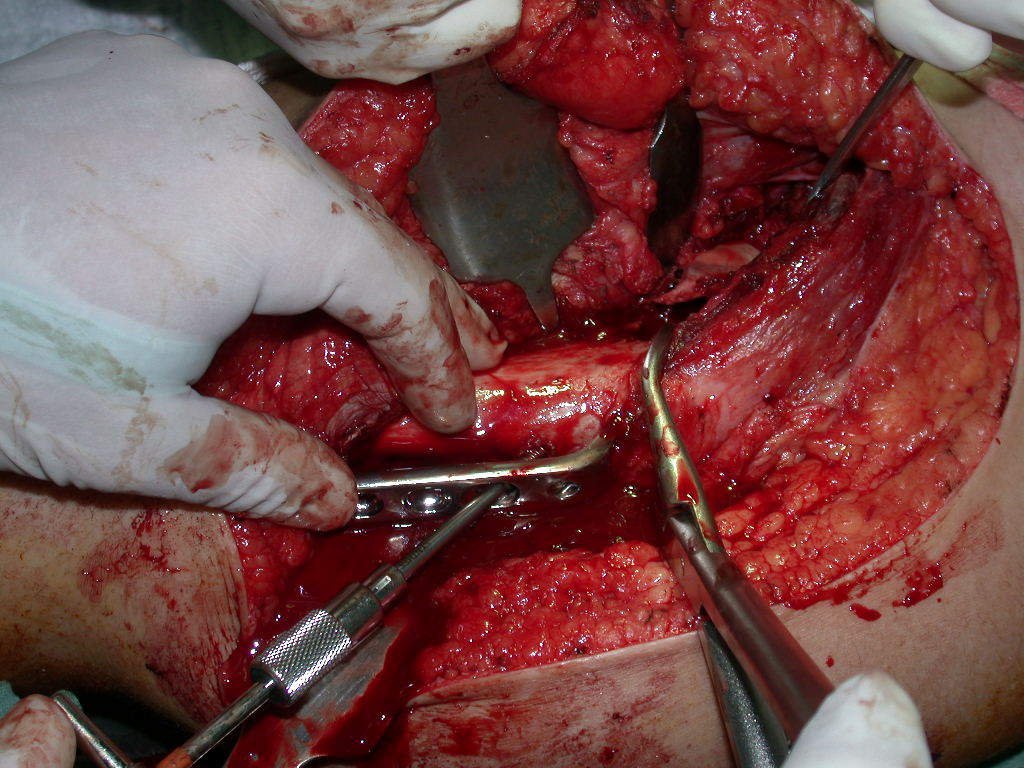
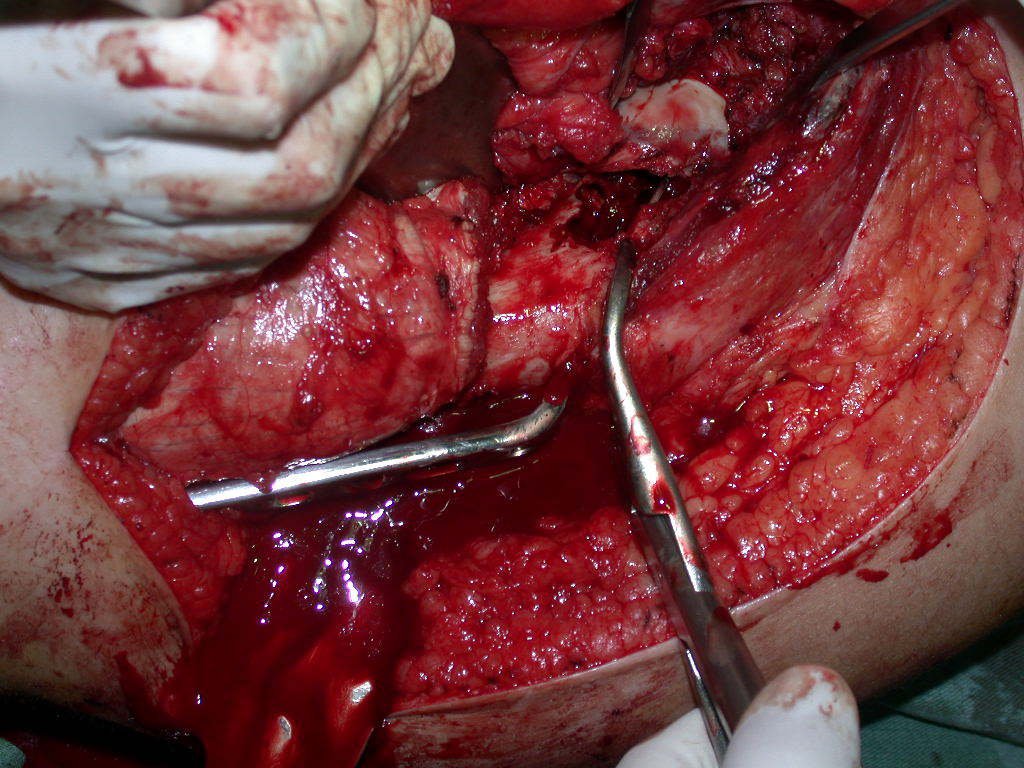
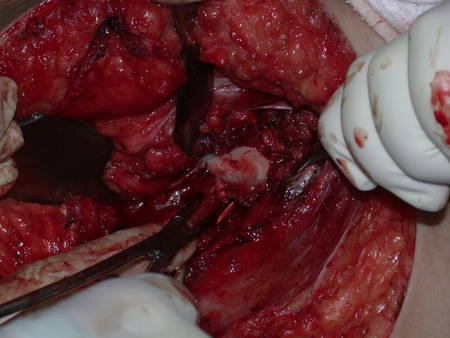
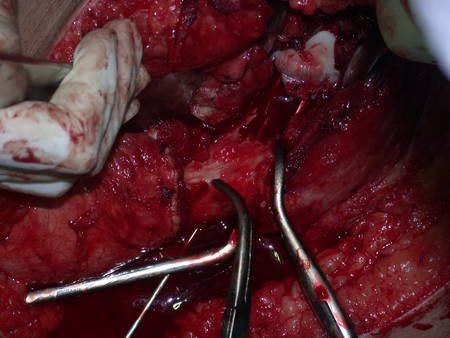
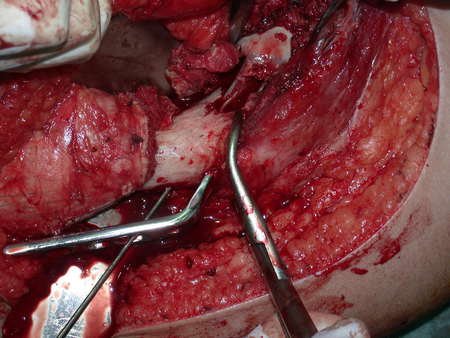
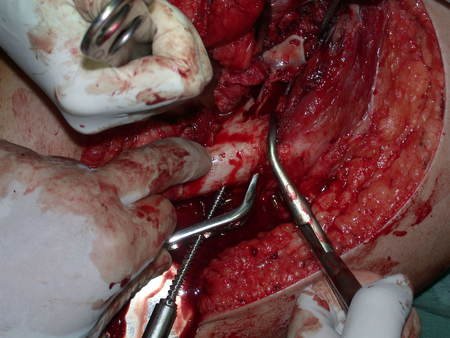
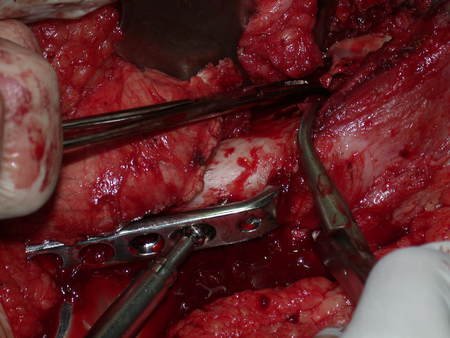
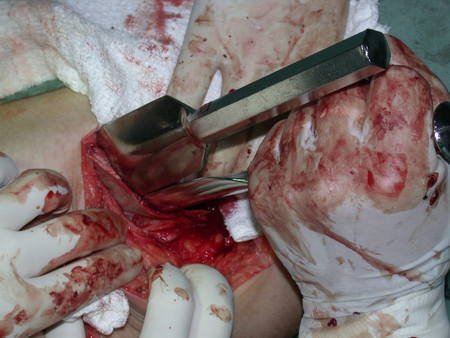
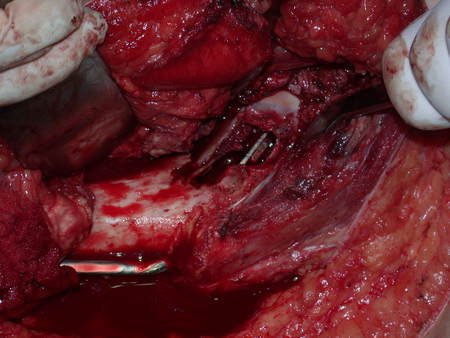
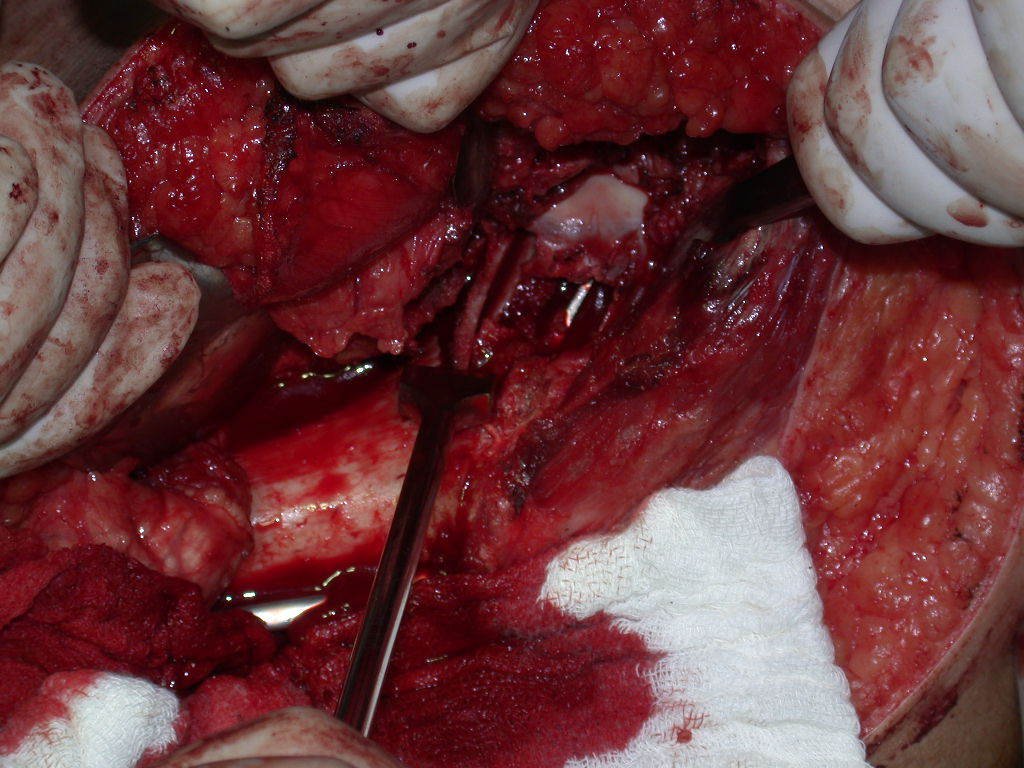
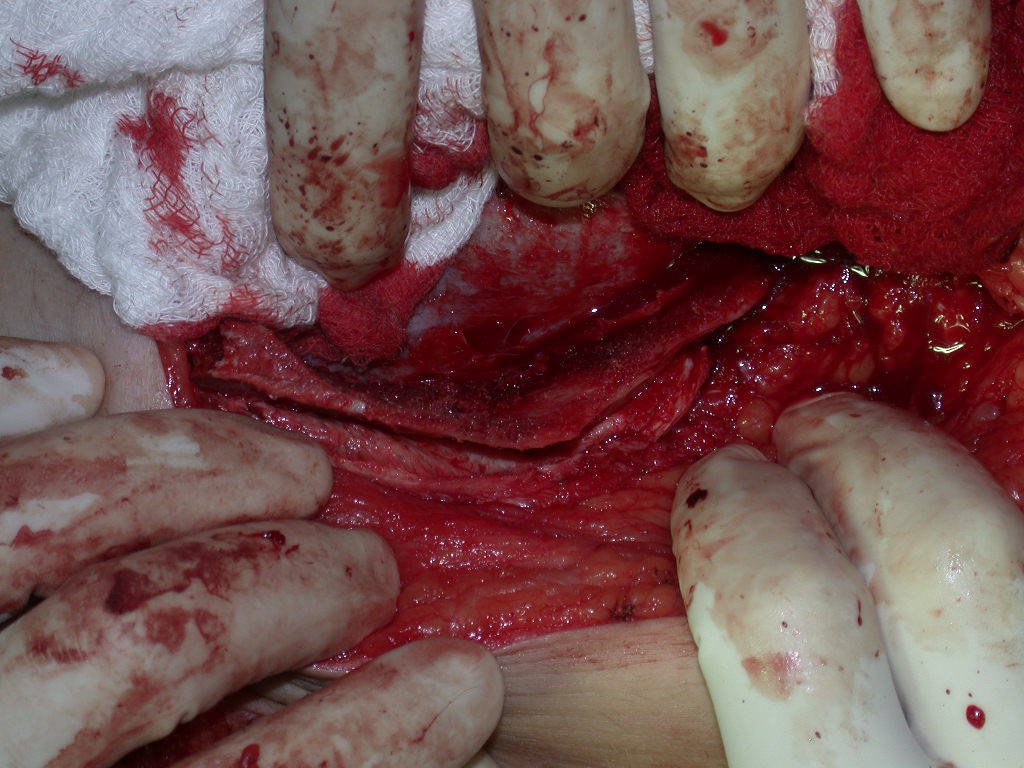
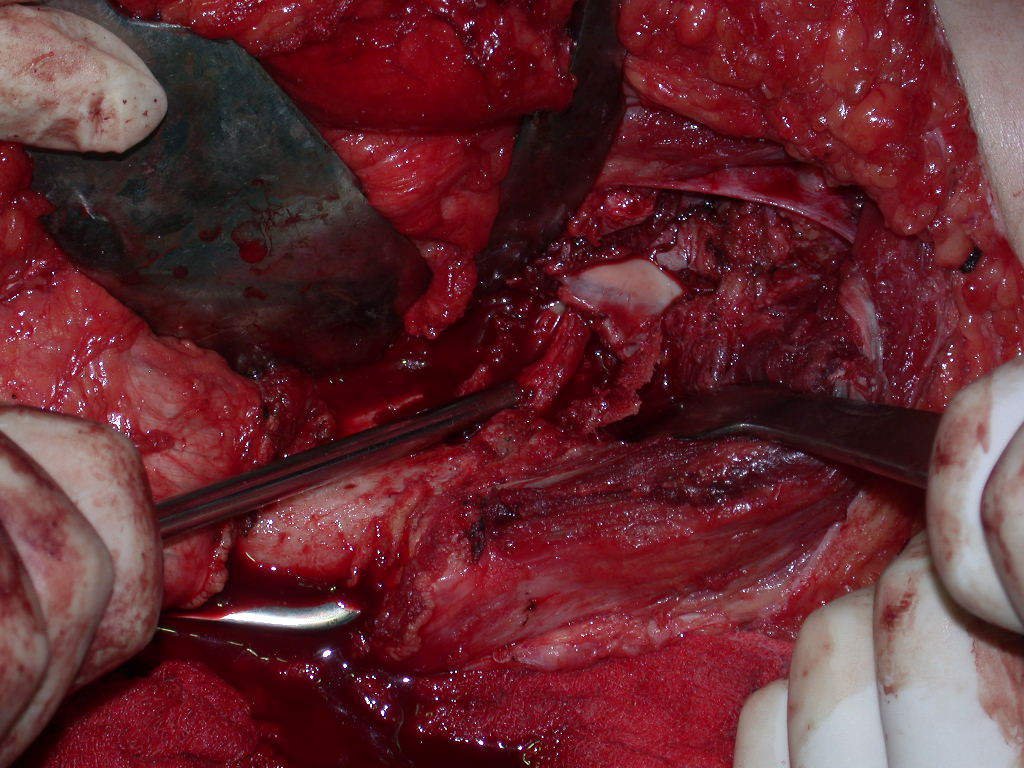
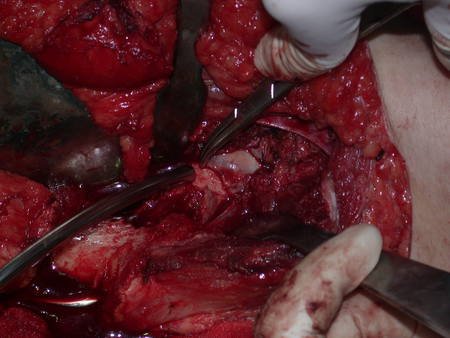
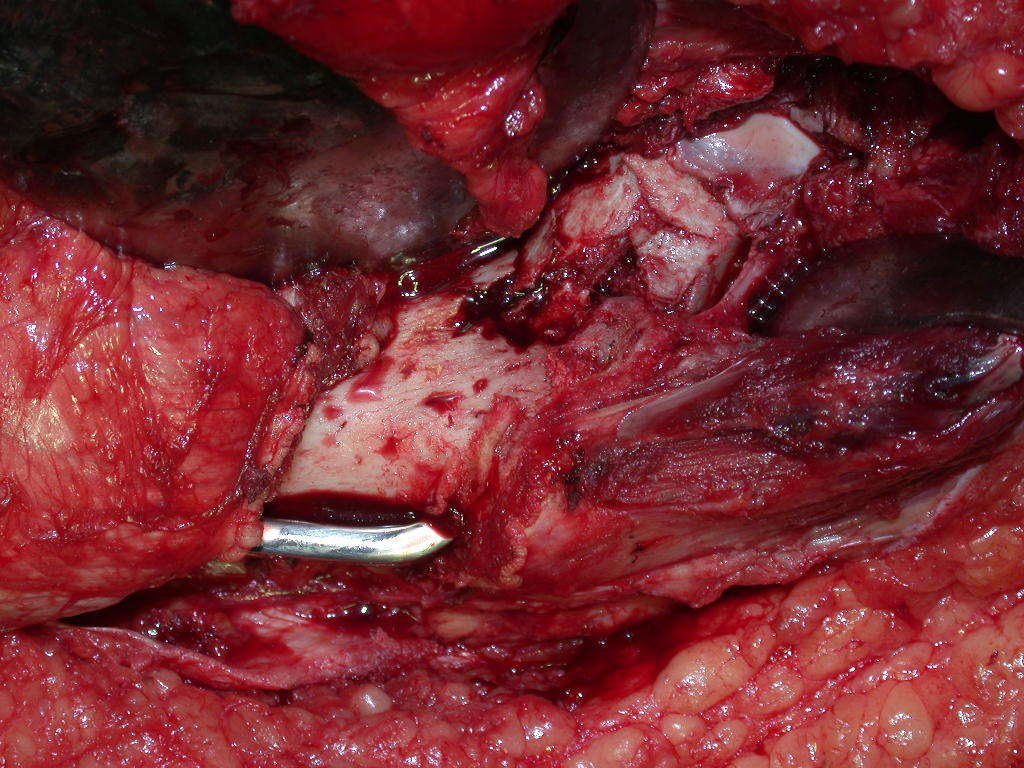
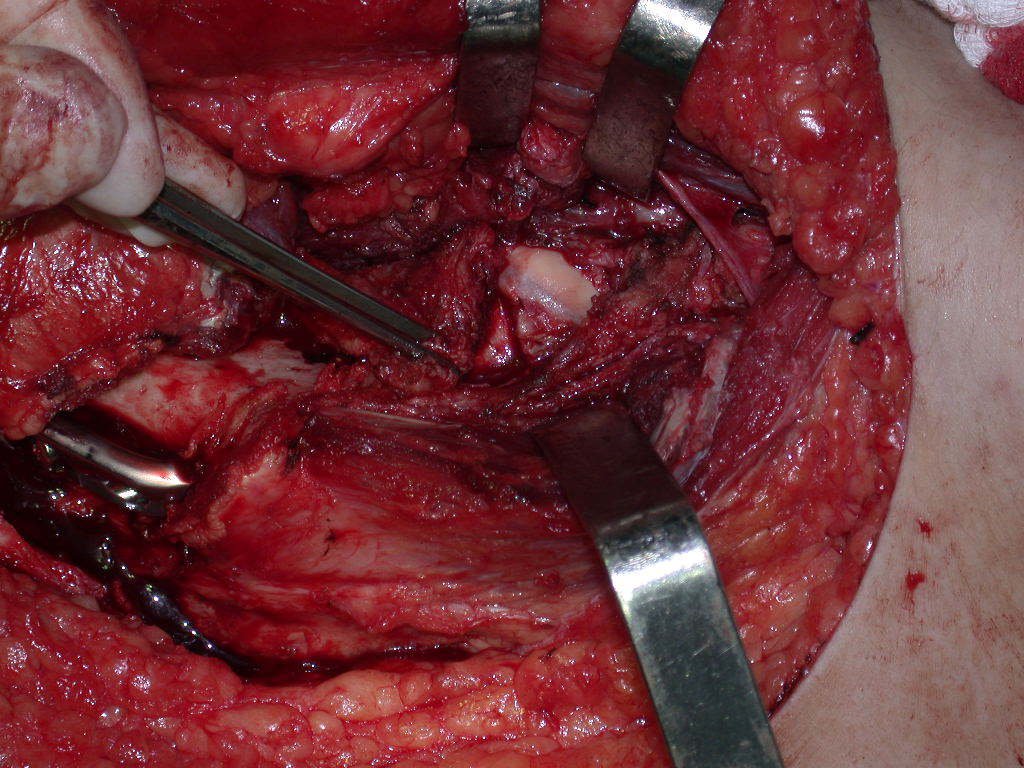
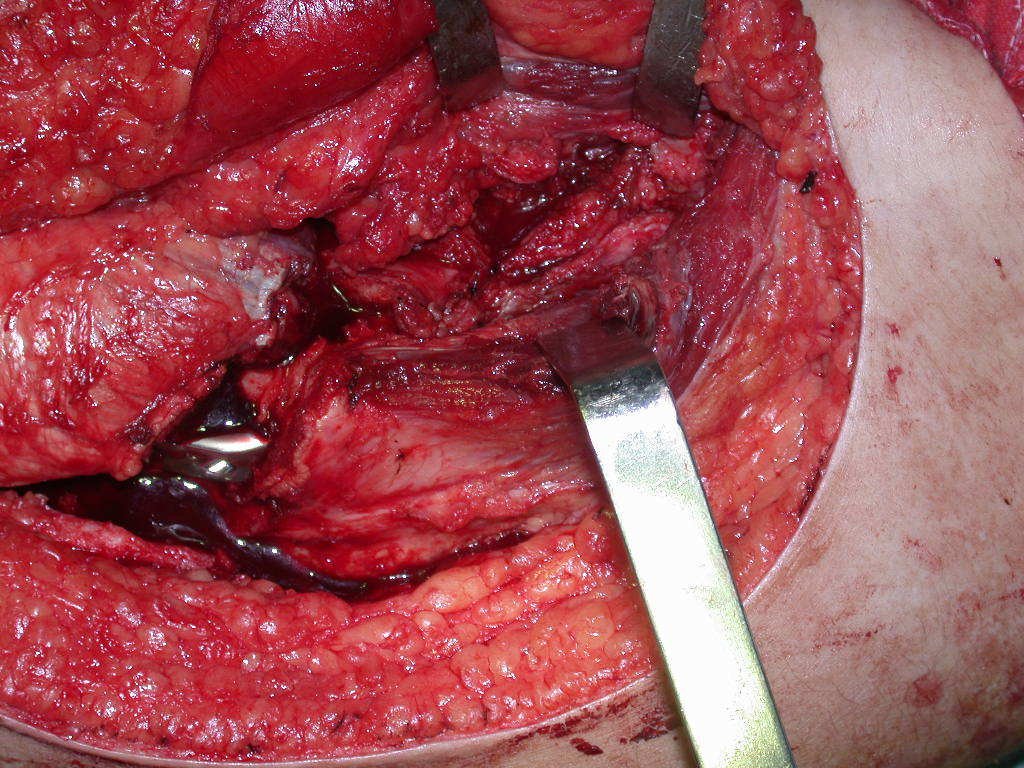
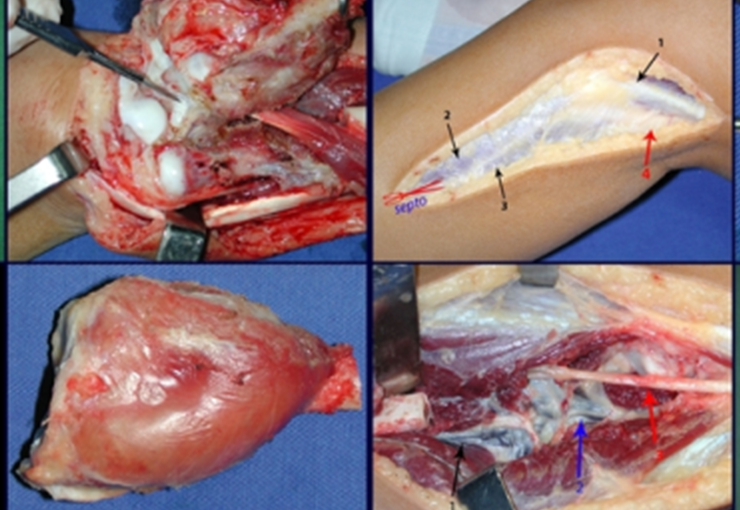
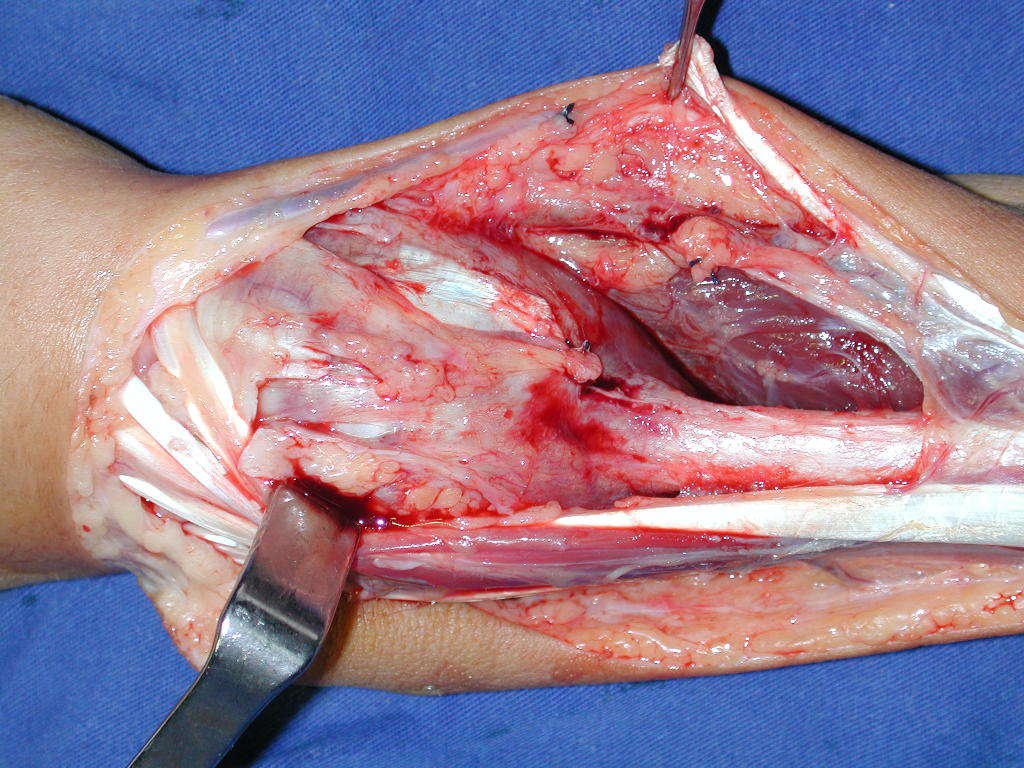
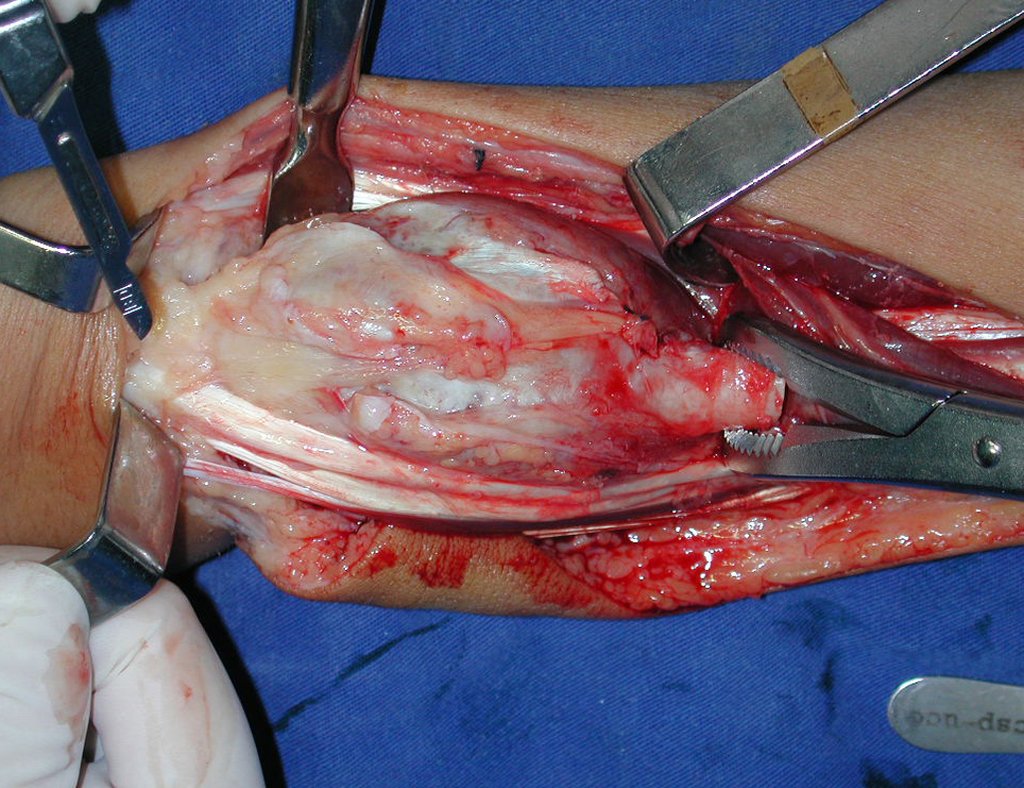
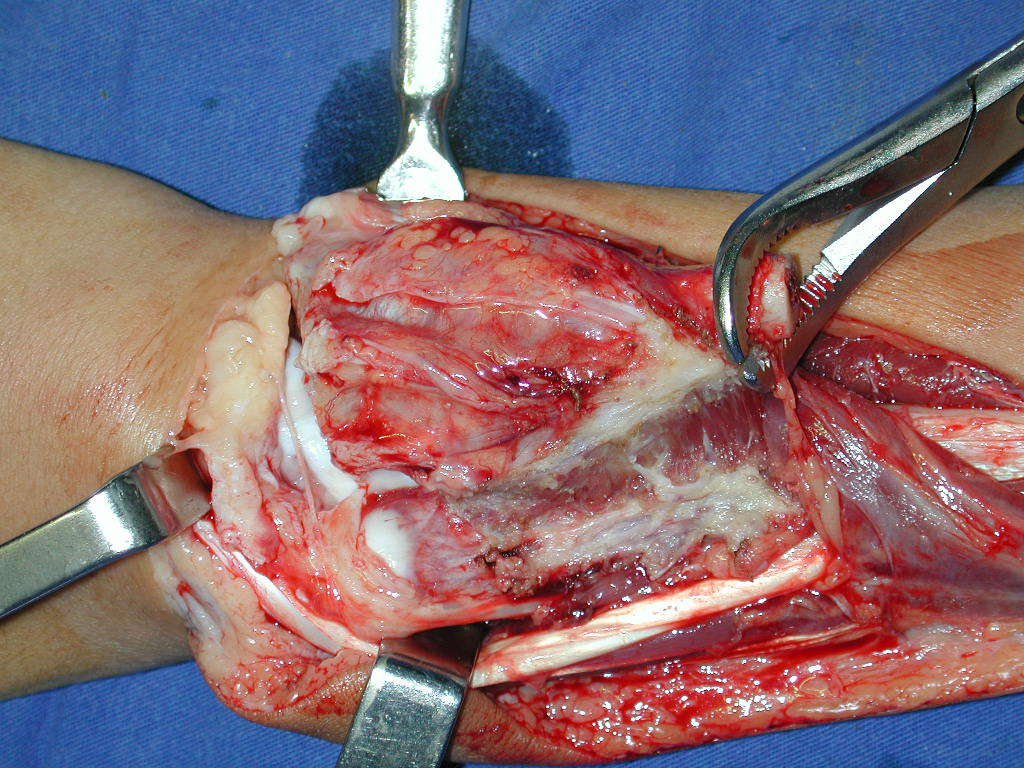
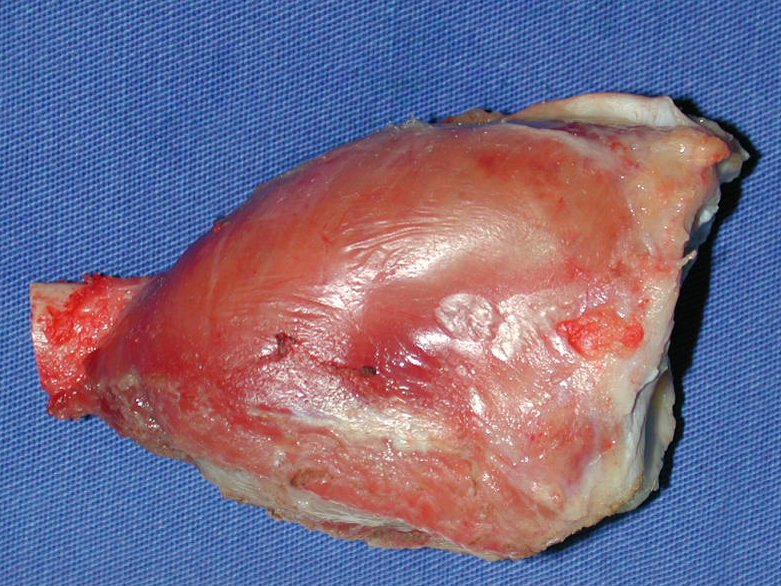
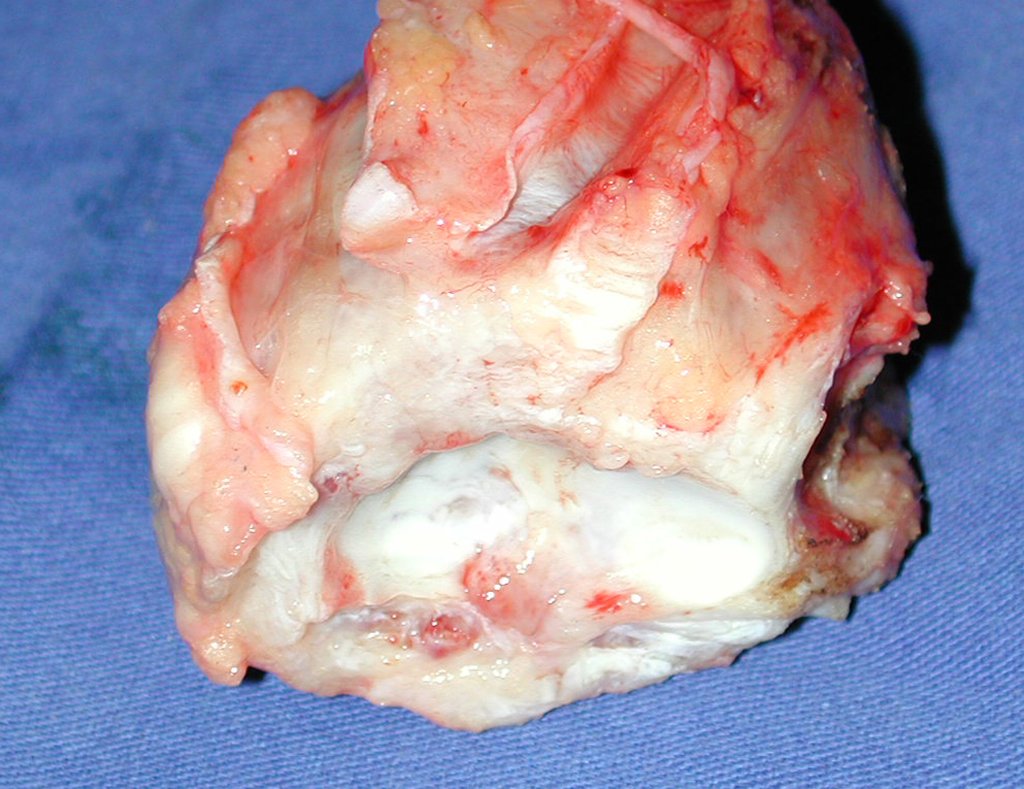
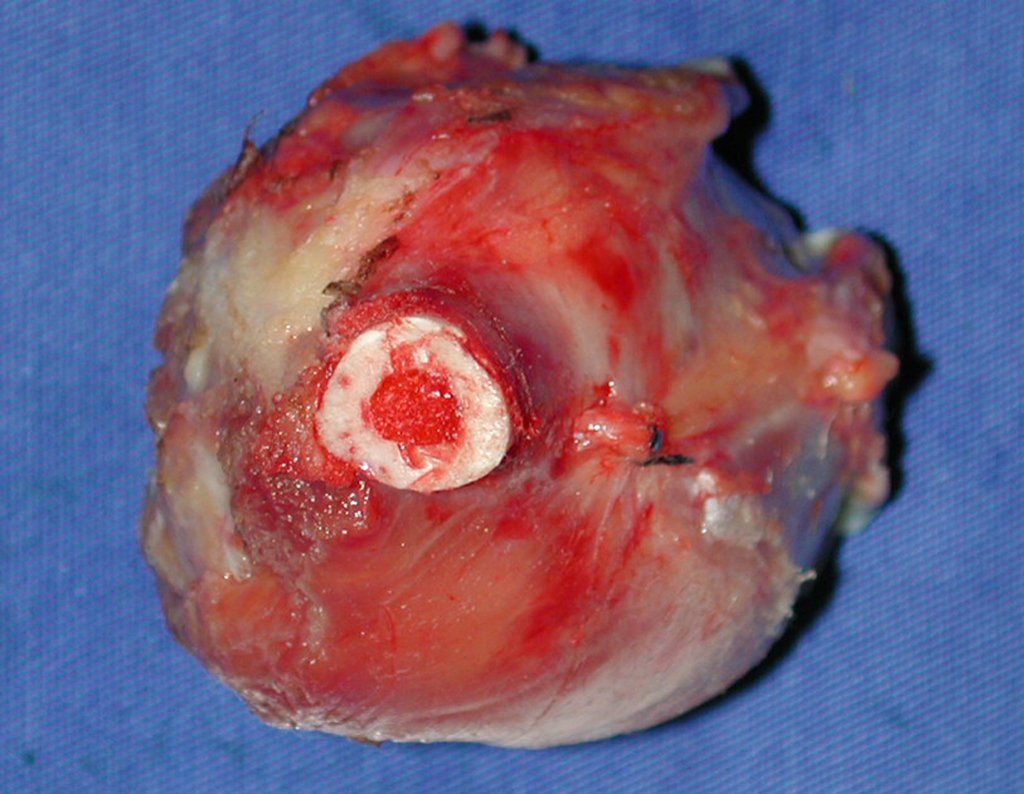
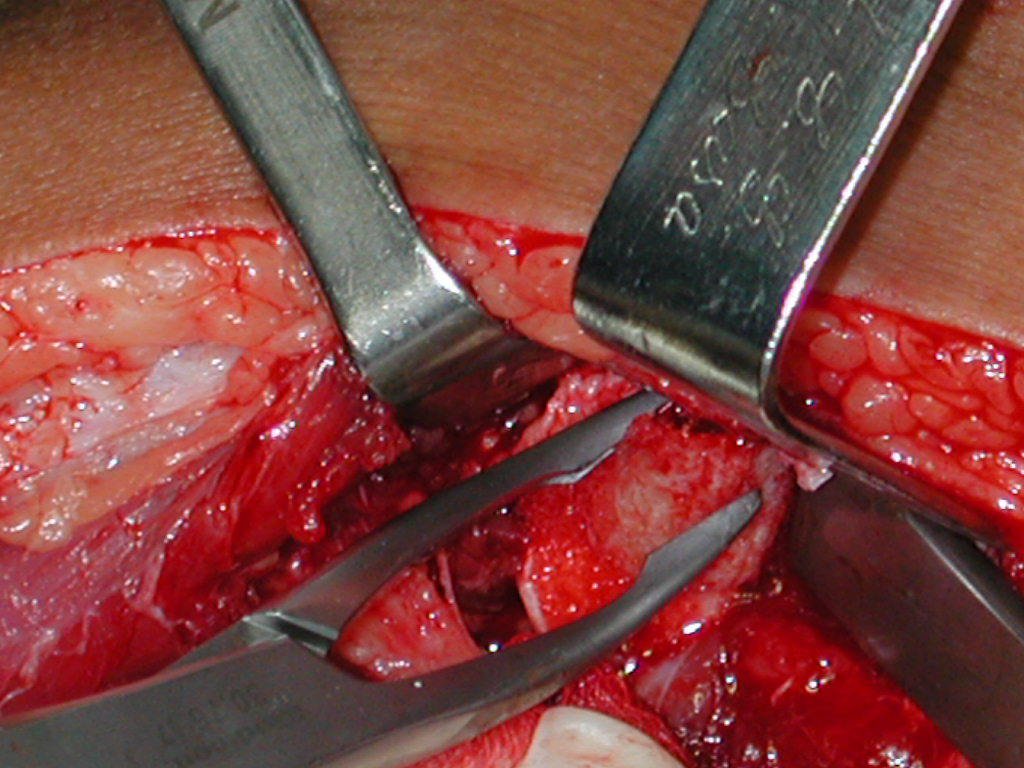
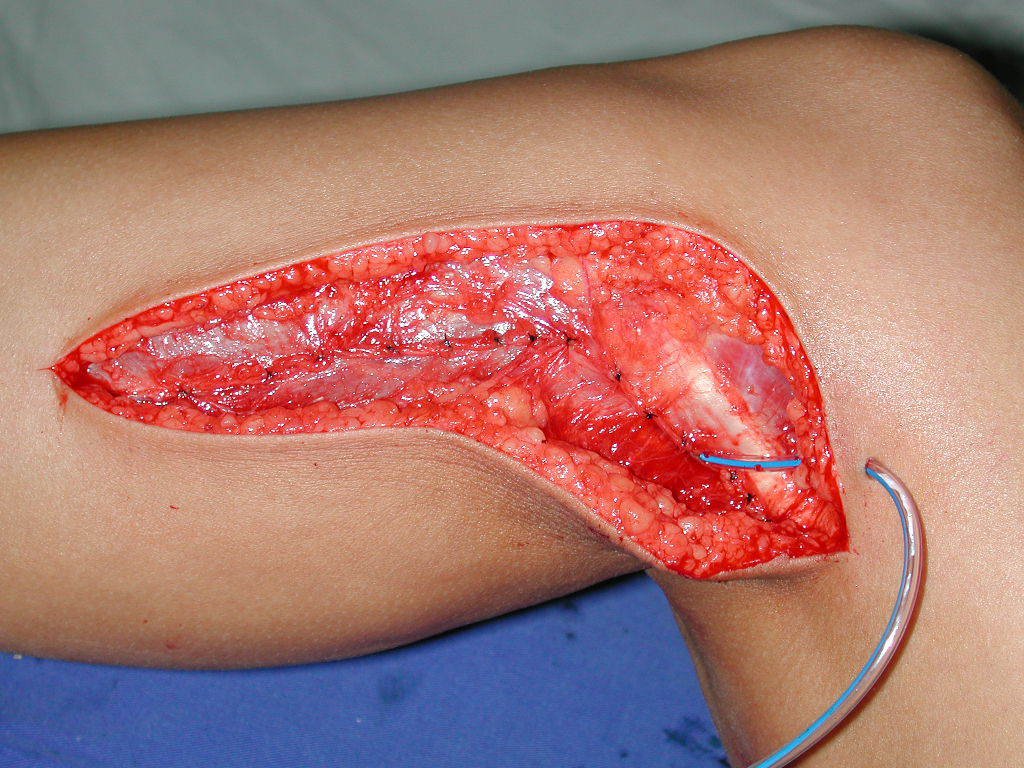
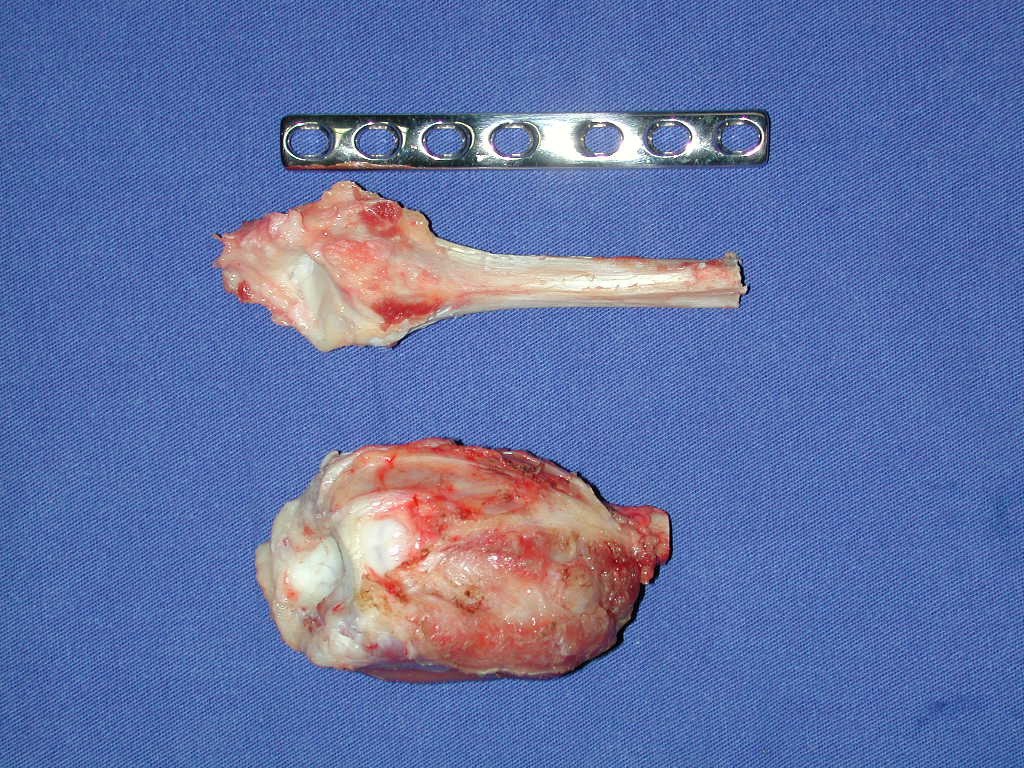
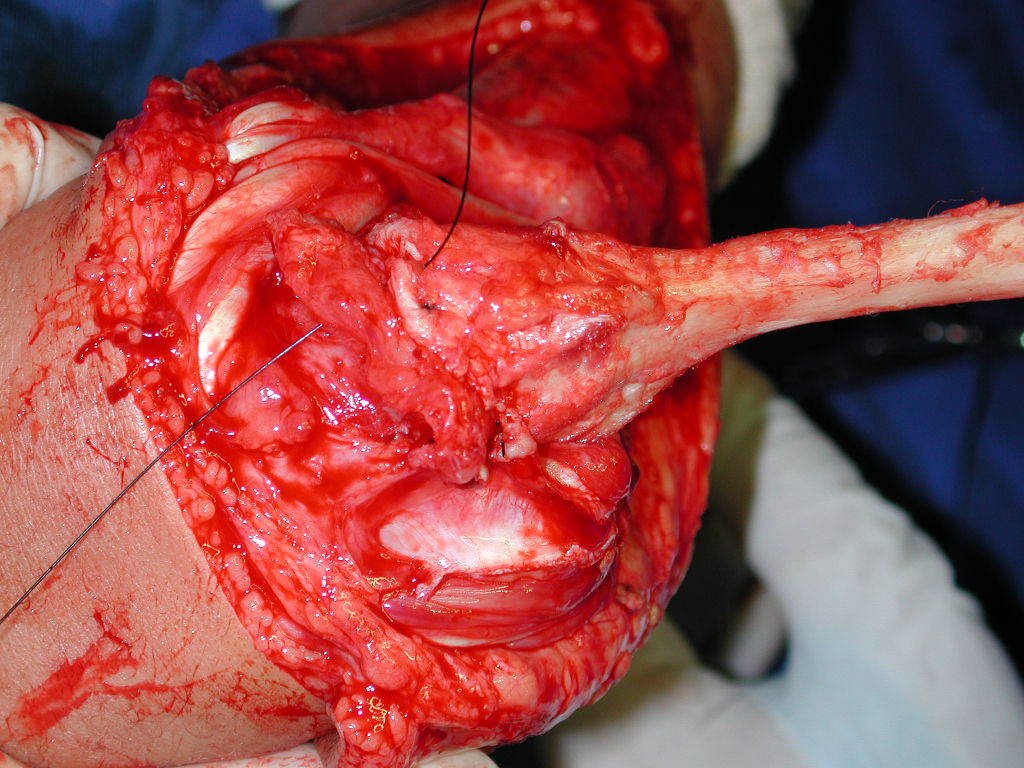
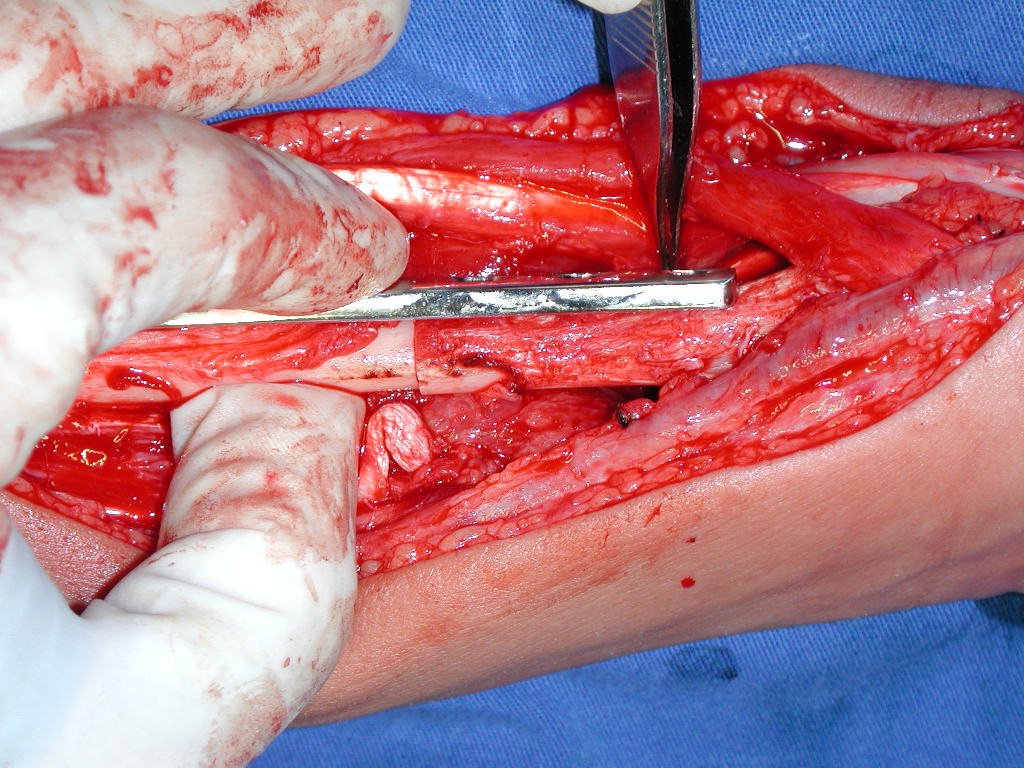
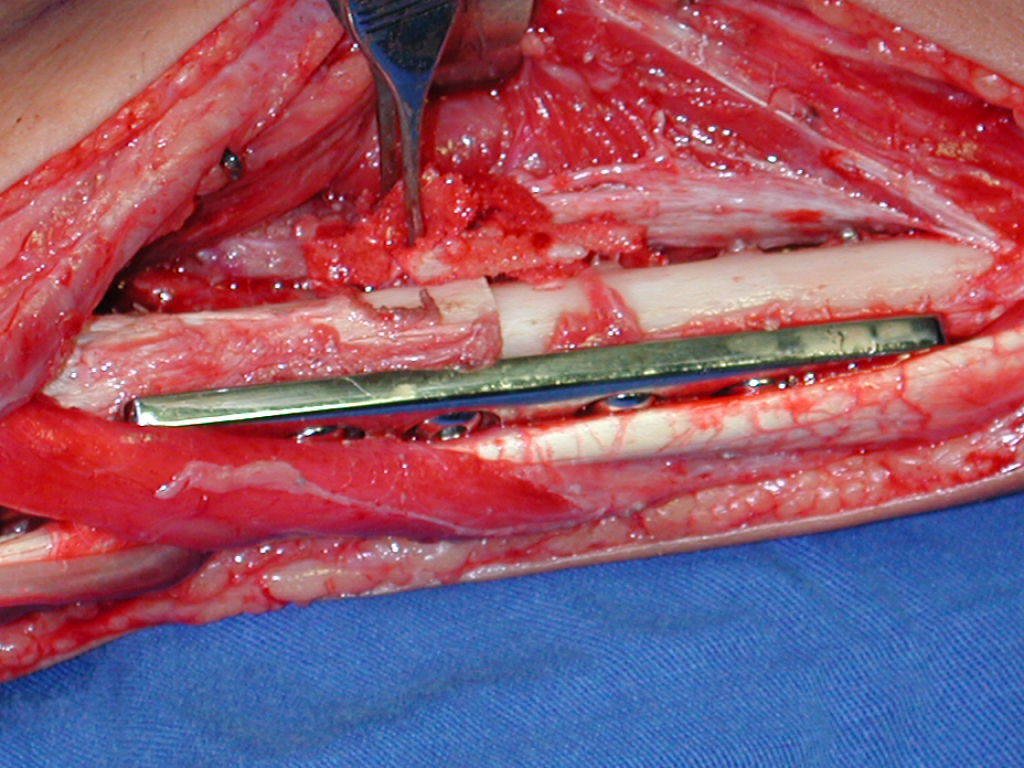
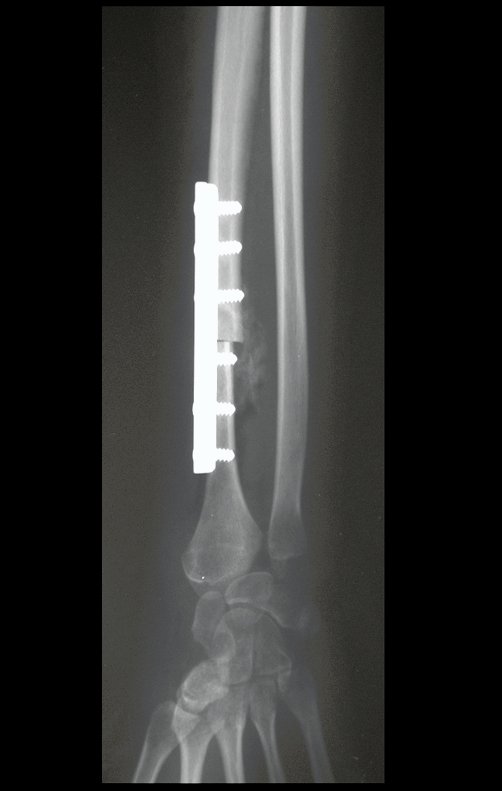
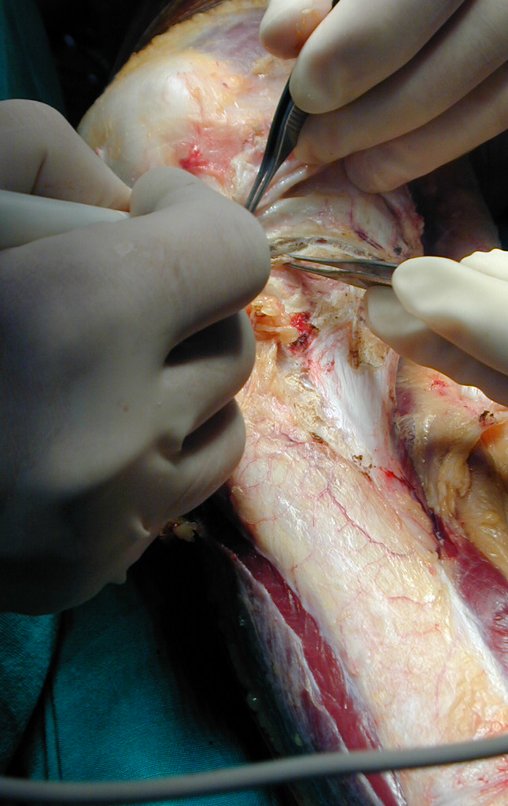
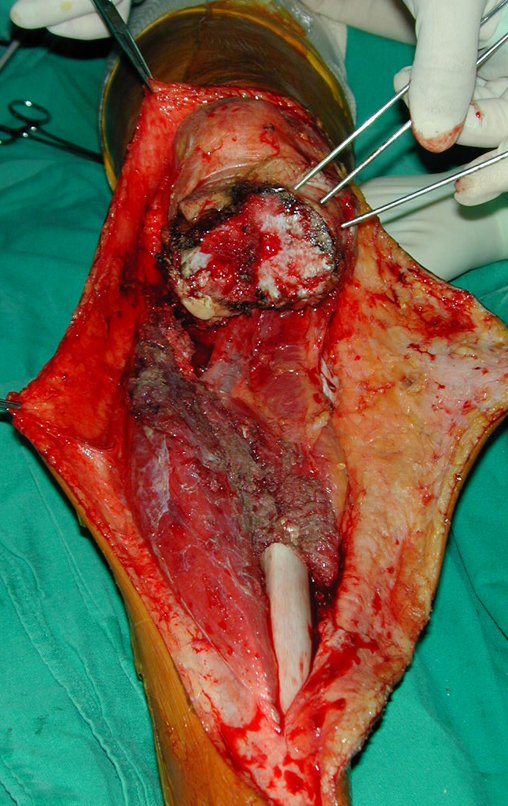
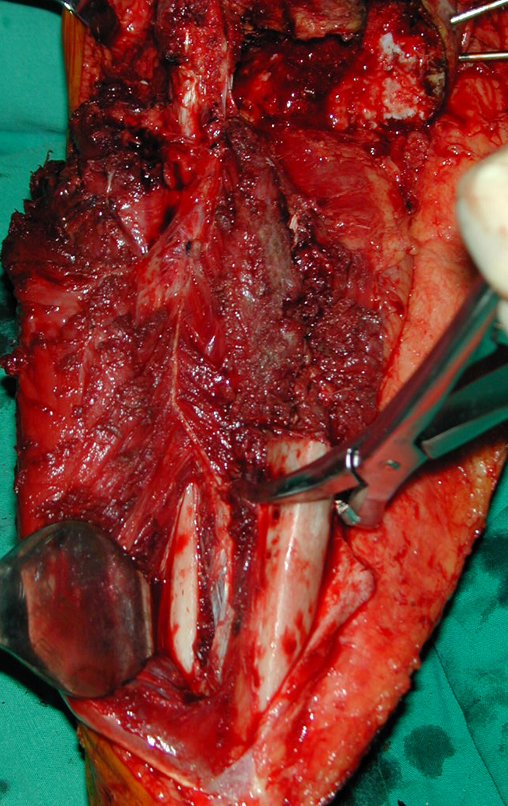
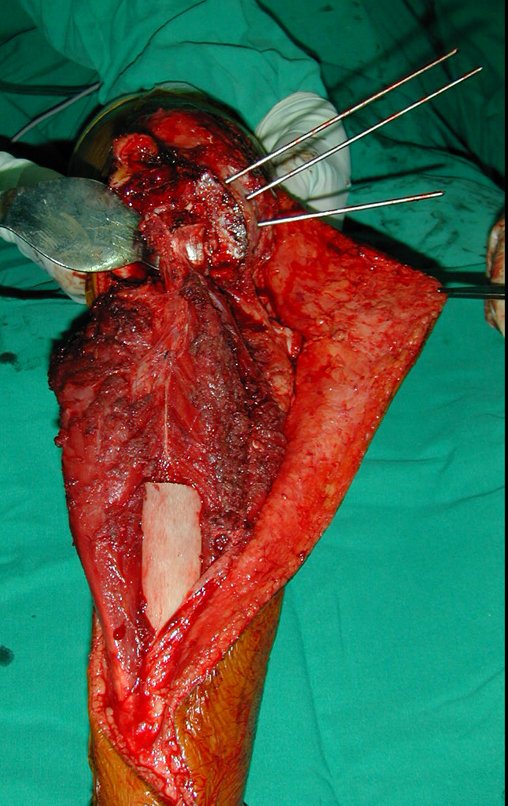
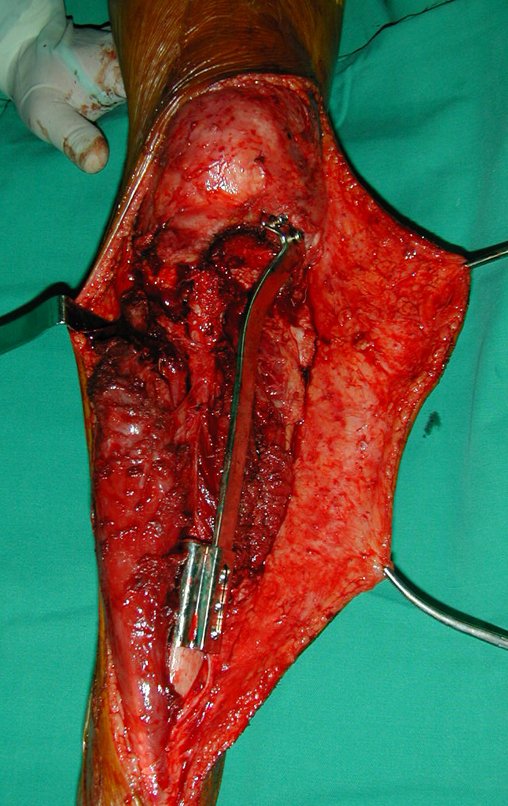
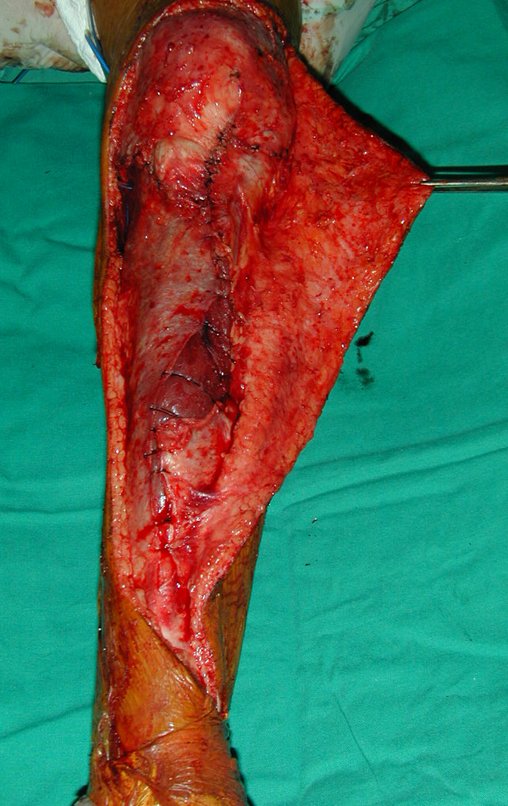
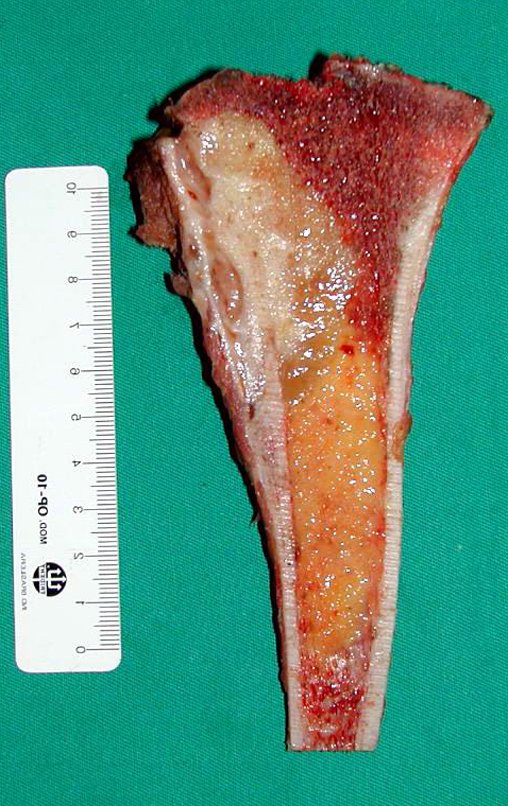
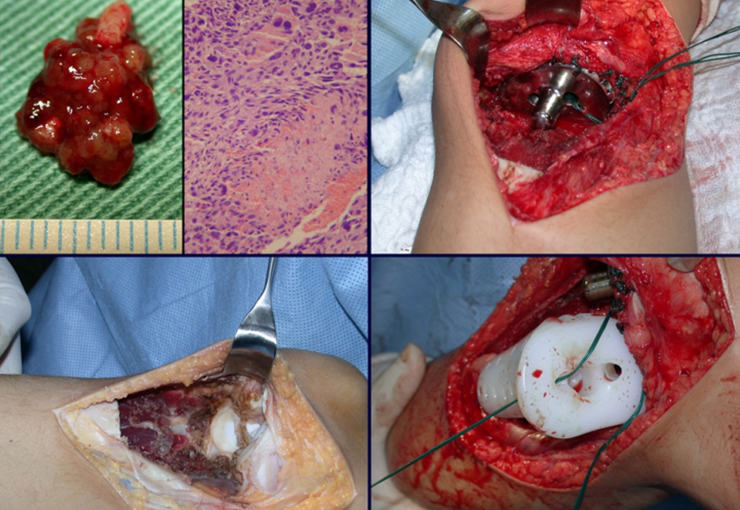
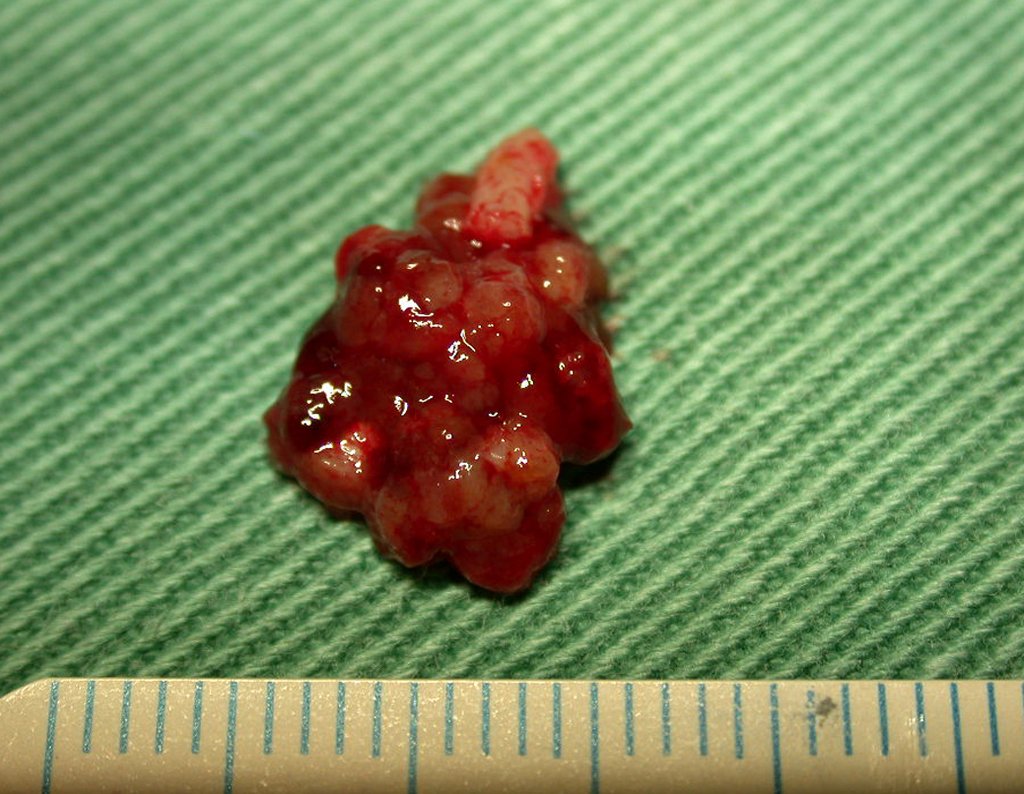
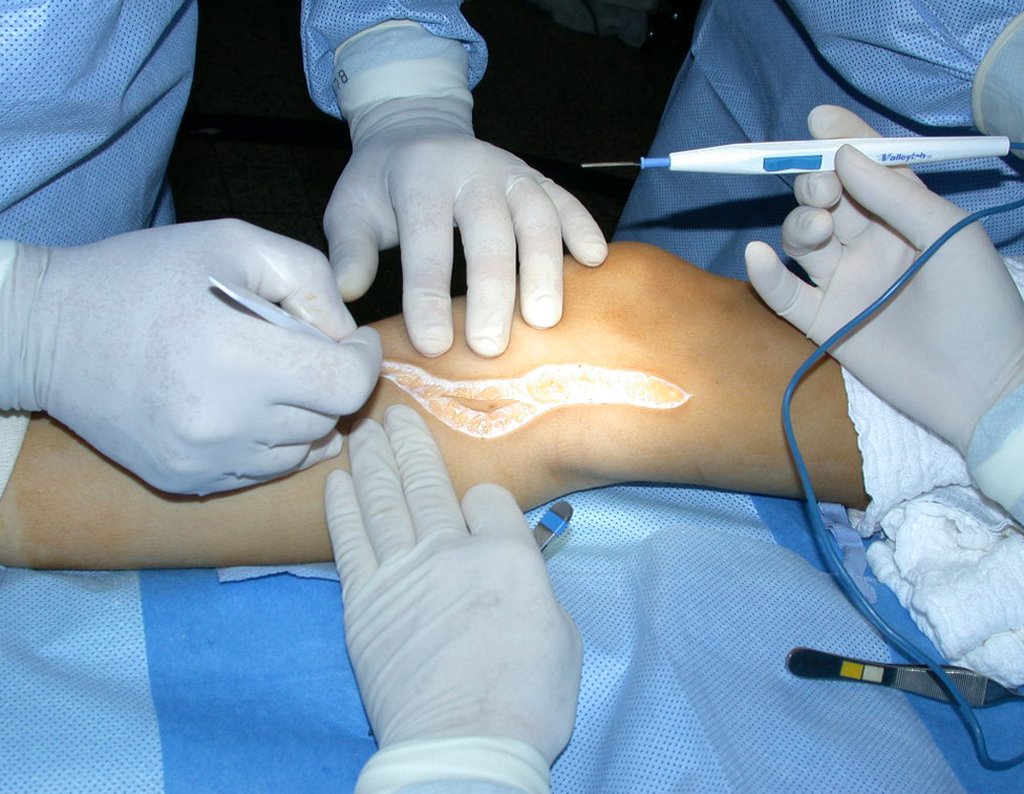
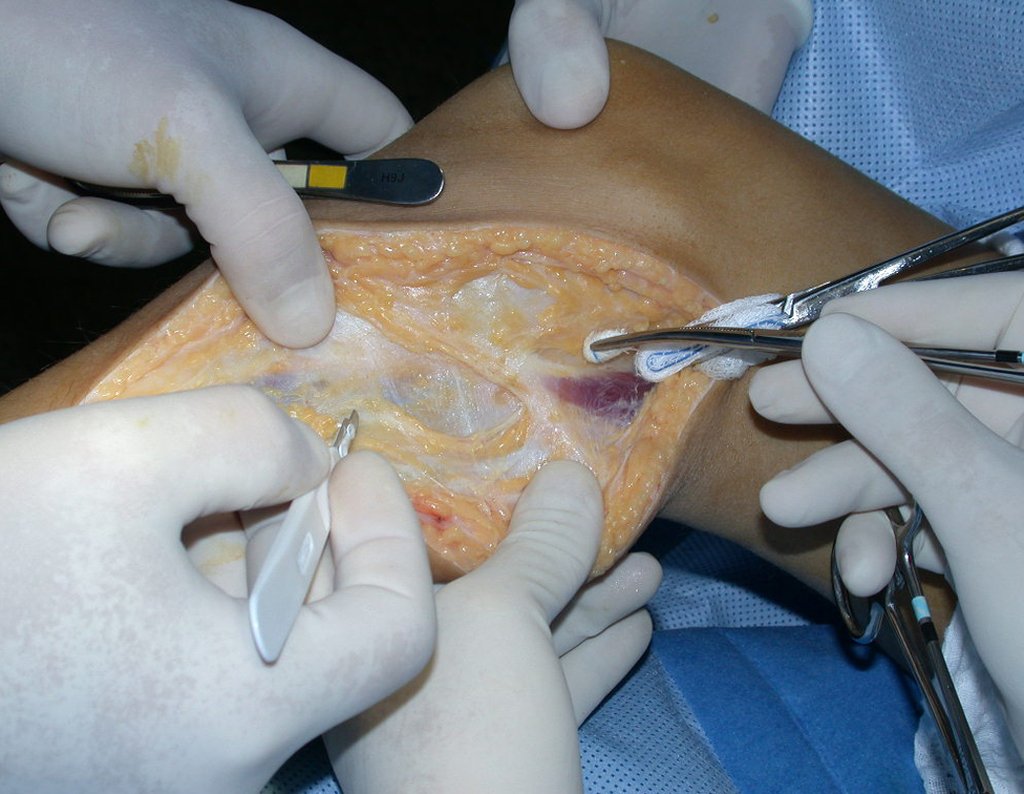
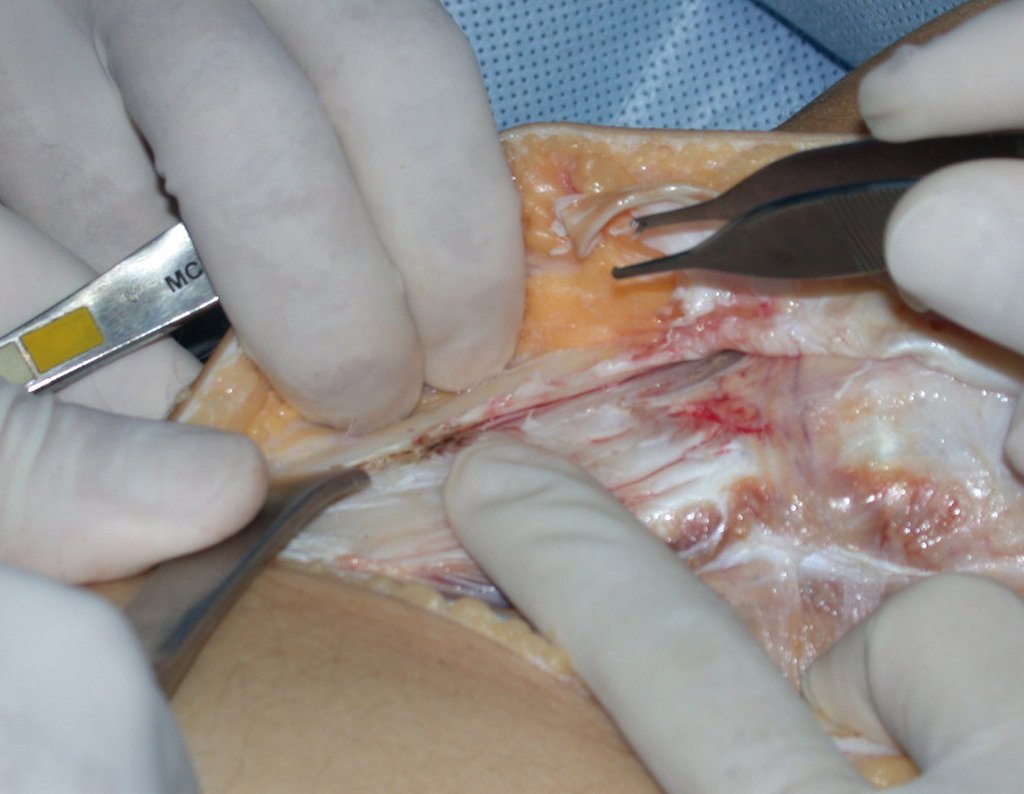
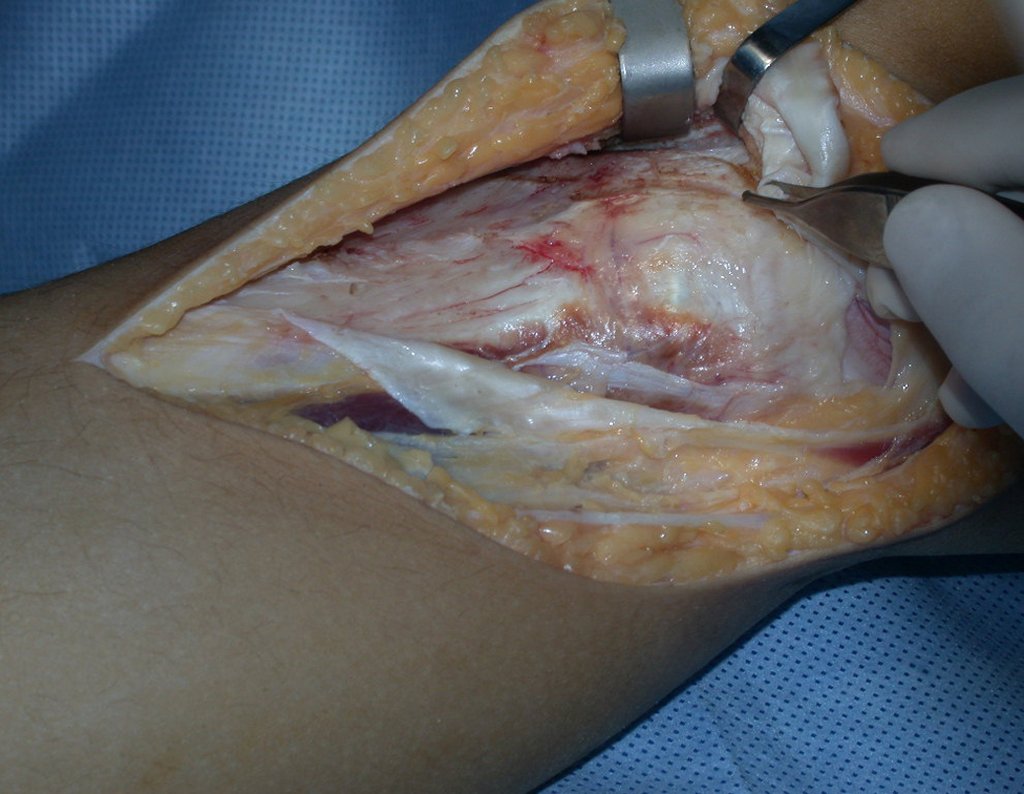
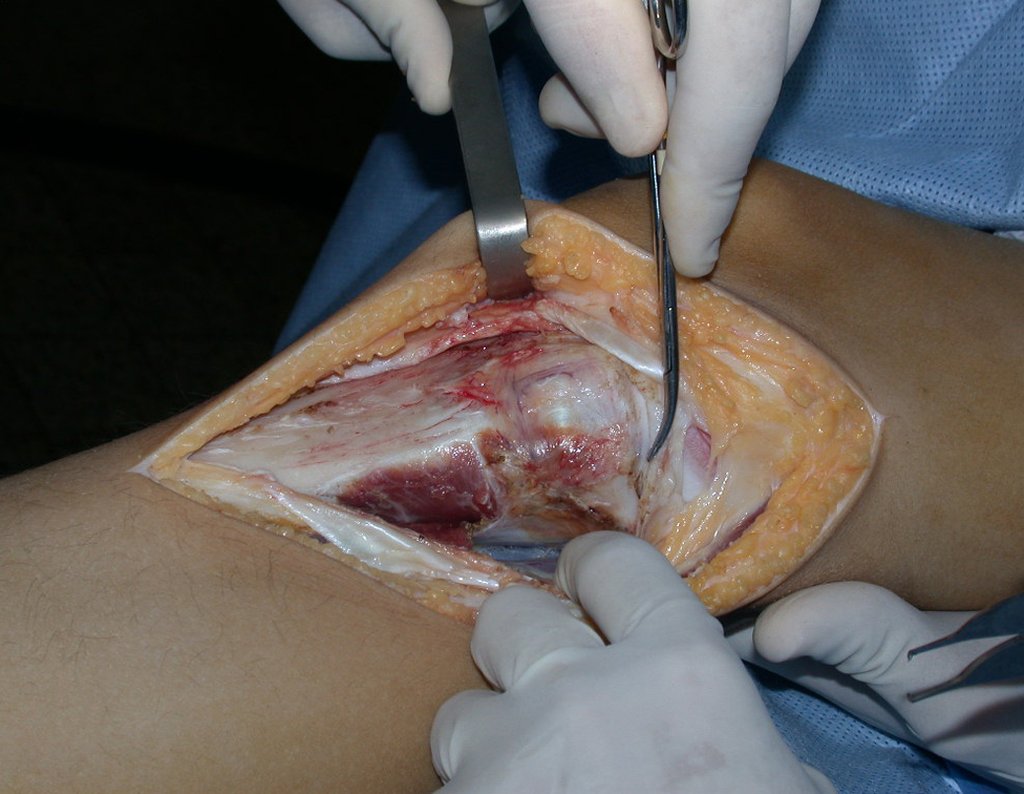
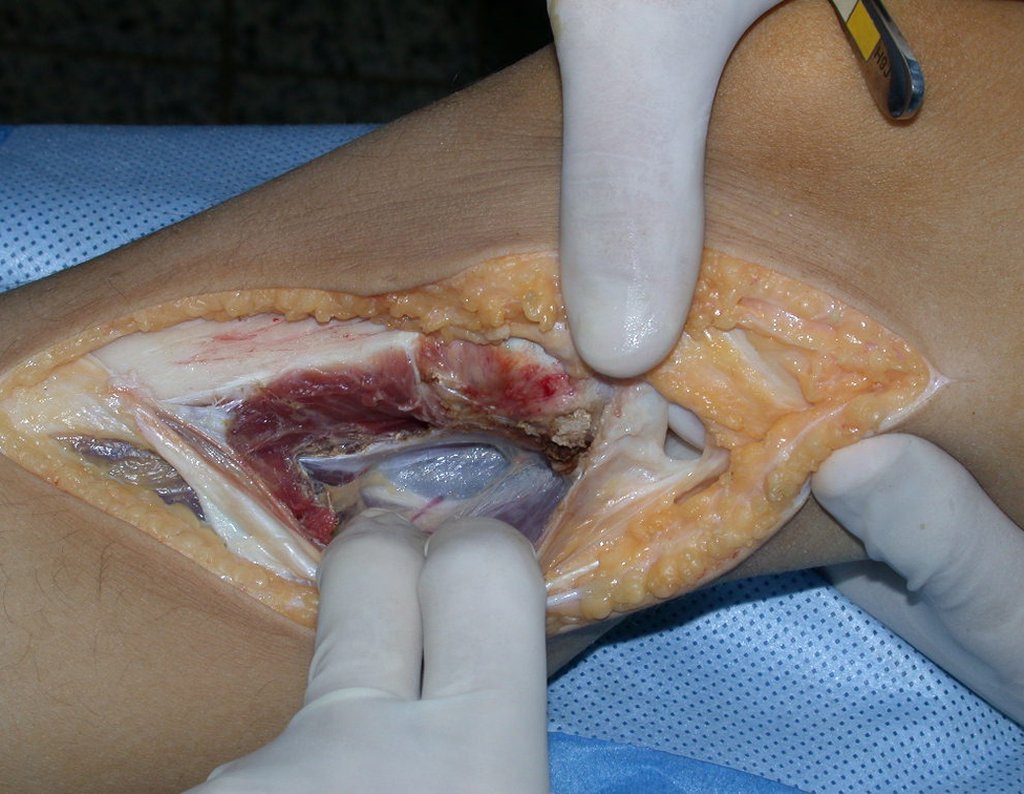
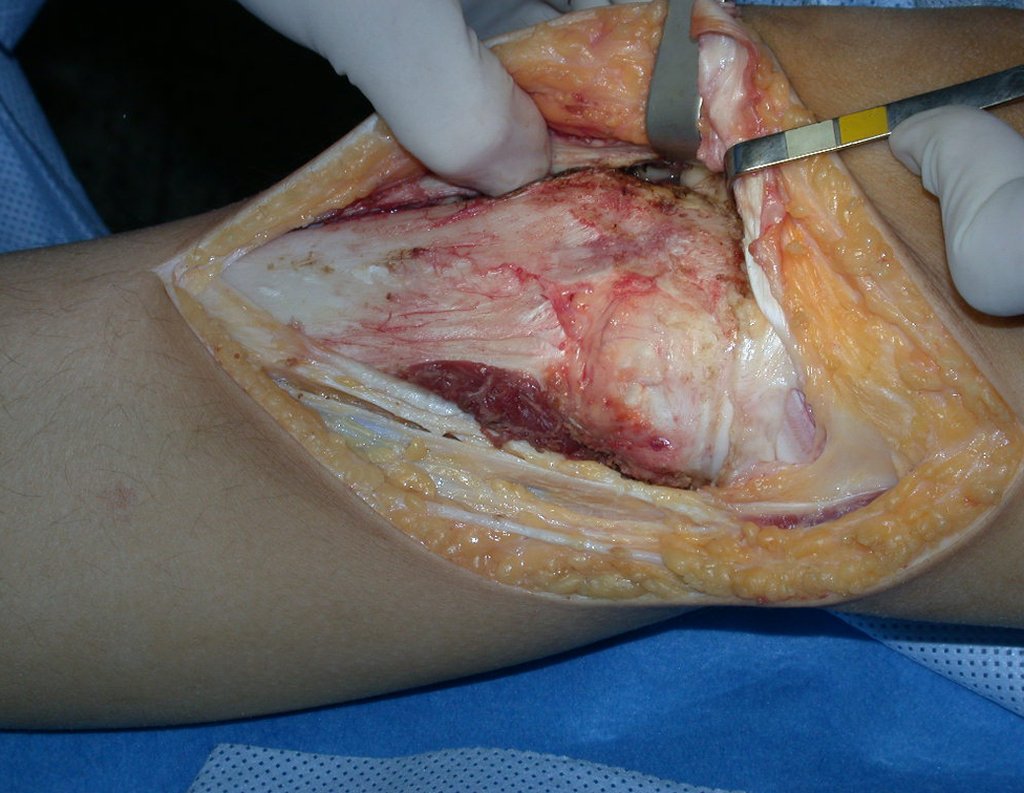
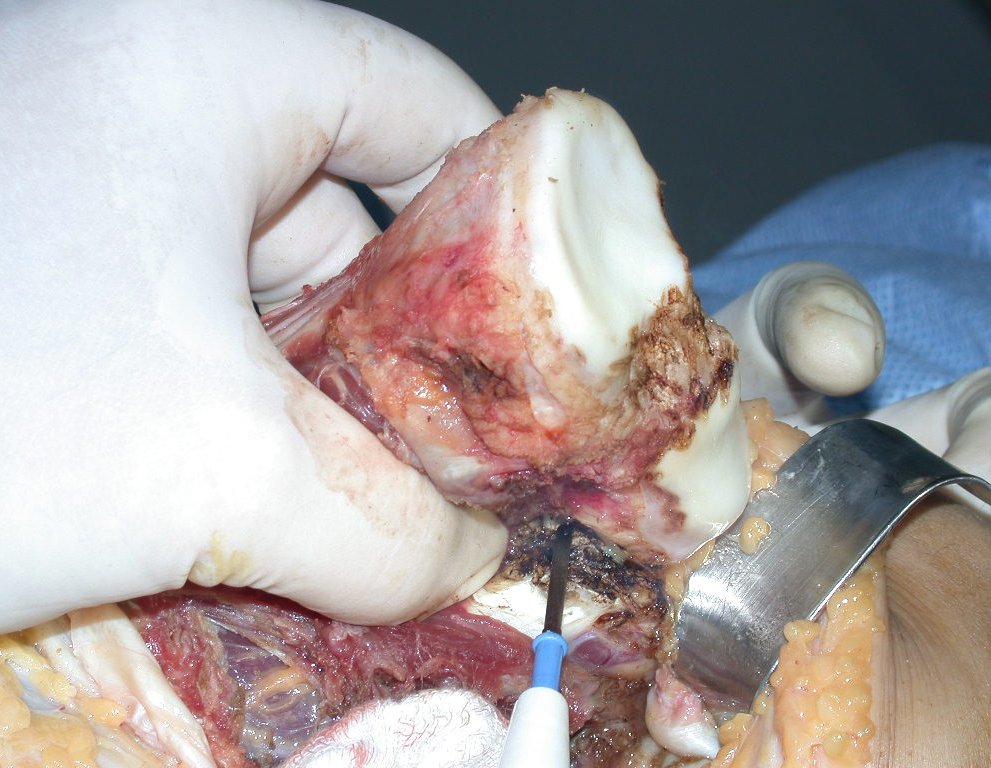
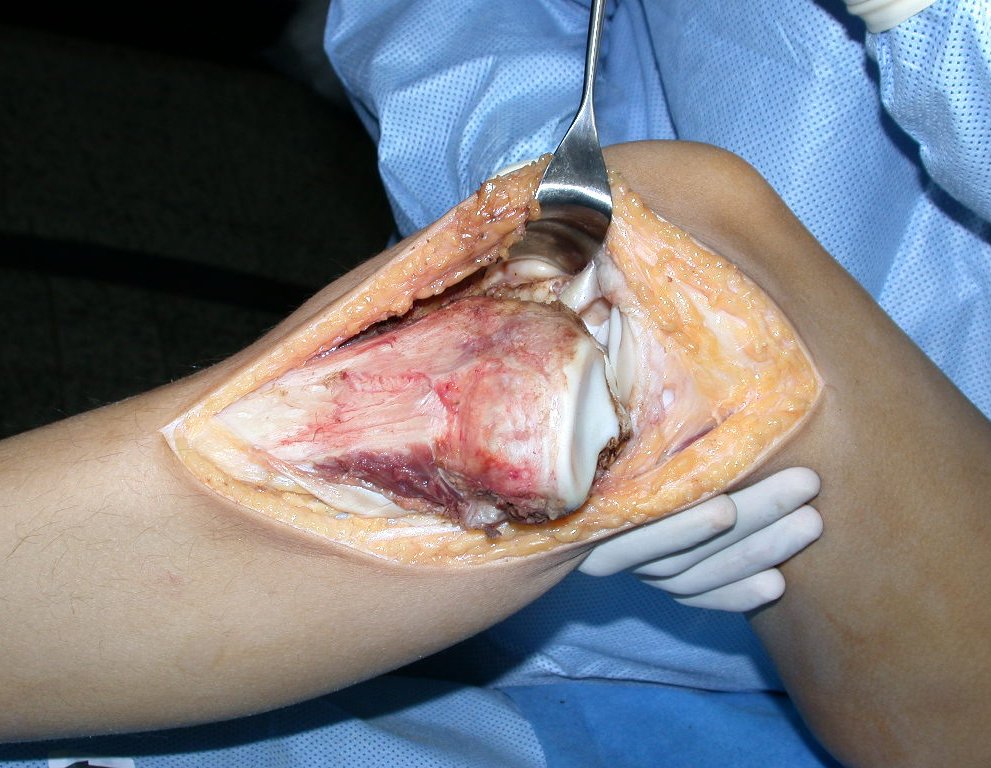
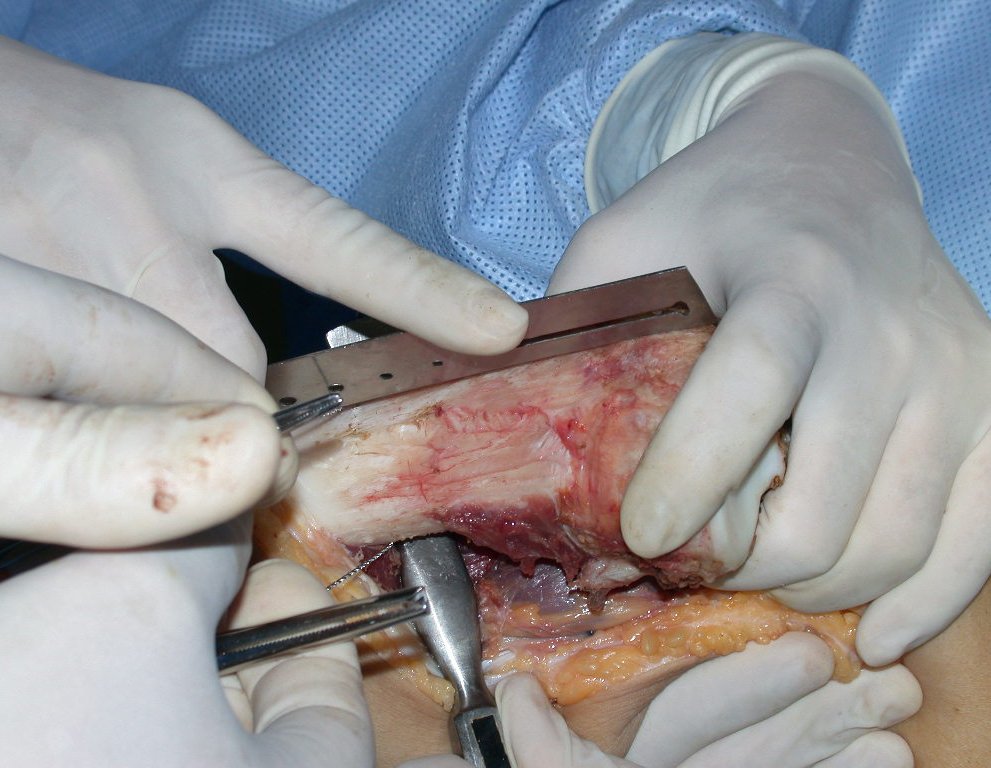
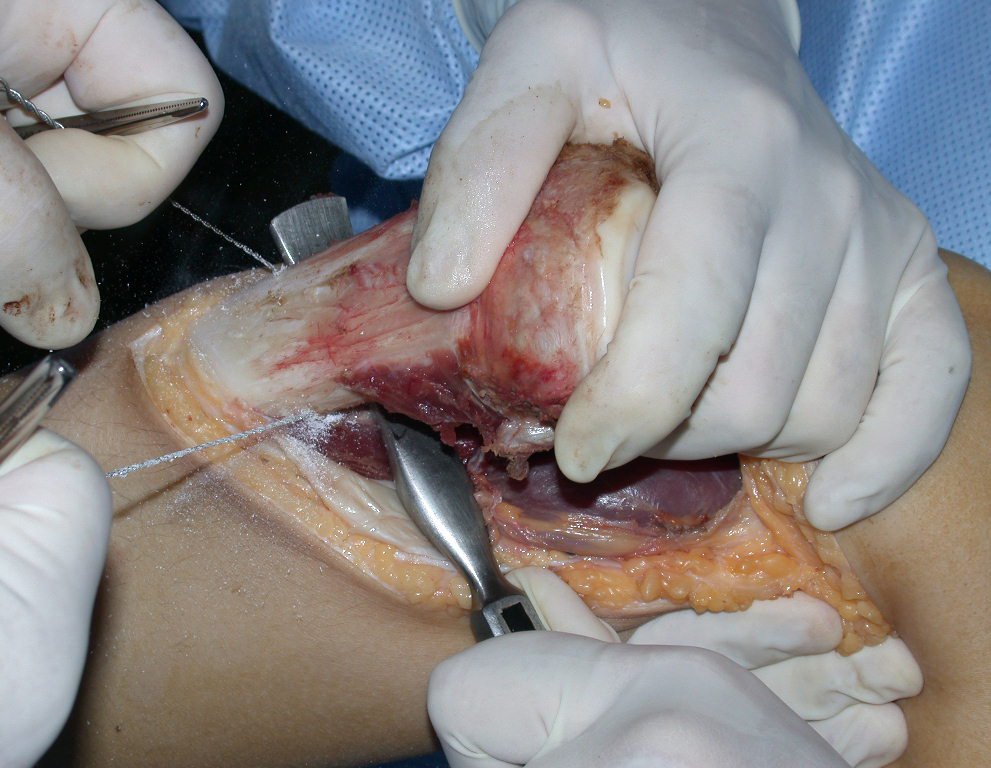
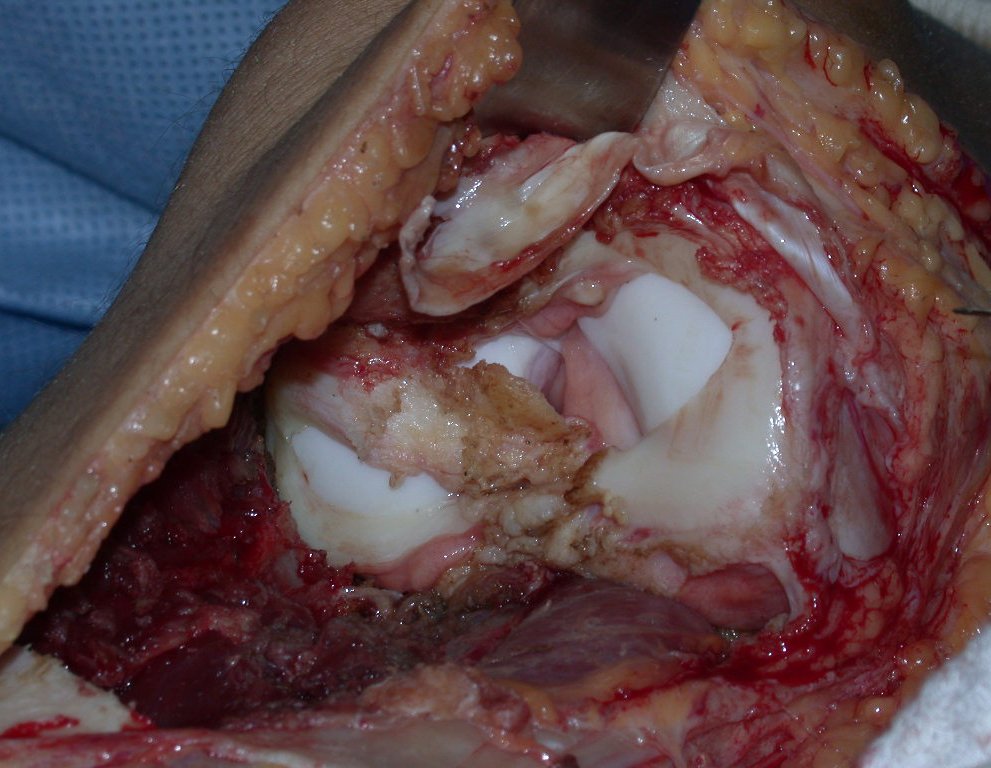
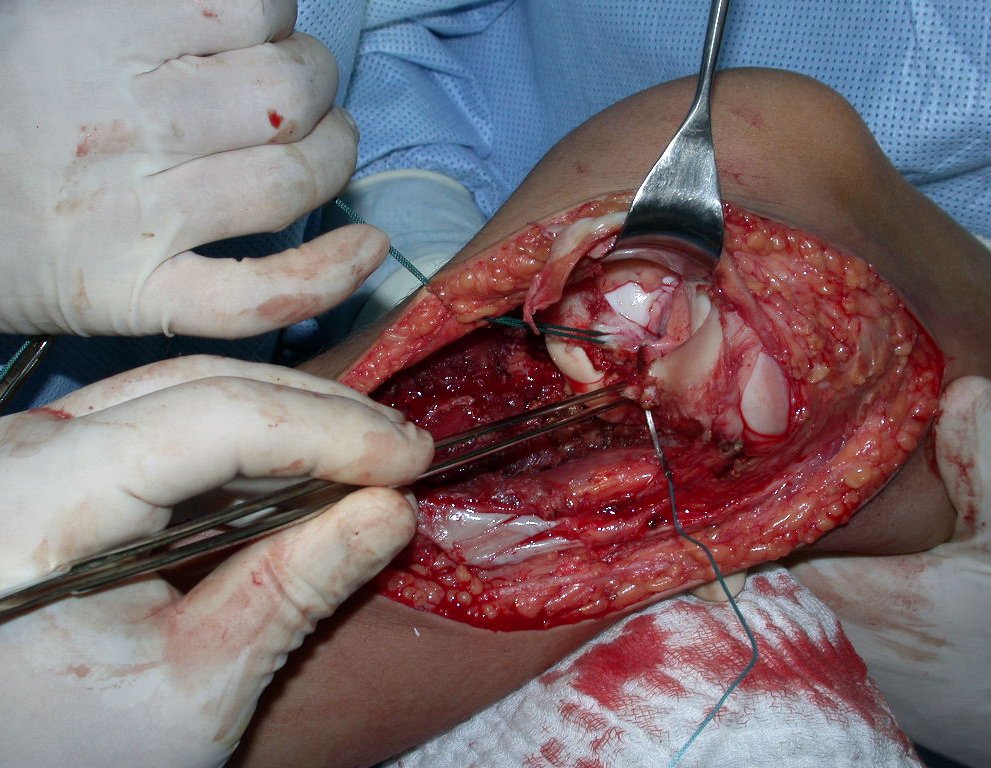
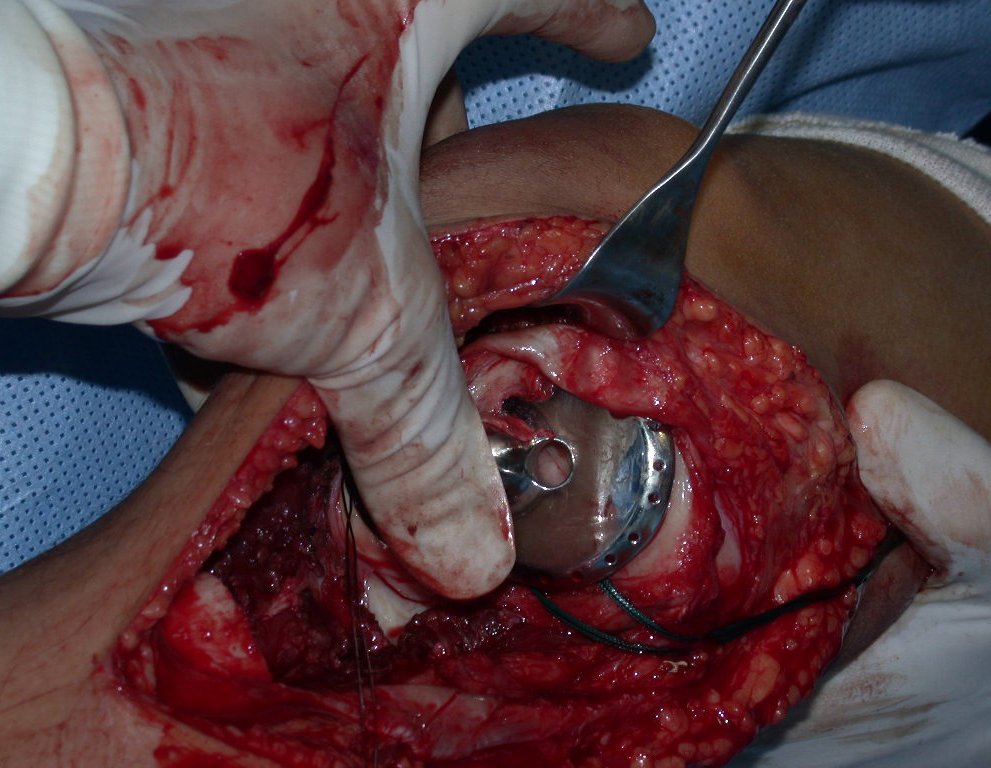
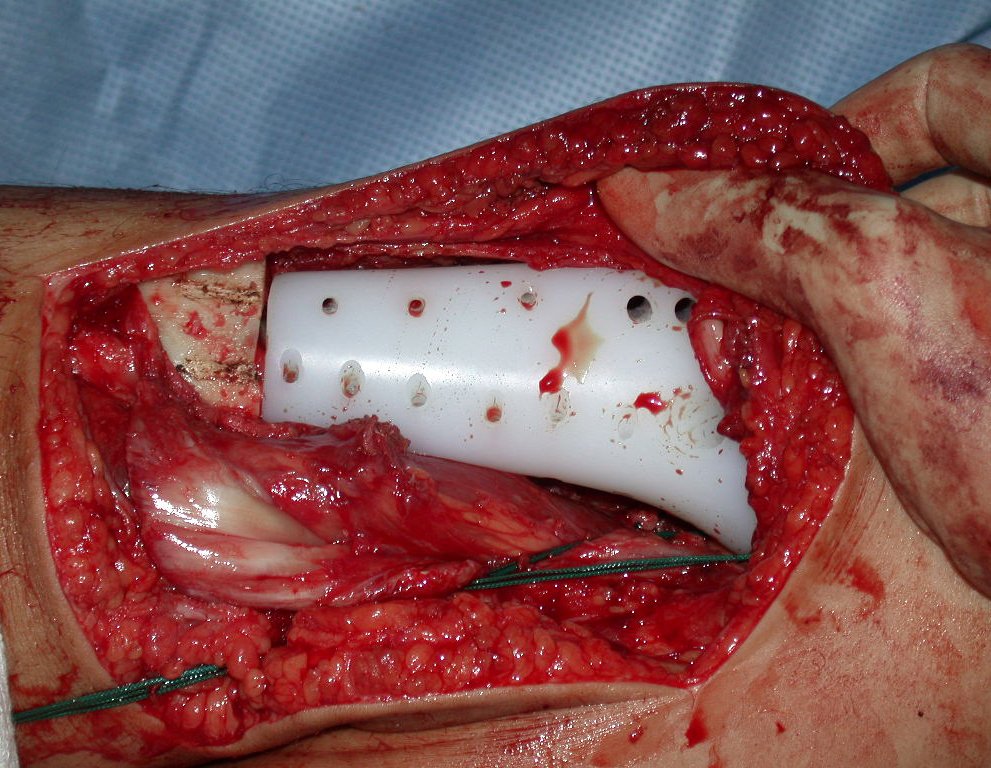
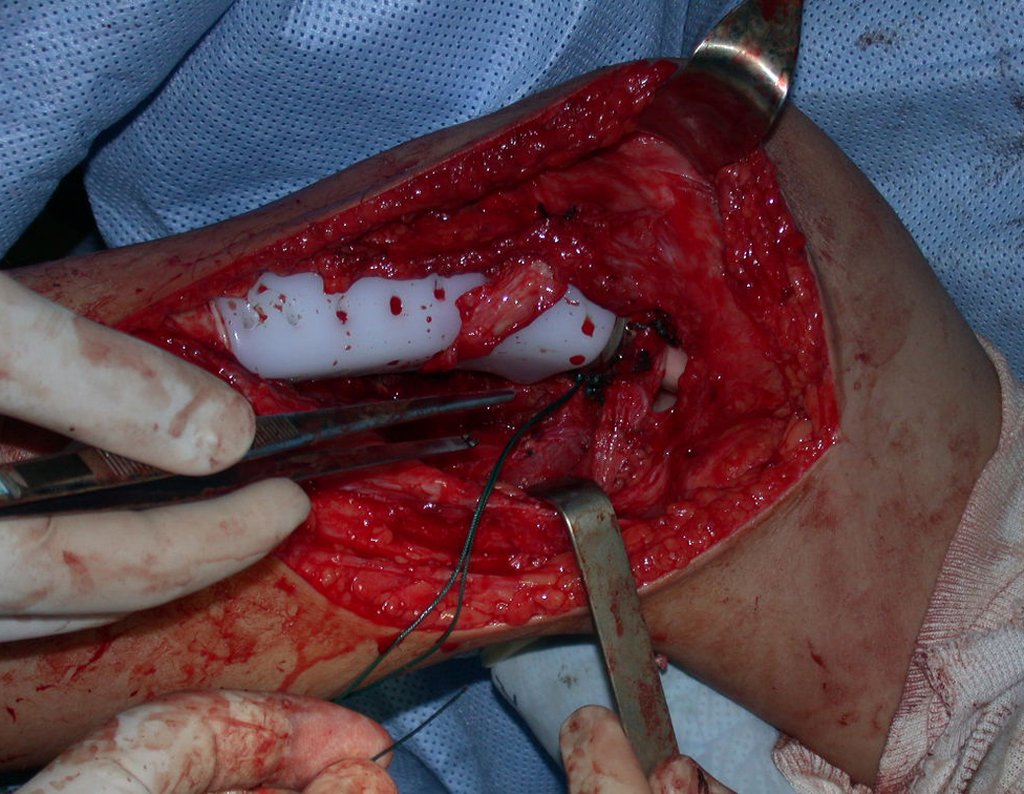
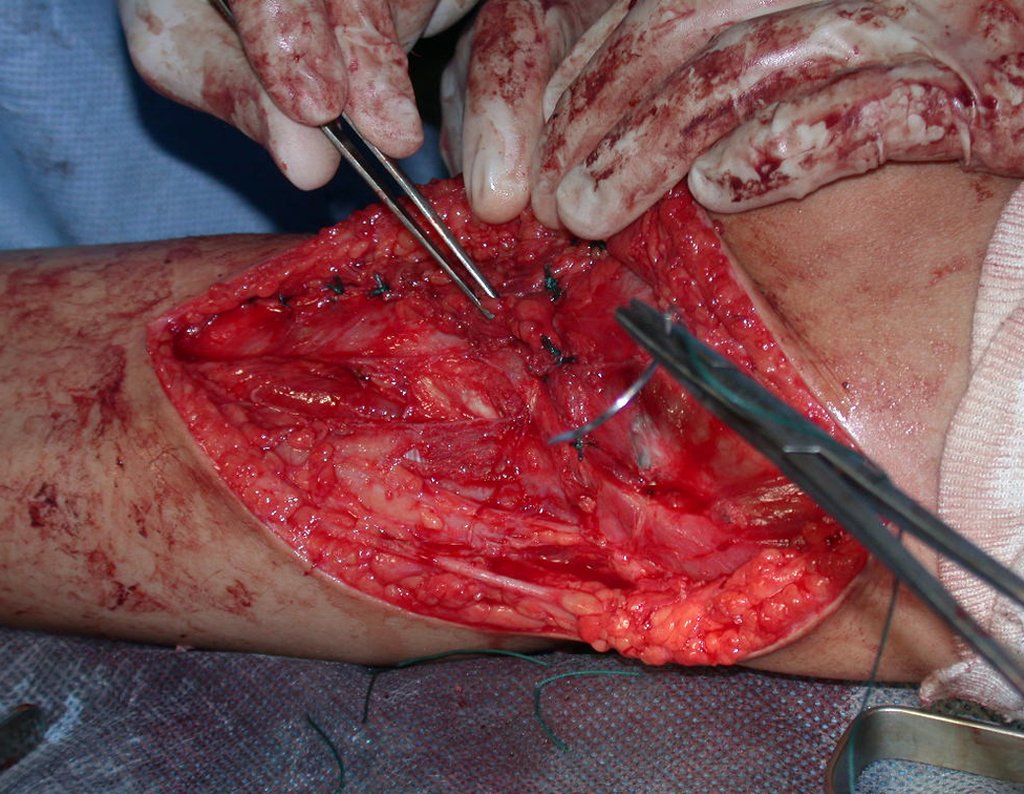
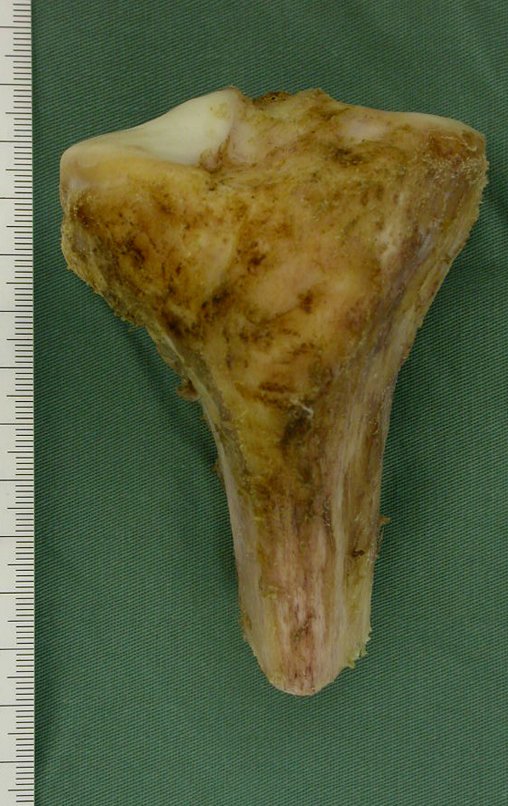
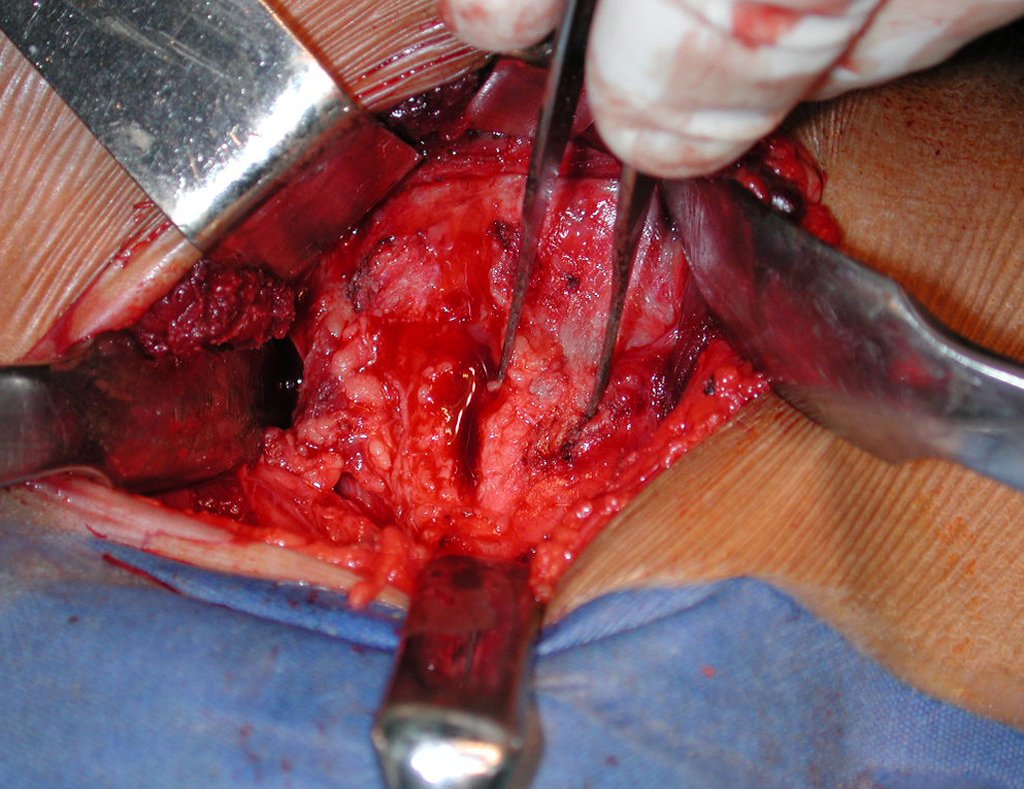
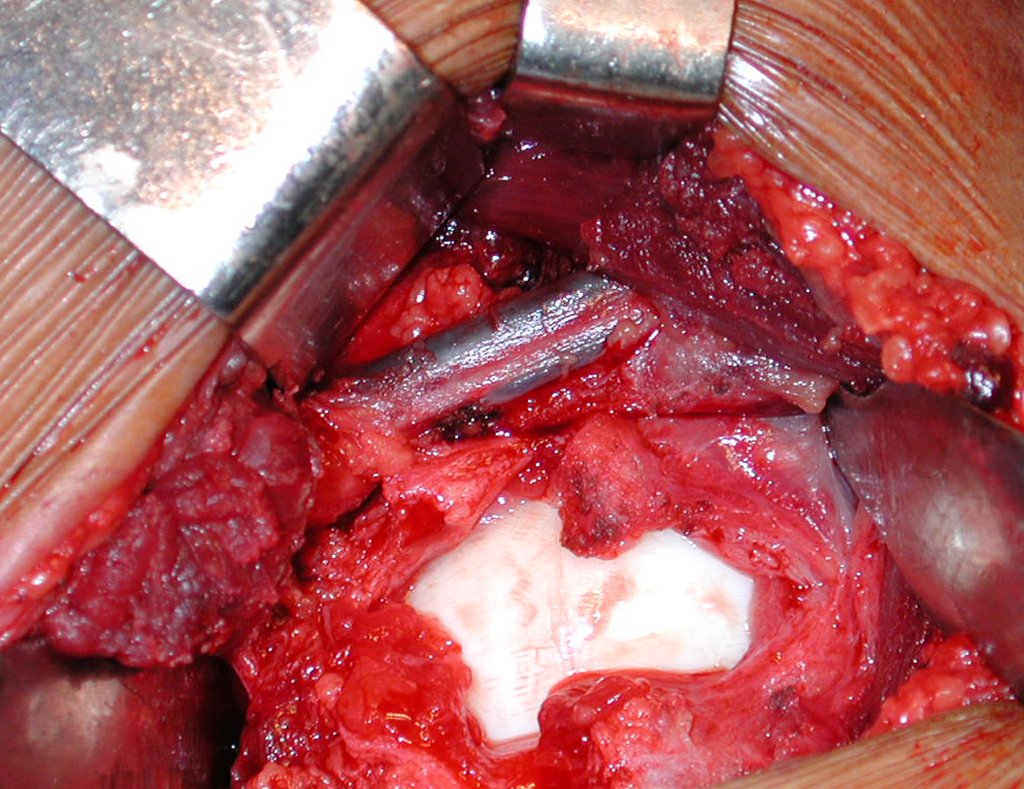
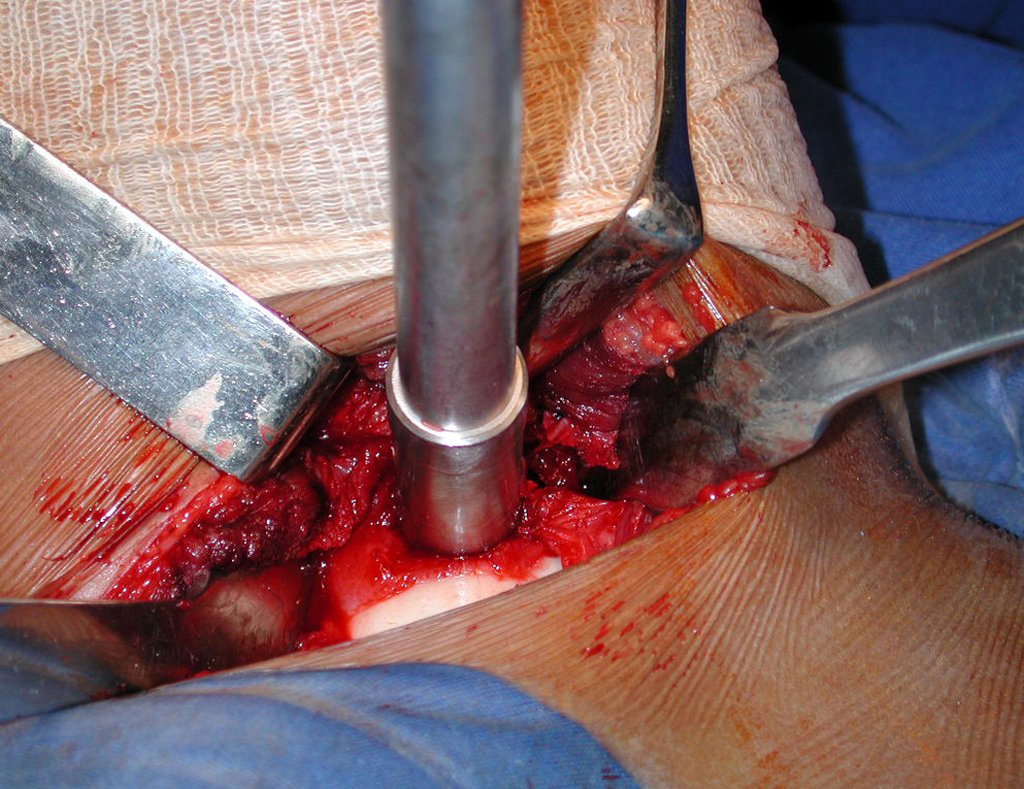
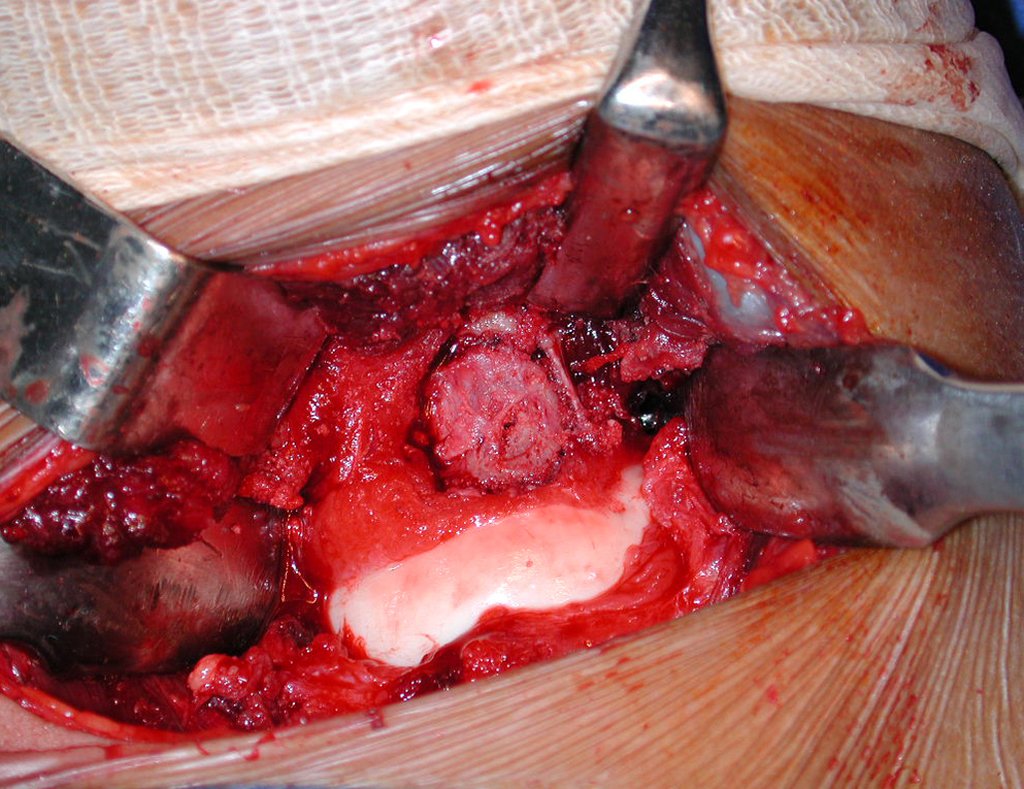
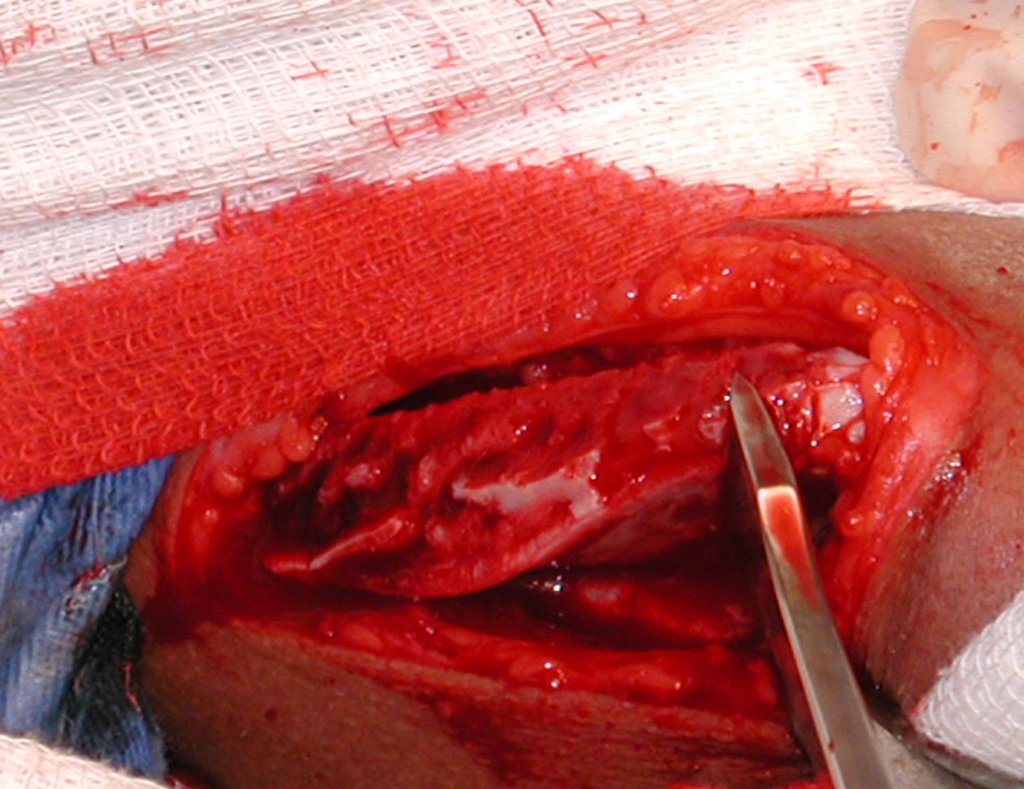
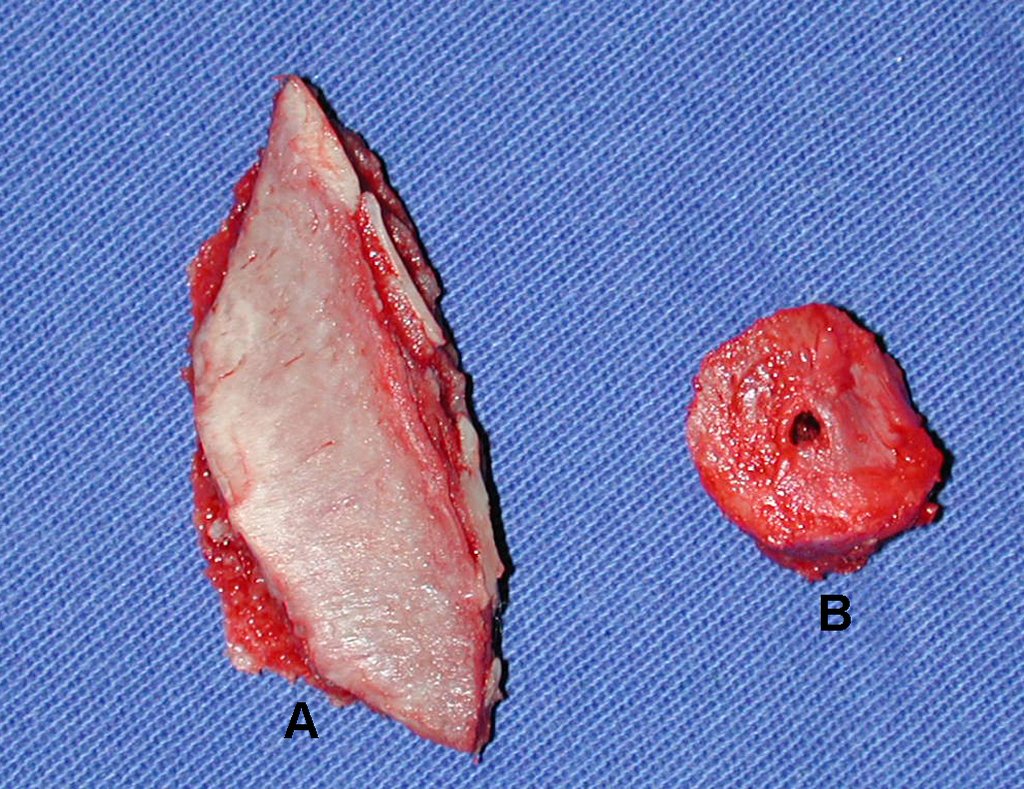
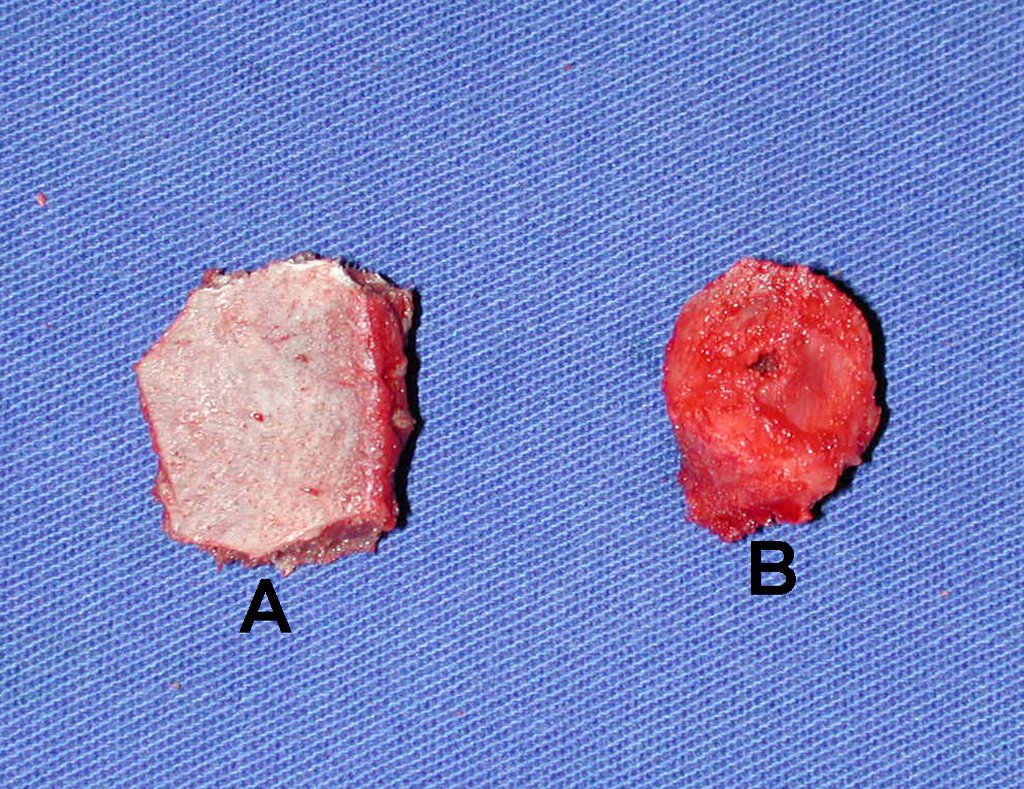
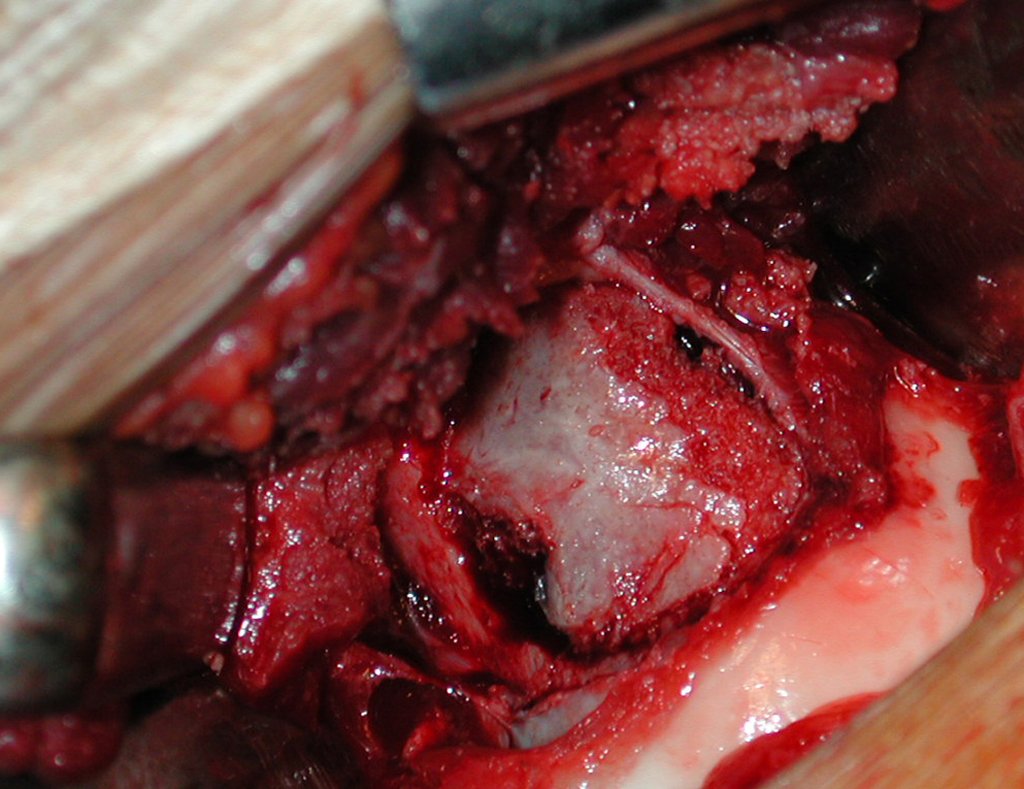
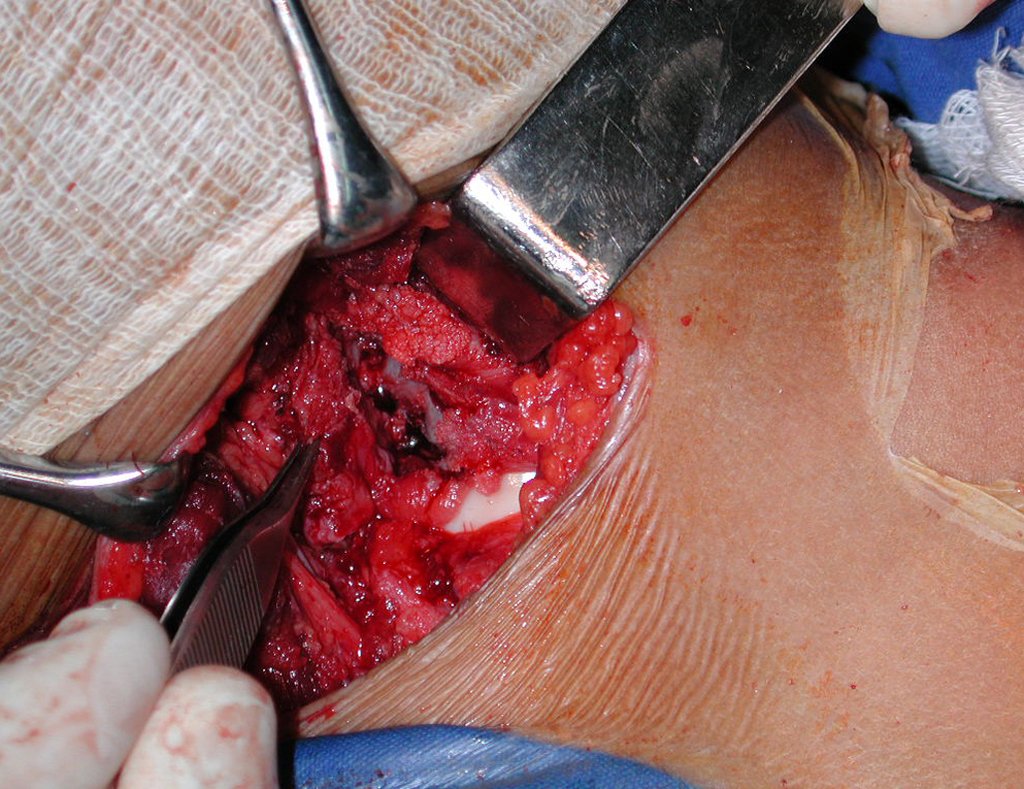
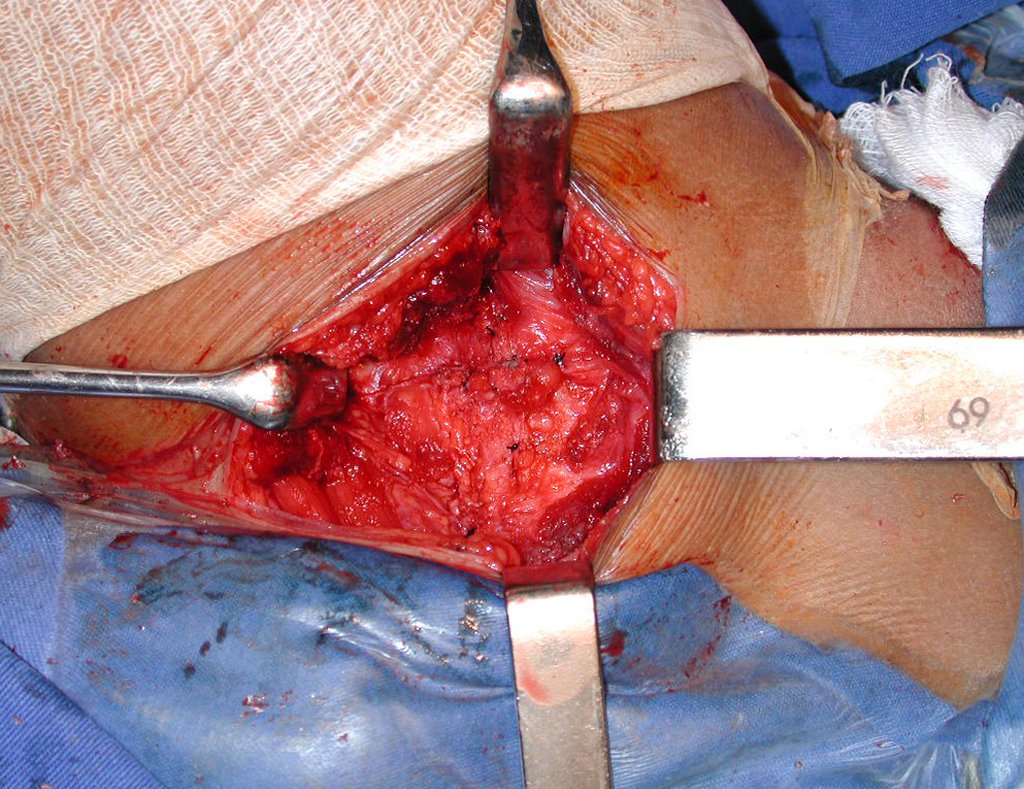
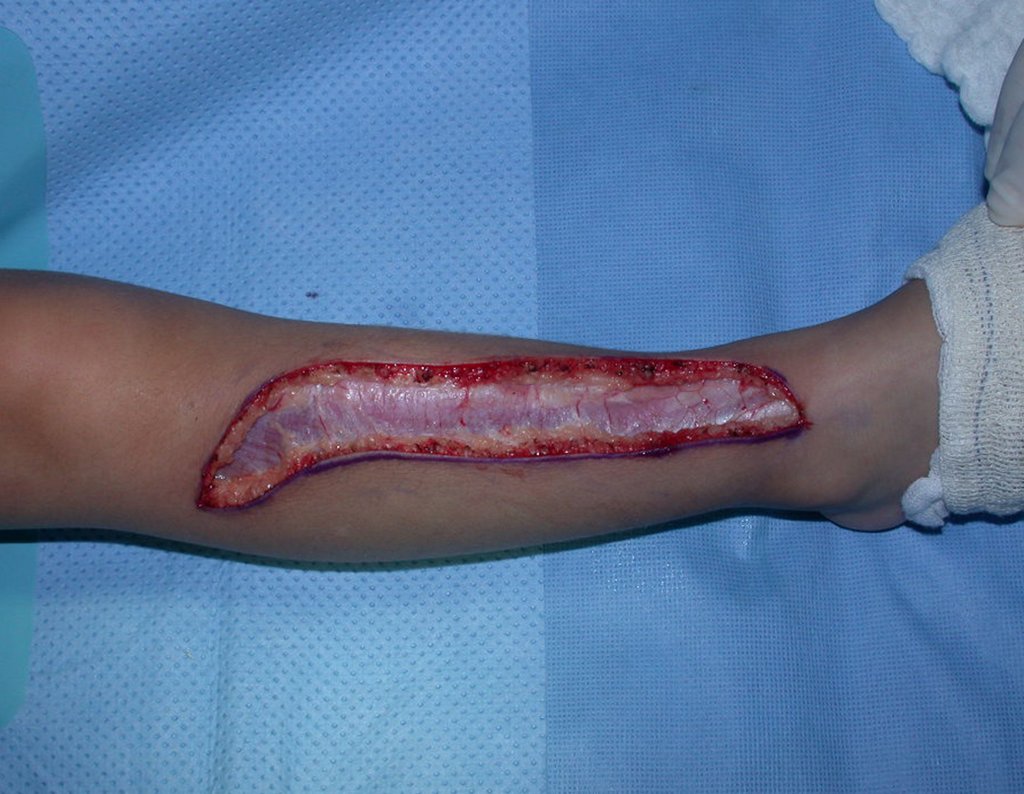
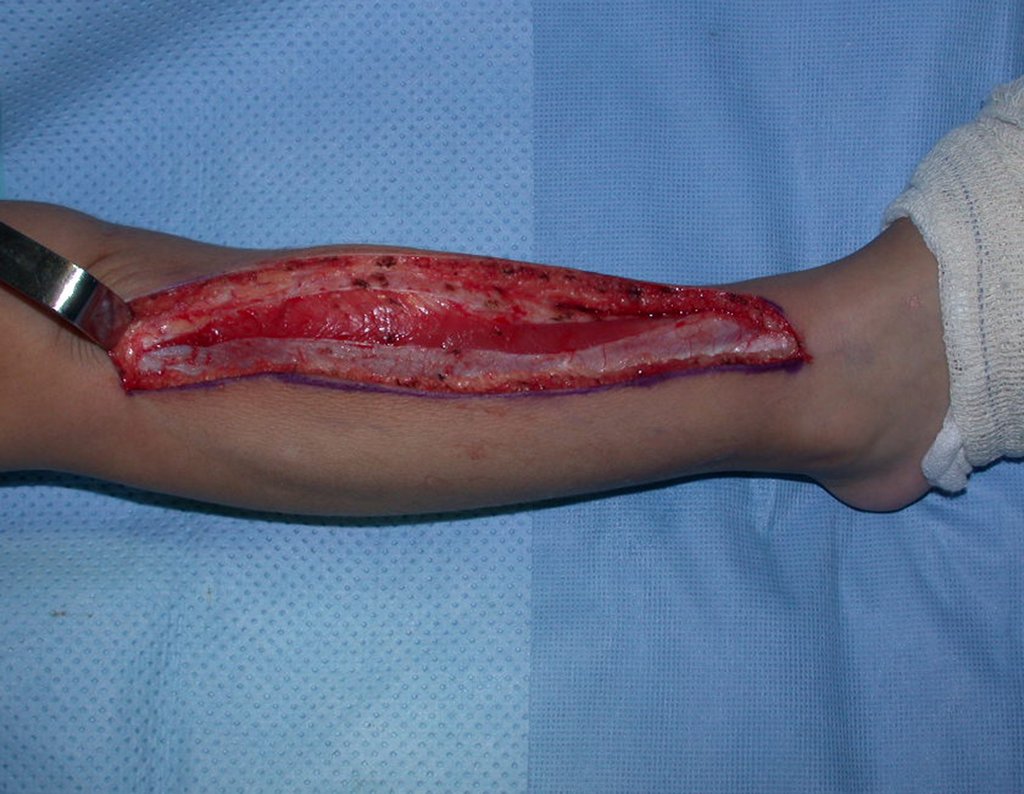
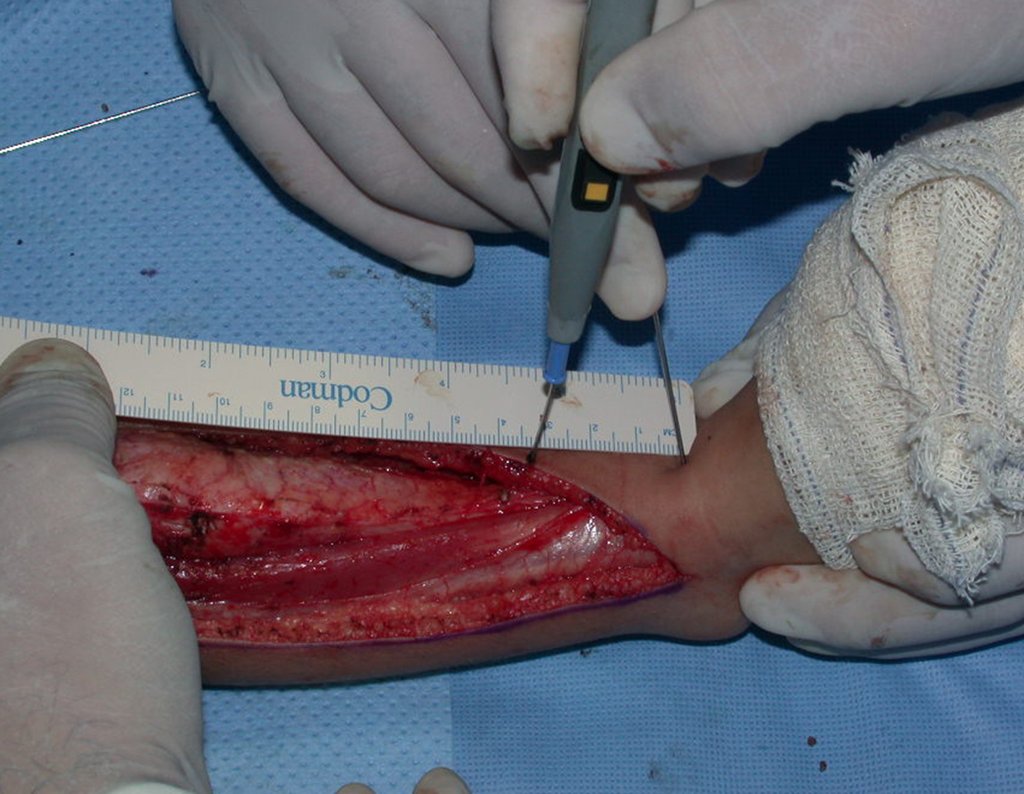
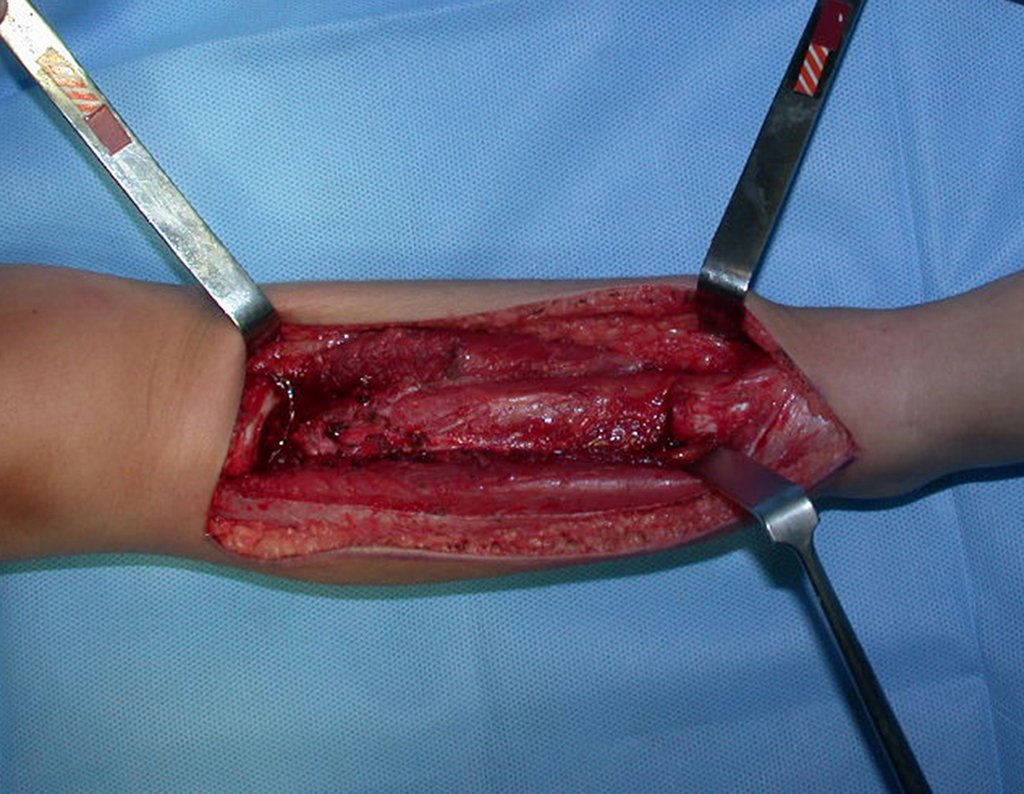
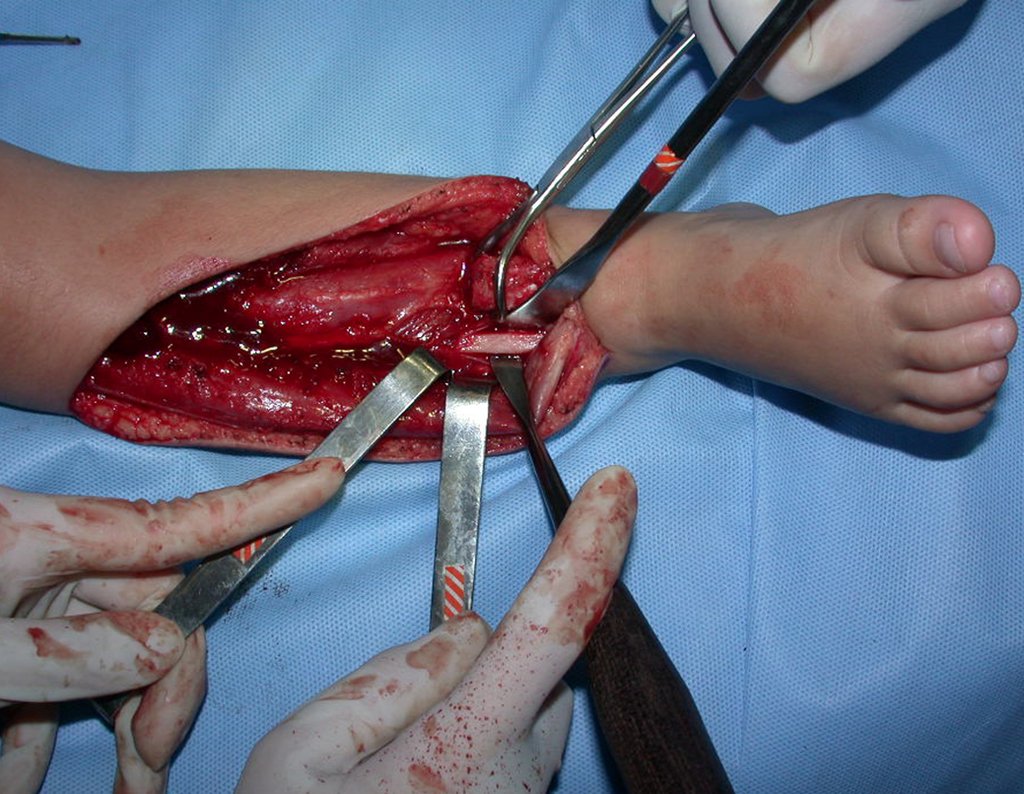
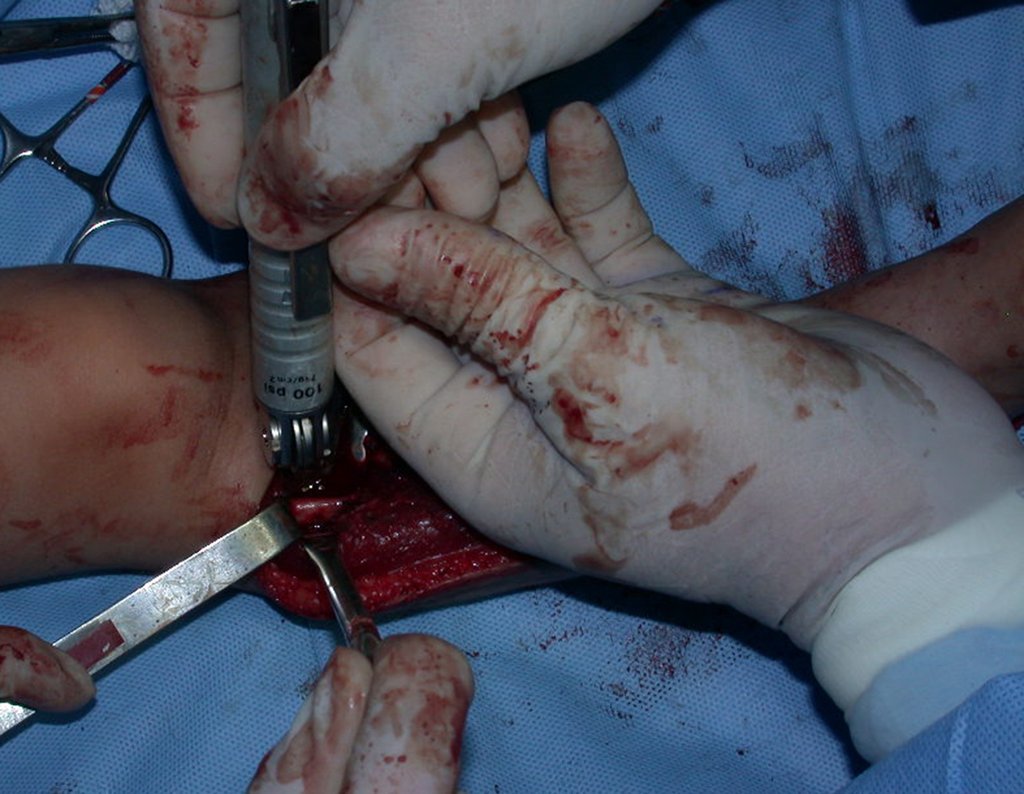
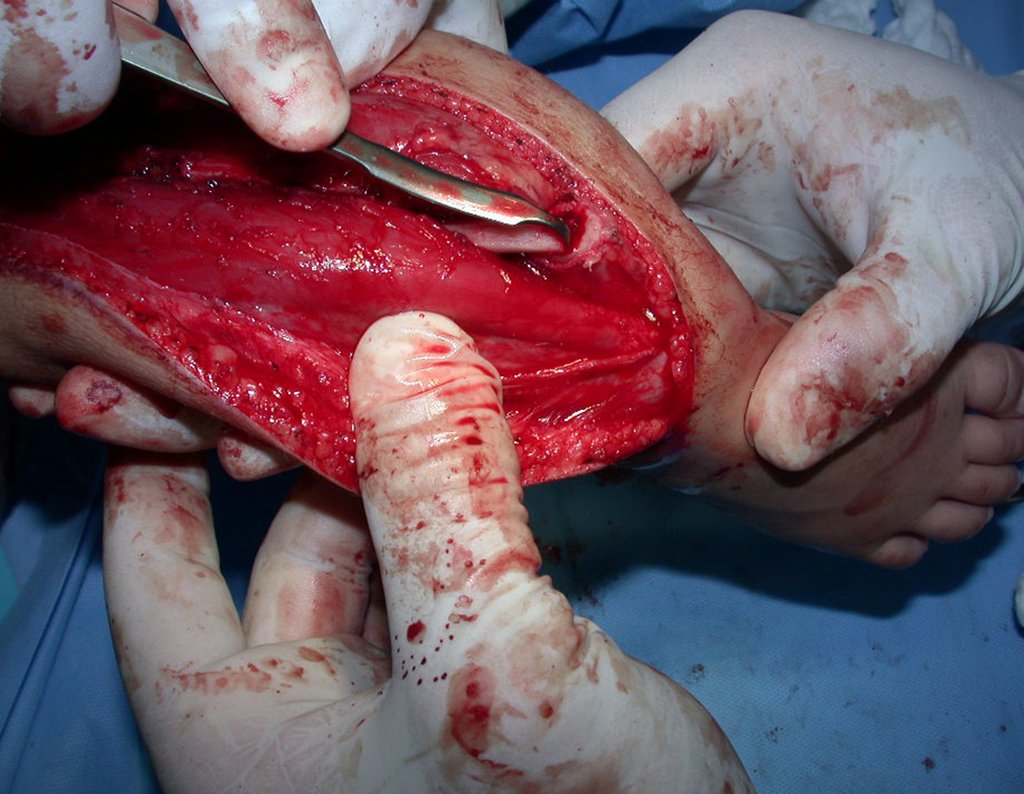
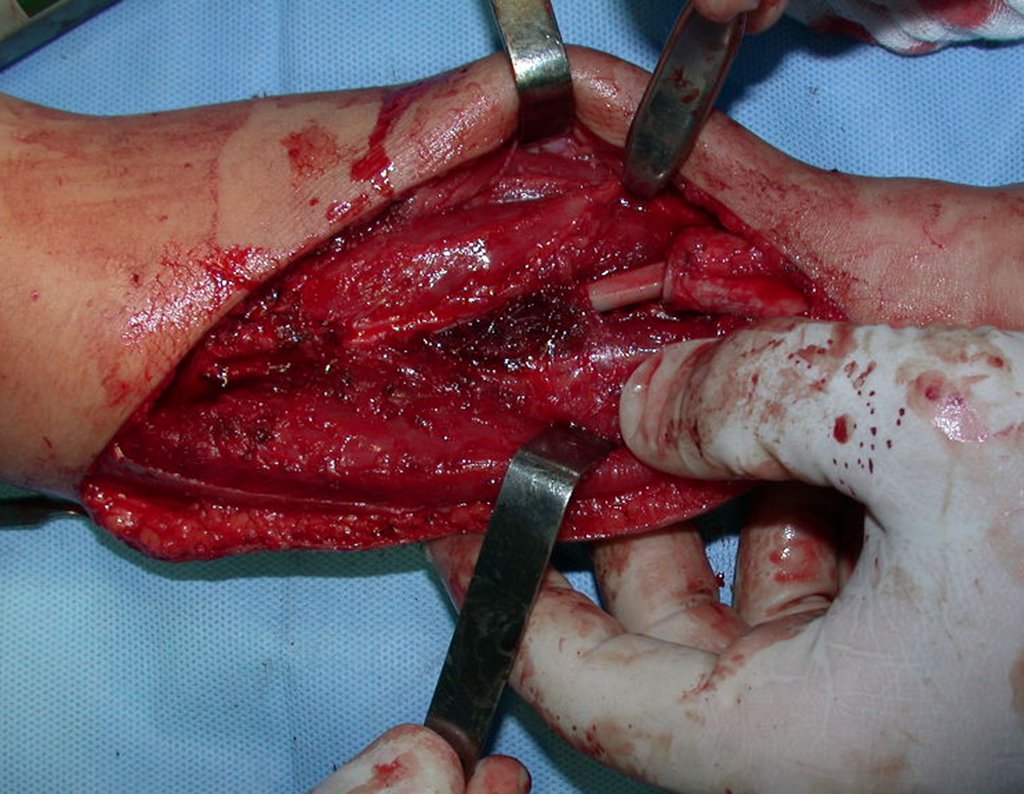
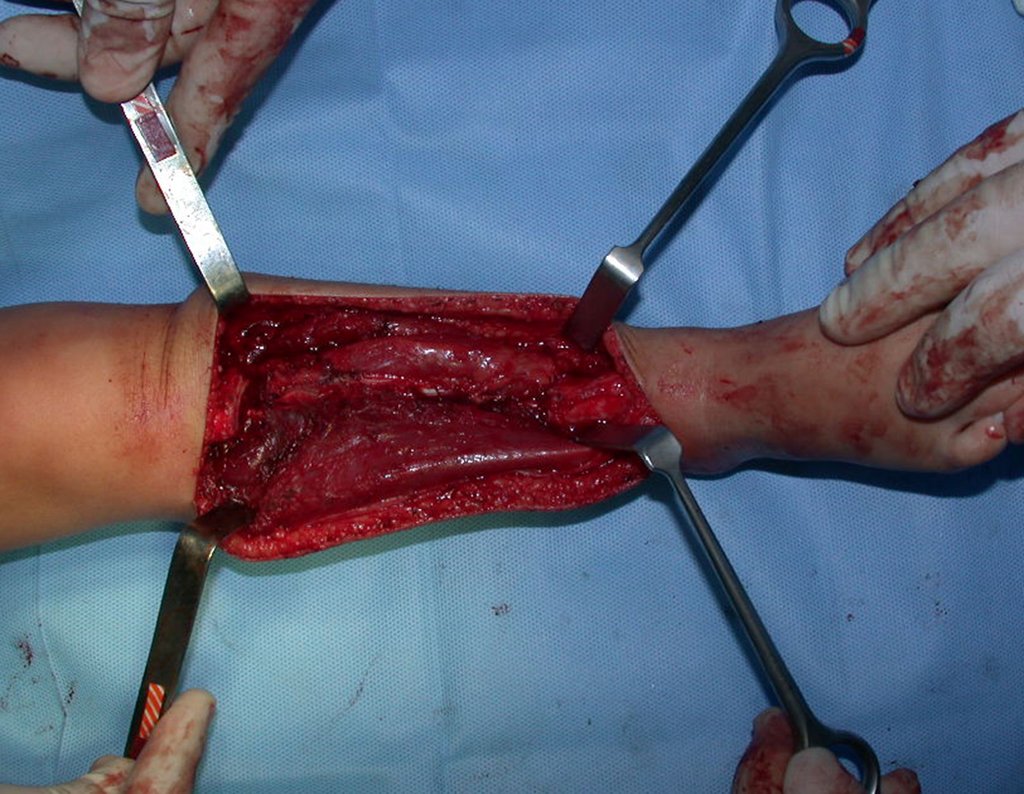
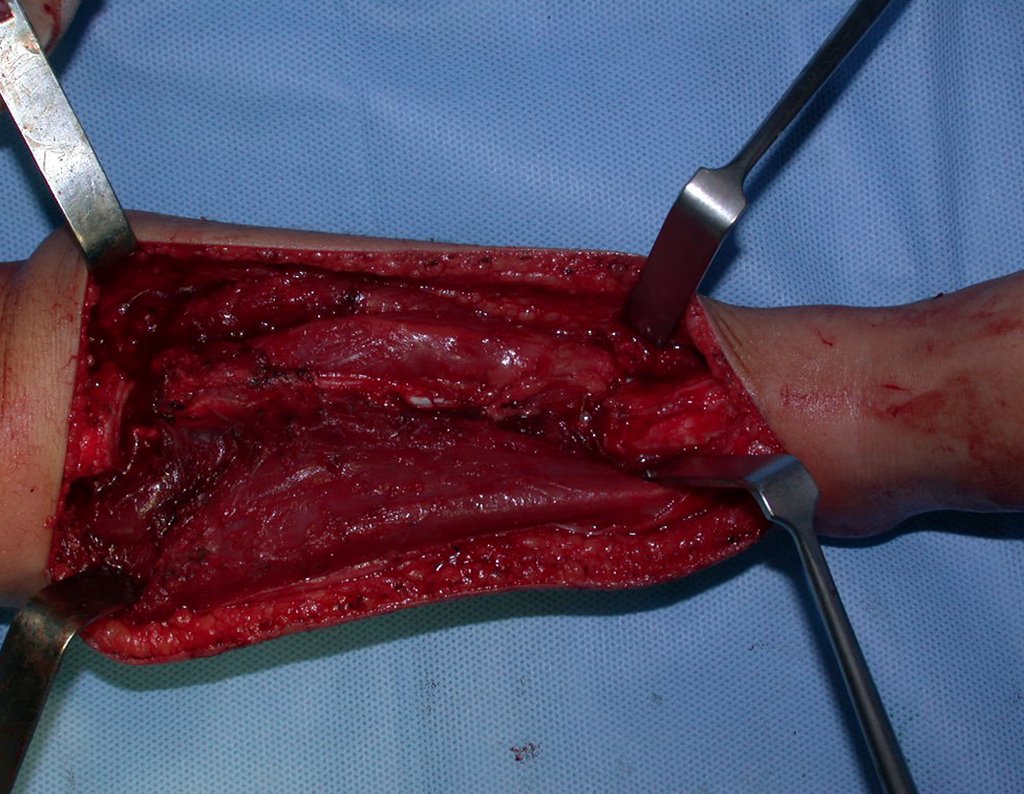
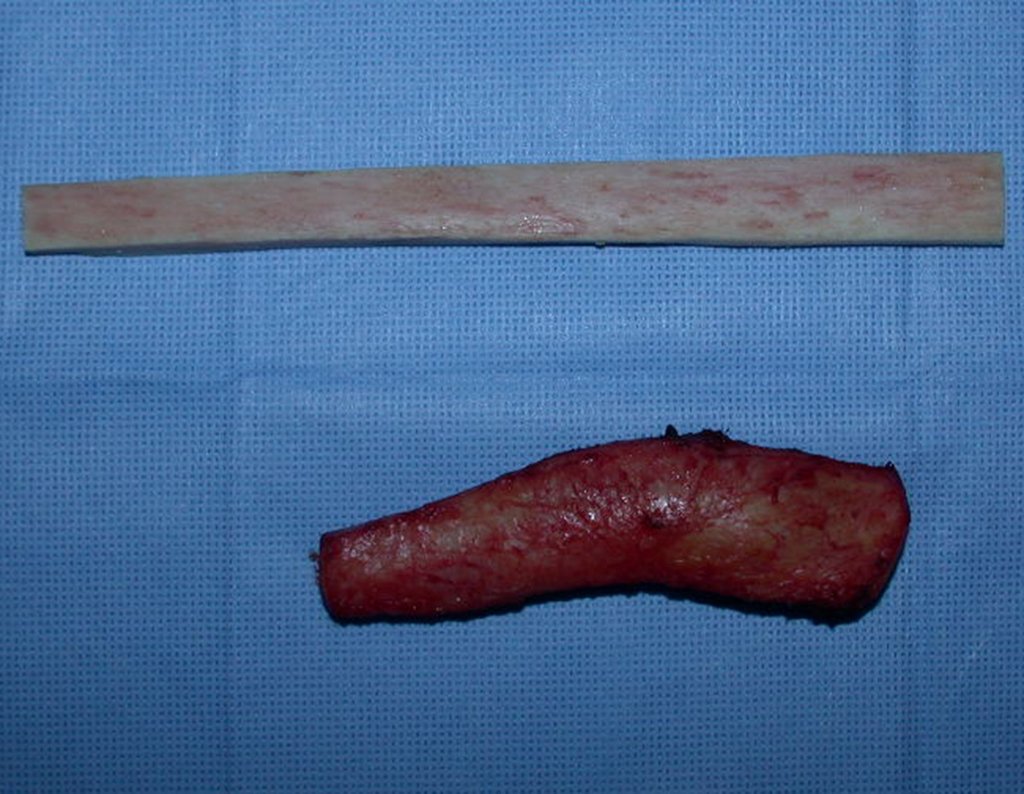
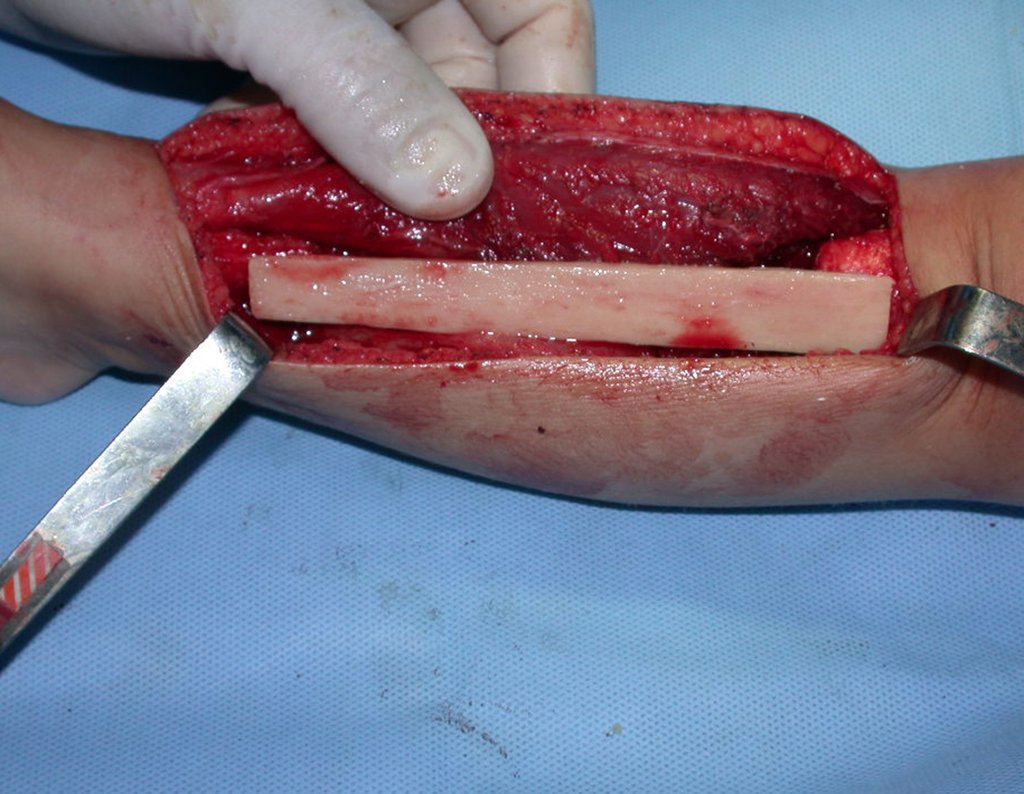
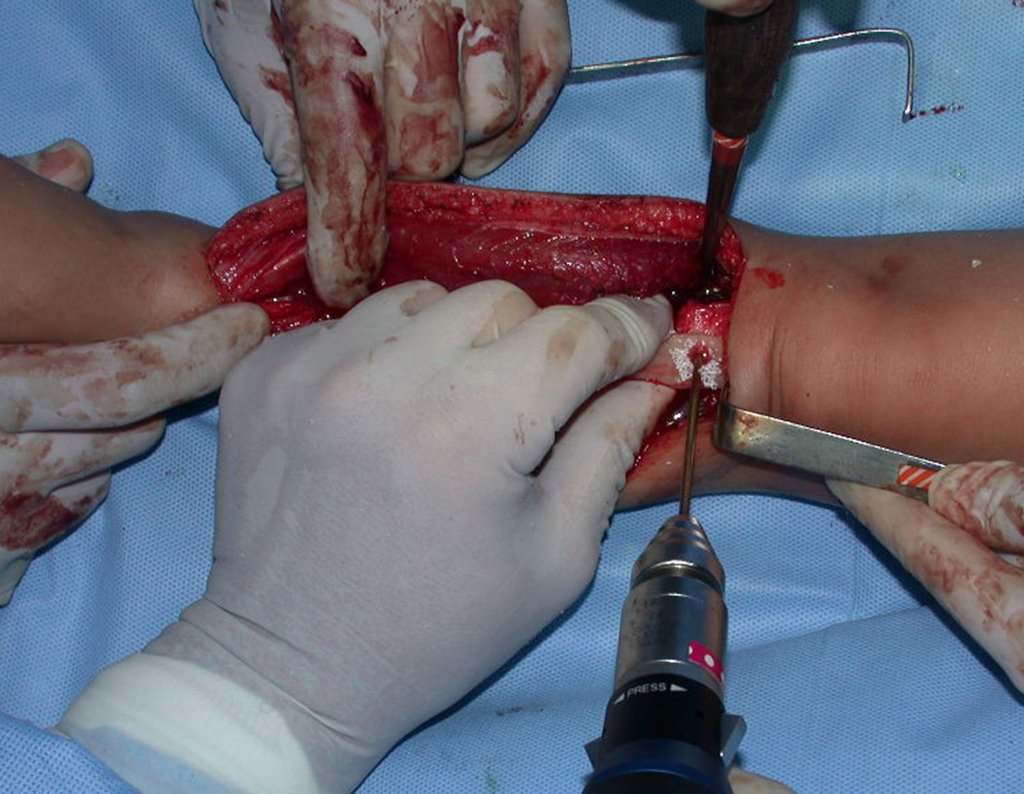
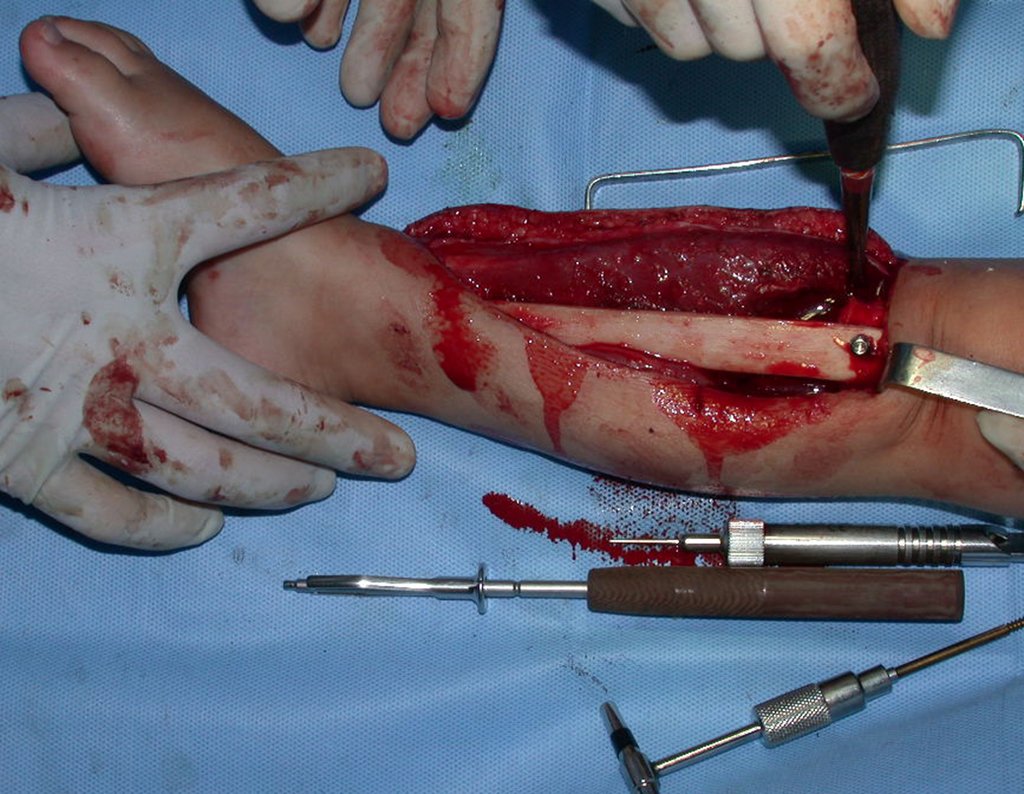
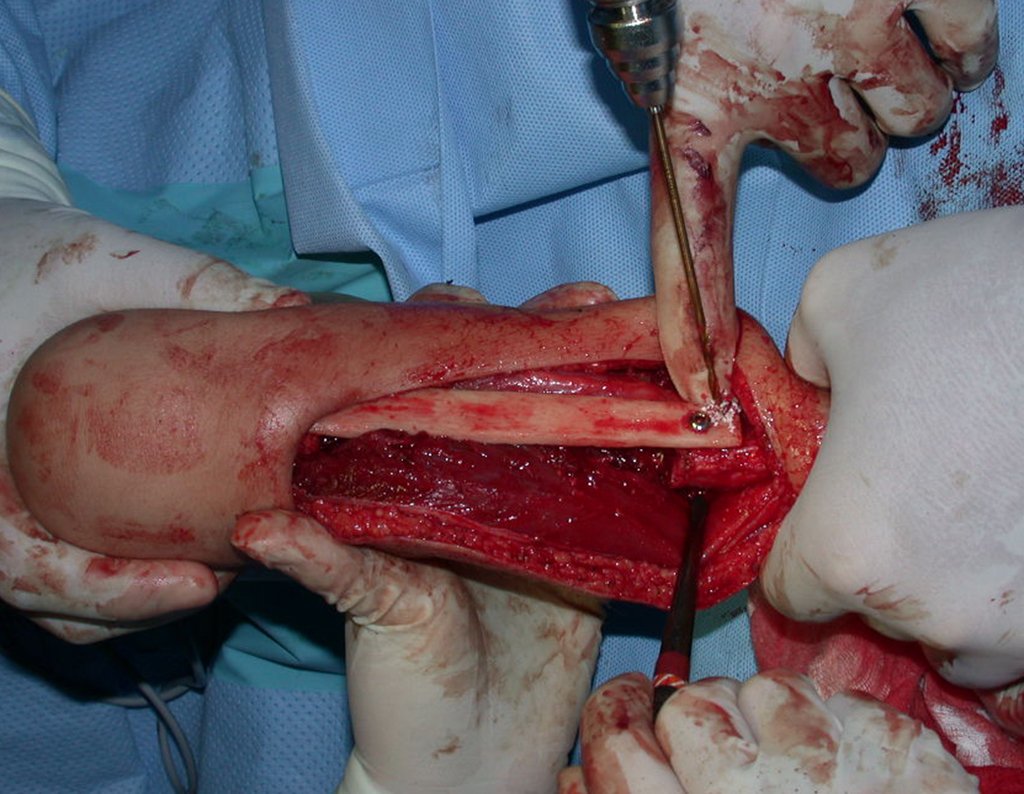
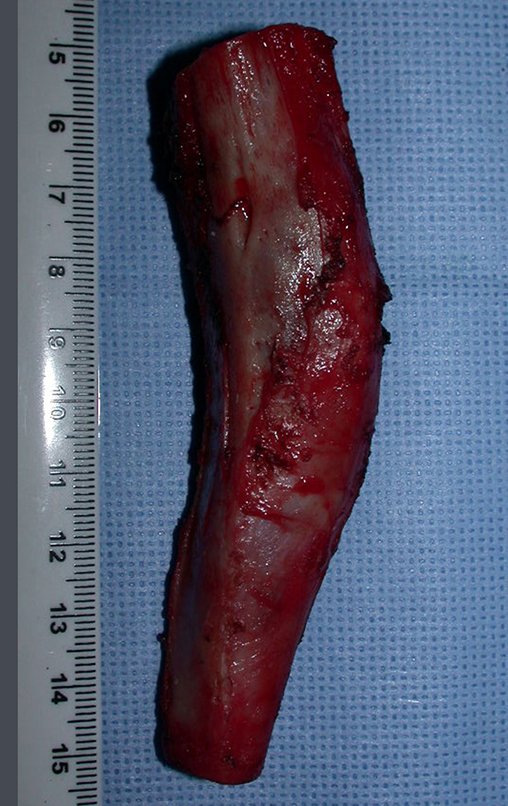
La cirugía de resección total del húmero izquierdo, incluyendo todo el músculo deltoides, y la reconstrucción con endoprótesis y malla de Marlex se pueden estudiar en las figuras 31 a 75.


El video 1 demuestra la reinserción del cable largo del músculo bíceps braquial.
Vídeo 1: Sutura de malla de Marlex alrededor de la glenoides.
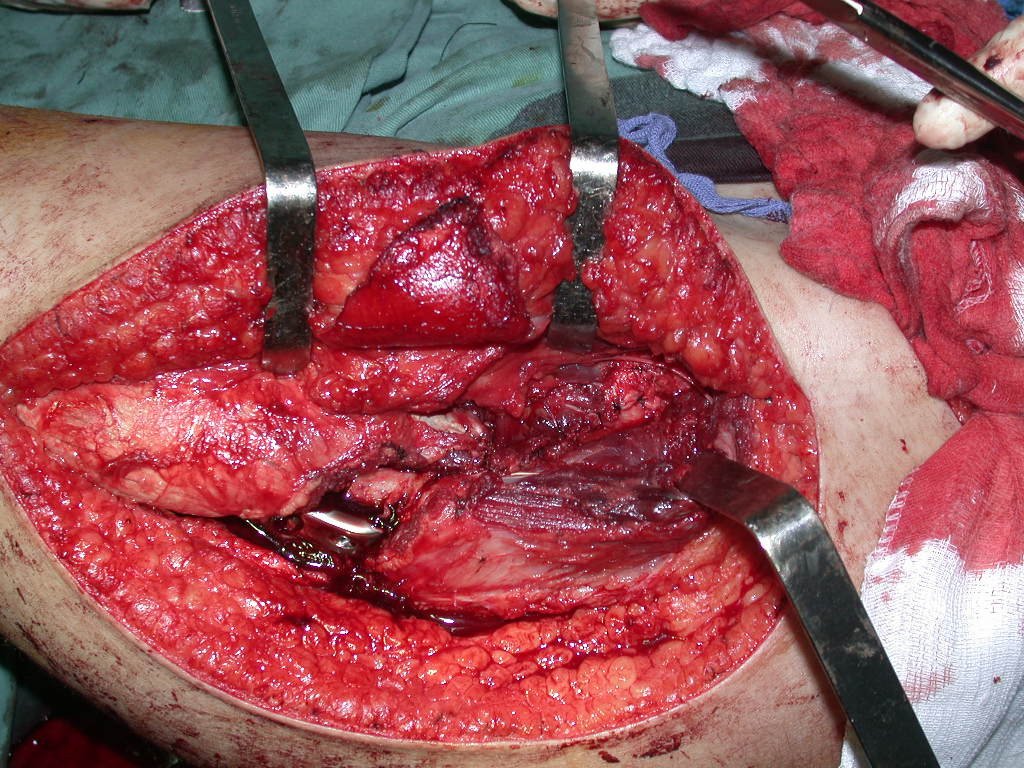
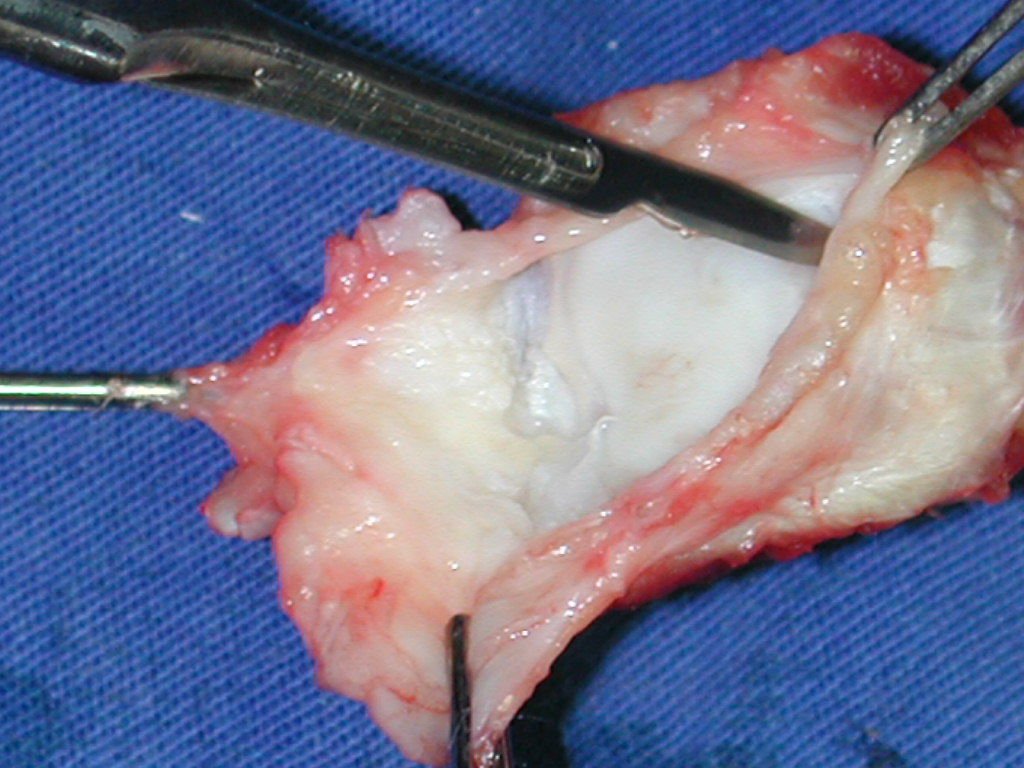
Como pudimos observar se resecó todo el músculo deltoides y el tracto de biopsia, junto con la cápsula articular. Sólo quedó piel y tejido celular subcutáneo para la cobertura proximal de la reconstrucción humeral.
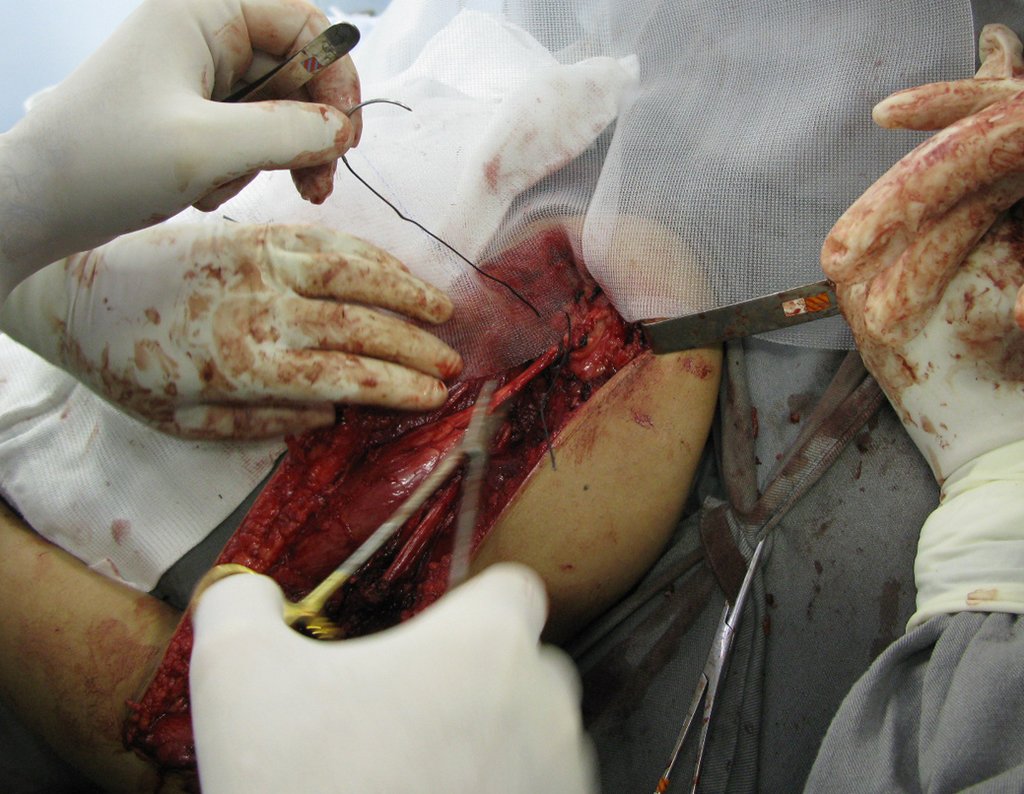
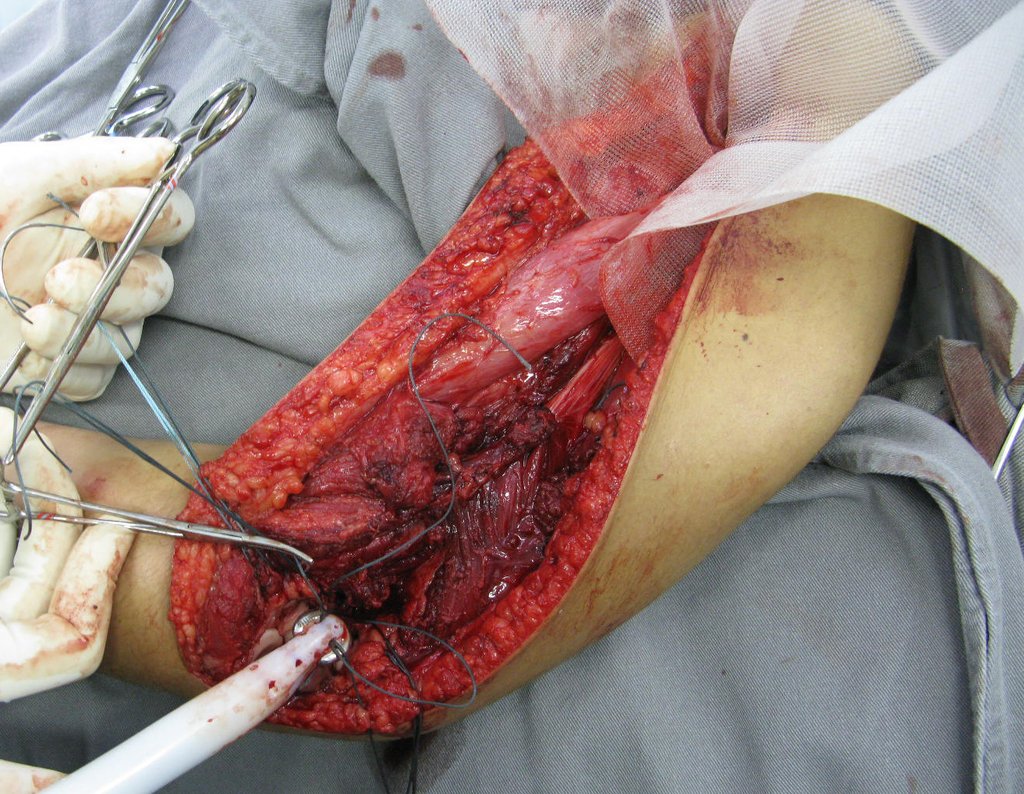
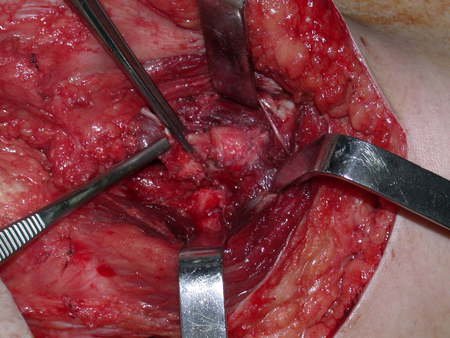
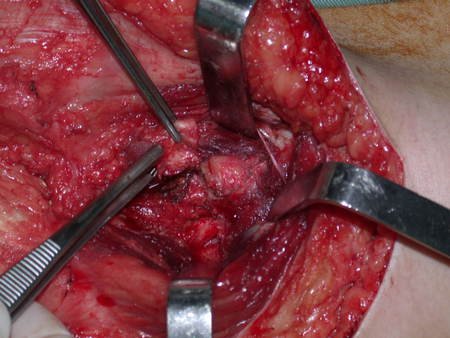
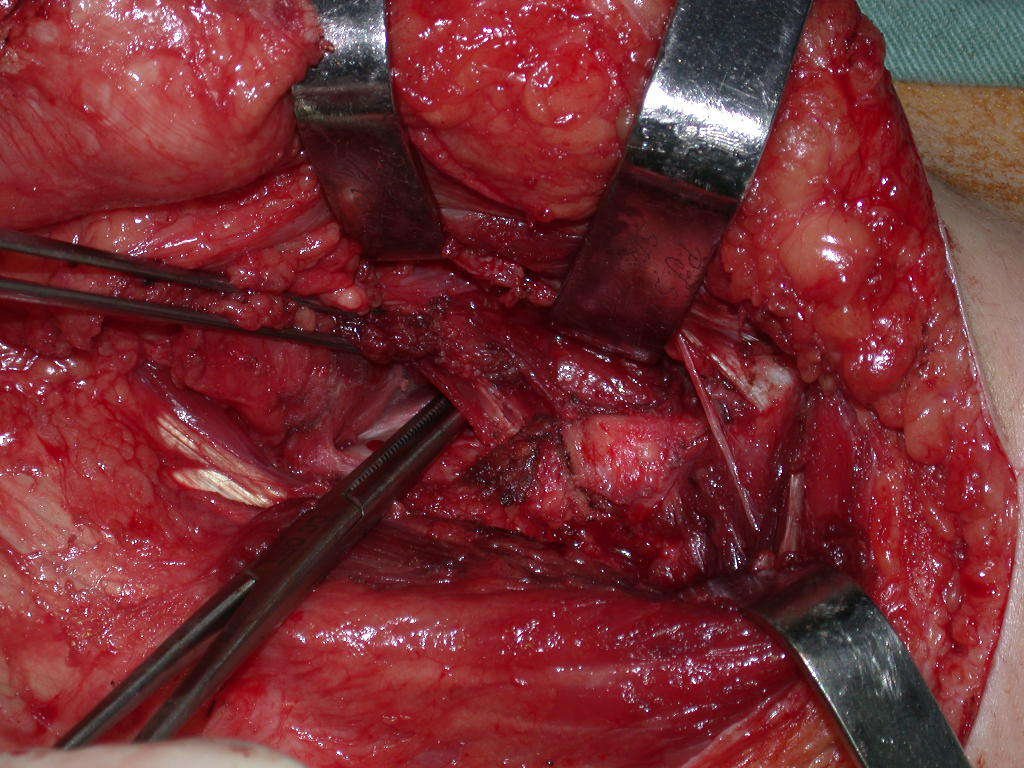
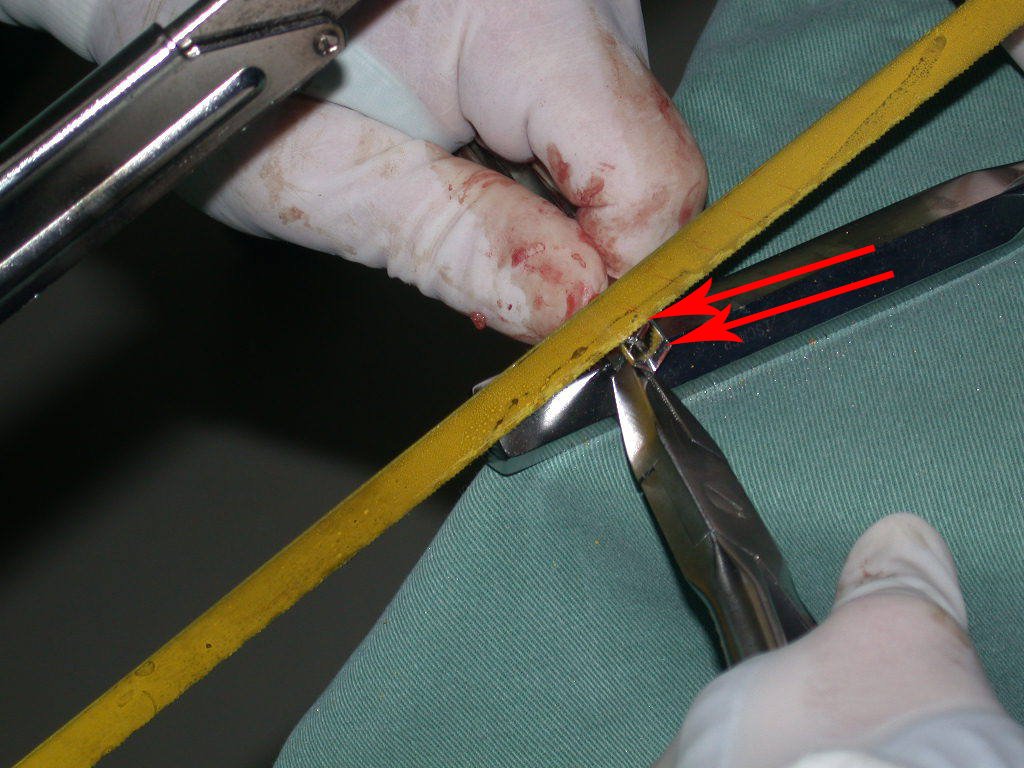
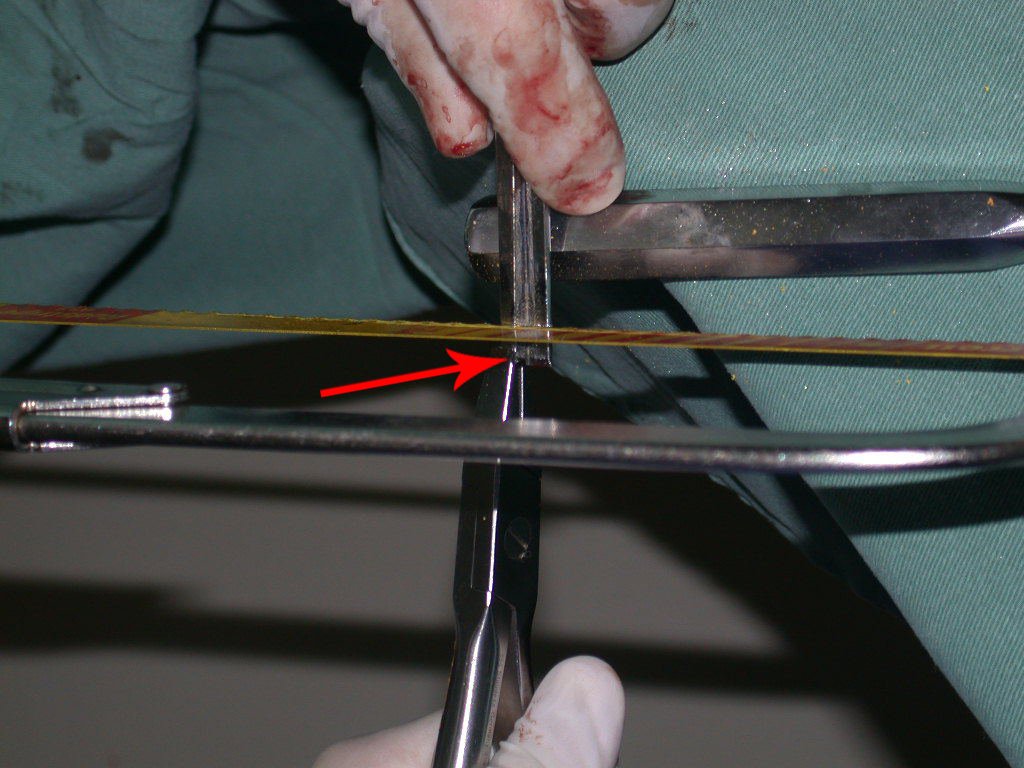
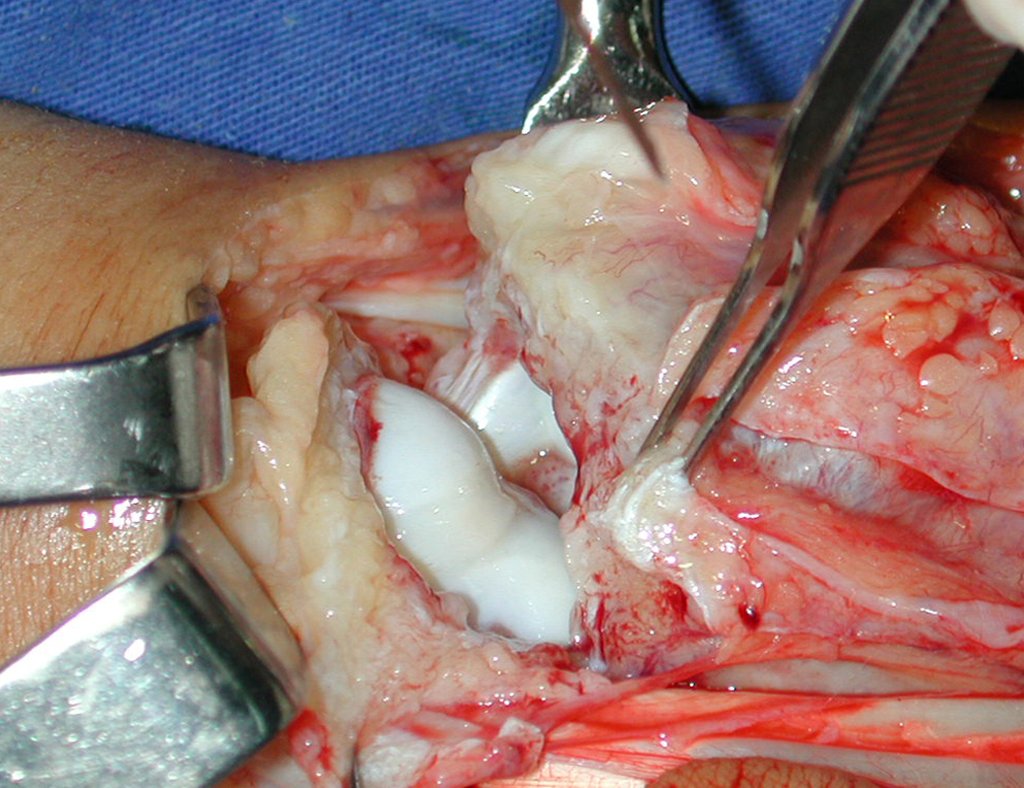
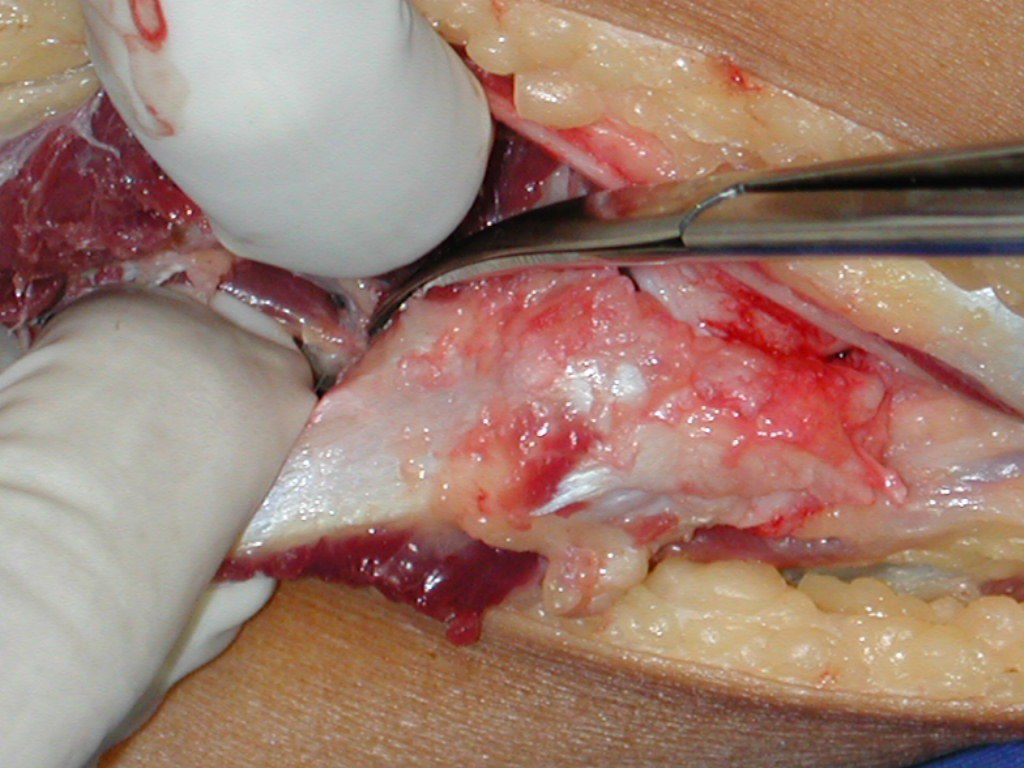
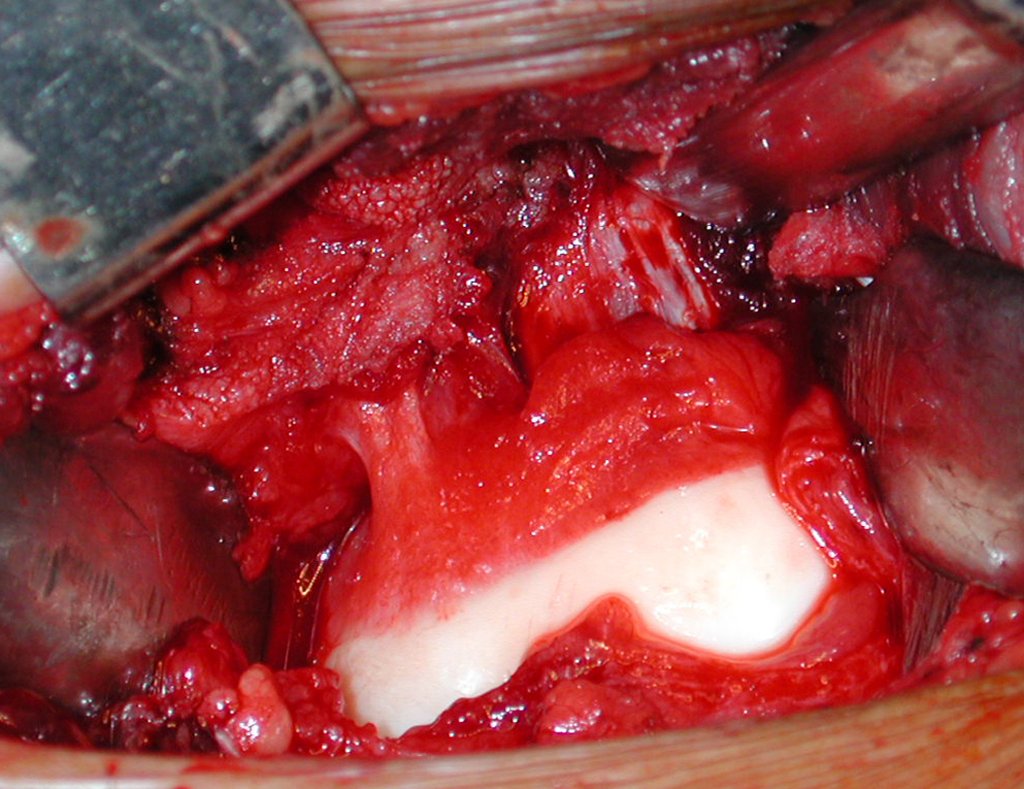
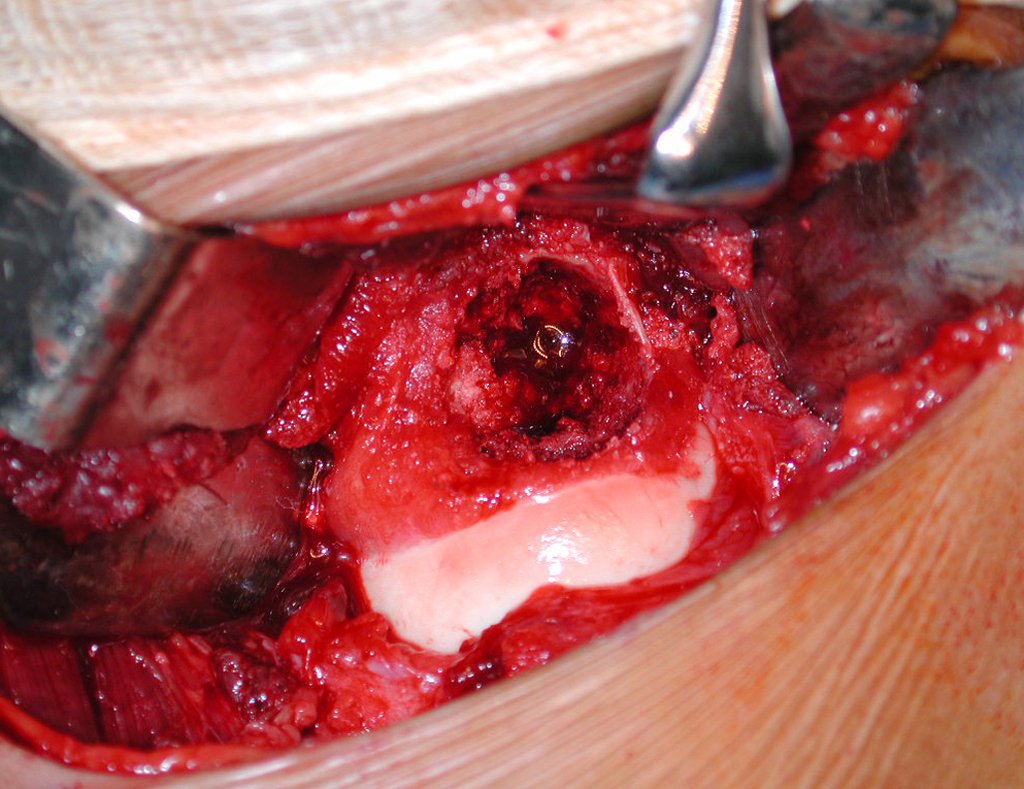
Es necesario crear una contención alrededor de la glenoidea para estabilizar la prótesis, evitando su desplazamiento. Este mecanismo de contención debe permitir los movimientos de rotación del húmero para proporcionar una función adecuada.
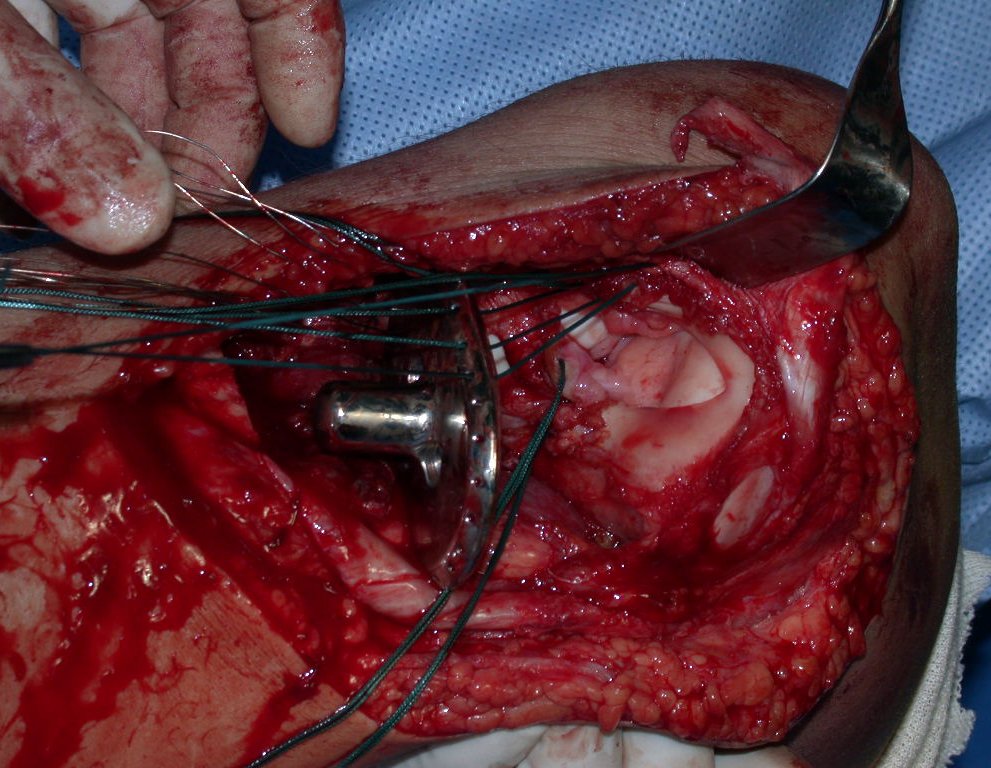
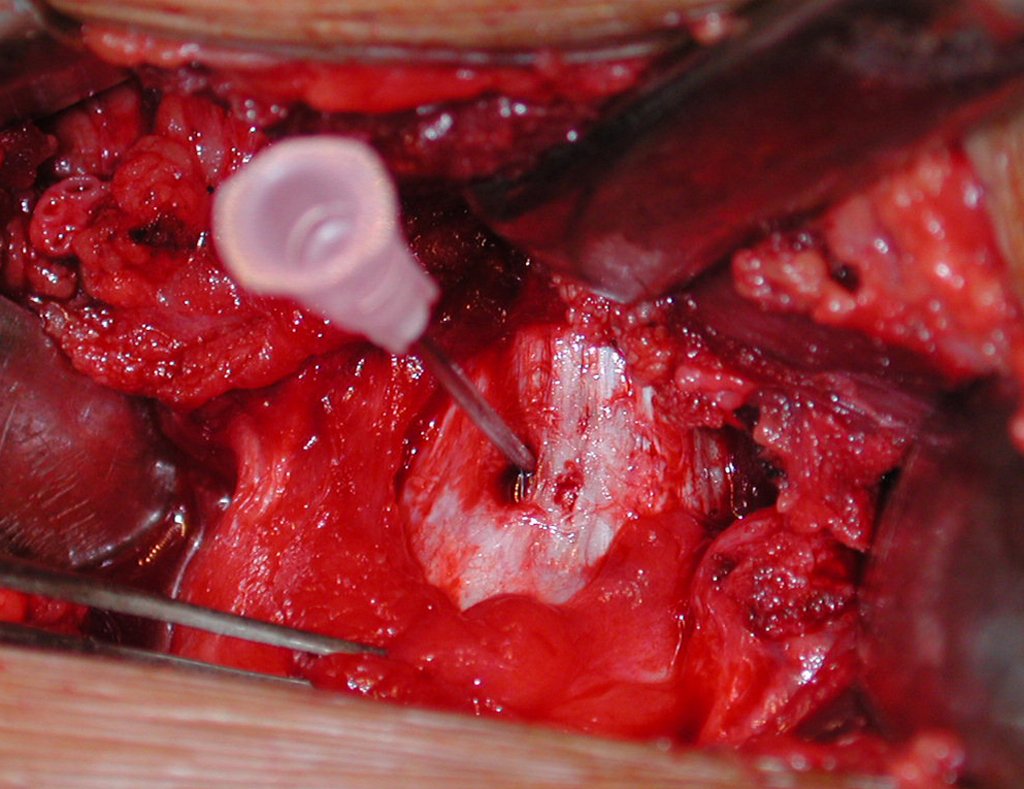
Para obtener este resultado describiremos nuestra técnica en detalle. El video 2 ilustra la sutura de una malla Marlex alrededor de la glenoides, con el objetivo de crear un punto de fijación para la porción proximal de la prótesis humeral que utilizamos en esta reconstrucción.
Video 2: Fijación de la malla Marlex en la porción anterior de la glenoidea.
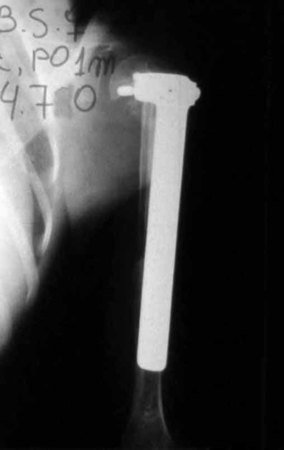
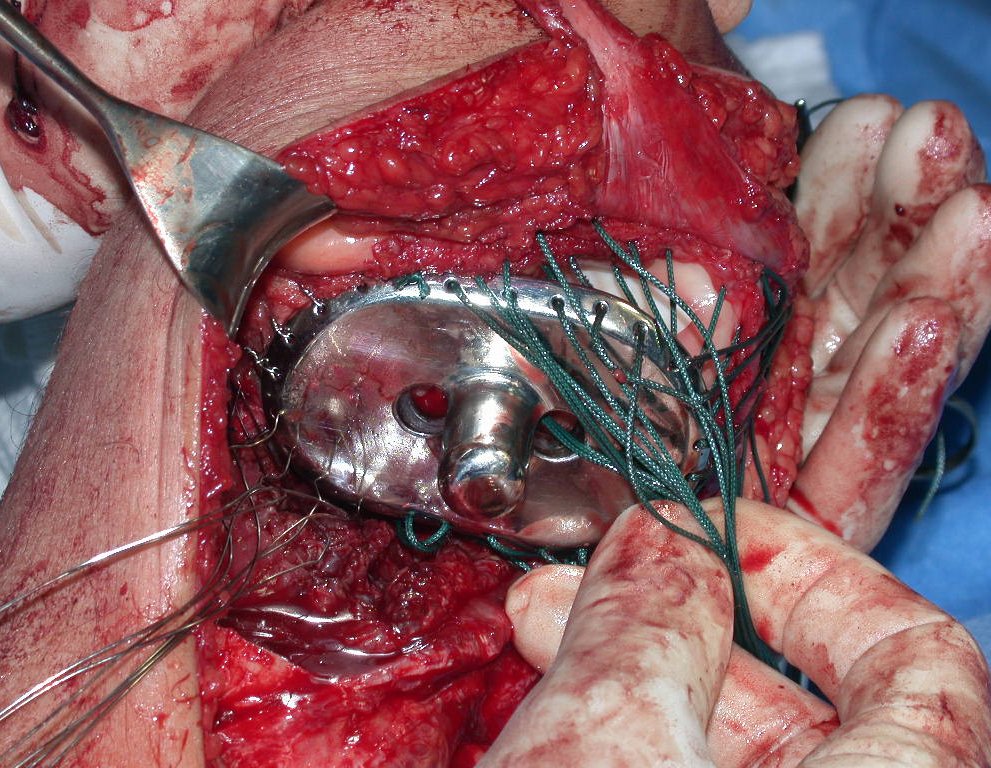
Vídeo 3: Cementación y montaje de la prótesis de húmero proximal, definiendo en este punto 20 grados de rotación interna. Hay un respiradero distal para que escape el exceso de cemento.
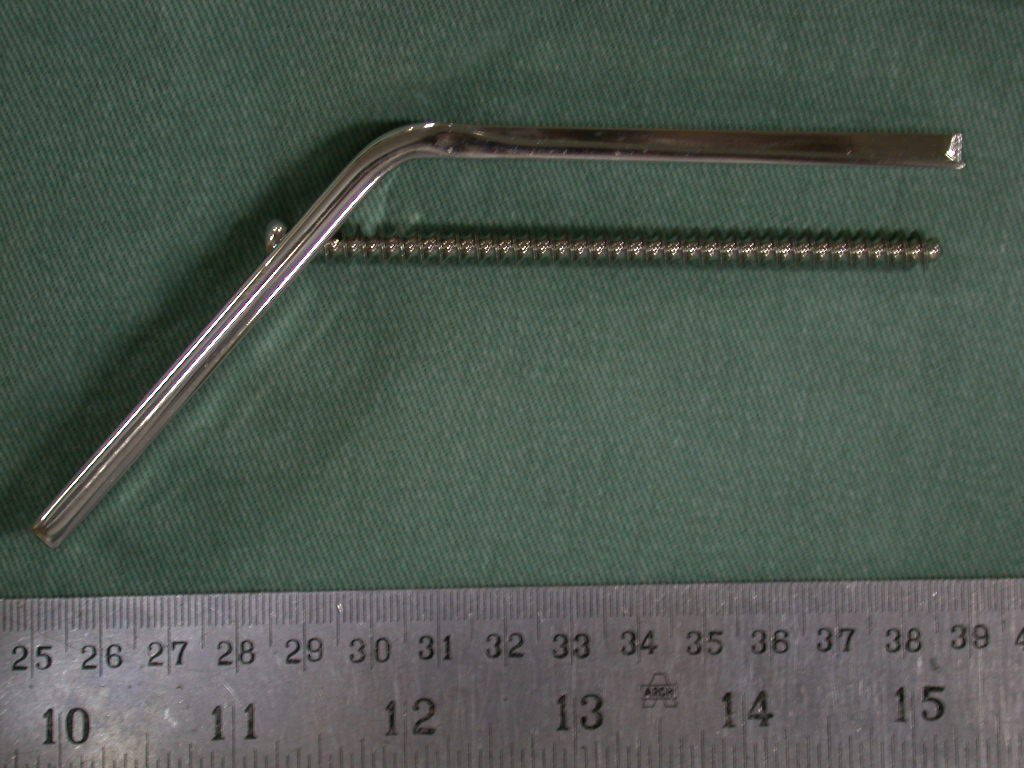
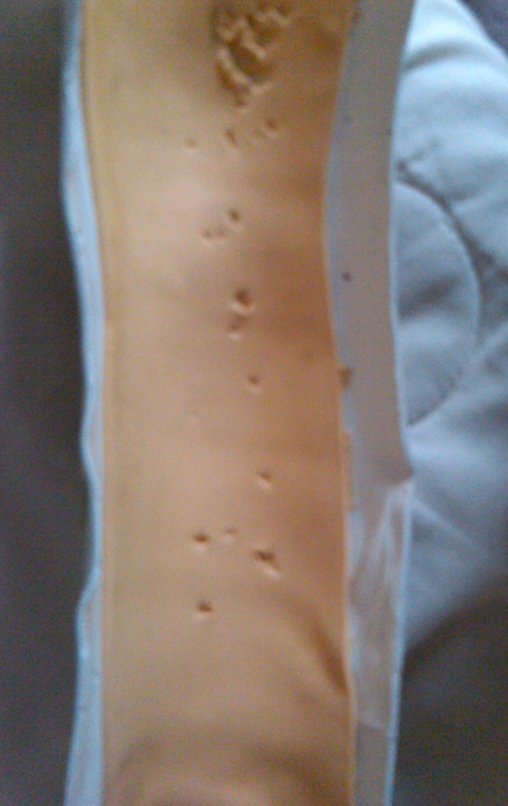
La prótesis de polietileno es más adecuada por su ligereza que una totalmente metálica. El polietileno tiene una elasticidad similar a la del hueso y nos permite crear orificios en puntos estratégicos para la reinserción de tendones y ligamentos, que pueden haber quedado acortados por la necesidad de un margen quirúrgico durante la resección.
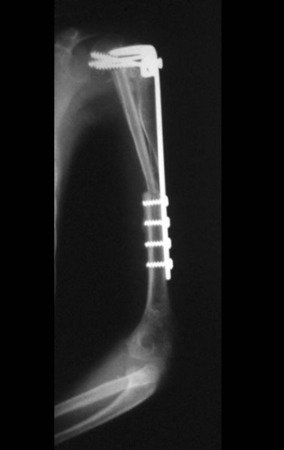
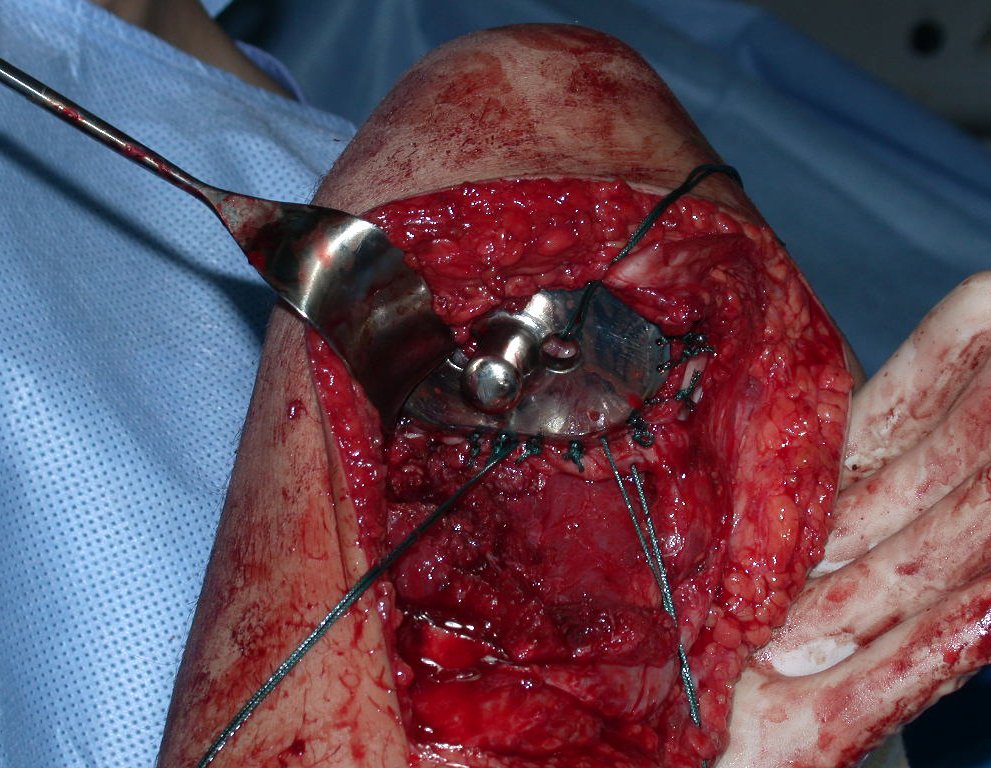
Video 4: Demostramos una buena fijación de los alambres y la malla Marlex en la región proximal de la prótesis humeral total. Esta sutura se realiza con un pliegue similar a una falda escocesa, para permitir movimientos de rotación.
Video 5: Paciente a una semana del postoperatorio, buen aspecto estético, iniciando fisioterapia.
Video 6: Función de la muñeca a los 15 días de la cirugía. Por ahora, realice únicamente movimientos de manos y muñecas.
Video 7: Función en agosto de 2015, nueve meses después de la resección total del húmero izquierdo, con escisión de todo el deltoides y reconstrucción con endoprótesis humeral total mediante malla Marlex, para estabilizar la prótesis de articulación gleno. Buena flexión del codo, excelente función y pronosupinación de la mano y buena rotación del húmero.
Vídeo 8: Paciente en fisioterapia, flexionando el hombro con ayuda del miembro contralateral, el 09/09/2015
Vídeo 9: Elevación de hombros con ayuda del balón y apoyo en la pared, el 09-09-2015
Autor: Profr. Dr. Pedro Péricles Ribeiro Baptista
Oncocirugía Ortopédica en el Instituto Oncológico Dr. Arnaldo Vieira de Carvalho
Oficina : Rua General Jardim, 846 – Cj 41 – Cep: 01223-010 Higienópolis São Paulo – SP
Teléfono: +55 11 3231-4638 Celular:+55 11 99863-5577 Correo electrónico: drpprb@gmail.com